
Charakteristiky Acinetobacter baumannii, morfologie, příznaky
Acinetobacter baumannii Je to gramnegativní bakterie patřící do řádu Pseudomonas. Během své taxonomické historie se nacházel v rodech Micrococcus, Moraxella, Alkaligeny, Mirococcuscalco-aceticus, Herellea Y Achromobacter, dokud nebyl uveden do svého současného žánru v roce 1968.
NA. baumannii je to patogenní bakterie, považovaná za druh, který se nejčastěji podílí na infekcích v rámci svého rodu. Bylo zjištěno, že se účastní různých typů infekcí, jako je septikémie, pneumonie a meningitida.
Jedná se o oportunního parazita, který má významný výskyt u nemocničních nebo nozokomiálních onemocnění. Přenos pomocí mechanické ventilace byl identifikován jako důležitá příčina nákazy, zejména u jednotek intenzivní péče.
Přestože je považován za patogen nízké kvality, má schopnost zvyšovat svou virulenci u kmenů zapojených do častých infekcí. Má velkou schopnost vyvinout rezistenci a multirezistenci na antibiotika.
V nemocnicích se přenáší hlavně kontaktem personálu, použitím kontaminovaných nemocničních materiálů a také vzduchem na krátké vzdálenosti.
Světová zdravotnická organizace zahrnuje A. baumannii na seznamu rezistentních patogenů, pro které jsou naléhavě nutná nová antibiotika, a zařazuje jej do kategorie 1 s kritickou prioritou.
Rejstřík článků
- 1 Charakteristika Acinetobacter baumannii
- 2 Morfologie
- 3 Metabolismus
- 4 Rezistence na antibiotika
- 5 Patologie
- 6 Příznaky
- 7 Léčba
- 8 Reference
Charakteristika Acinetobacter baumannii
Všechny druhy rodu Acinetobacter mají širokou distribuci v různých přírodních výklencích. A. baumannii může přirozeně obývat kůži zdravých lidí a být schopen kolonizovat povrchy sliznic, což představuje důležitý epidemiologický rezervoár. Stanoviště však A. baumannii je téměř výlučně v nemocničním prostředí.
Těmto bakteriím chybí bičíky nebo struktury používané pro pohyb. Dosahují však pohybu strukturami, které jim umožňují vysouvat a zatahovat, a chemickými mechanismy, jako je vylučování filmu exopolysacharidu s vysokou molekulovou hmotností za bakteriemi..
A. baumannii může kolonizovat velké množství živých nebo inertních prostředí a má velkou schopnost přežít na umělých površích po delší dobu.
Tato schopnost je možná způsobena jejich schopností odolávat dehydrataci, využívat různé zdroje uhlíku různými metabolickými cestami a schopností vytvářet biofilmy. Z tohoto důvodu je běžné jej najít v nemocničním materiálu, jako jsou katétry a zařízení pro mechanickou ventilaci..
Morfologie
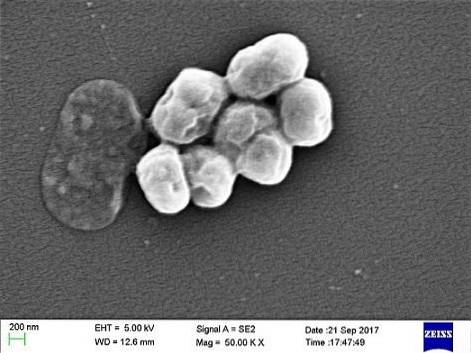
A. baumannii je coccobacillus, se středním tvarem mezi koky a pruty. Měří 1,5 až 2,5 až 1 až 1,5 mikronu, když jsou populace v logaritmické fázi růstu. Když dosáhnou stacionární fáze, jsou sférickější.
Metabolismus
Bakterie A. baumannii není to fermentor glukózy; je přísný aerobní, to znamená, že pro svůj metabolismus vyžaduje kyslík.
Druh rodu Acinetobacter jako jediní z čeledi Moraxellaceae postrádají cytochrom c oxidázy, pro které dávají negativní výsledky v oxidázových testech.
A. baumannii roste při teplotách, které se pohybují mezi 20 a 44 ° C, což je optimální teplota mezi 30 a 35 ° C.
Odolnost vůči antibiotikům
Neustálé vytváření rezistence na antibiotika nejen brání léčbě a kontrole infekcí způsobených A. baumannii, také podporuje výběr endemických a epidemických multirezistentních kmenů.
Některé vnitřní mechanismy A. baumannii, které podporují rezistenci na antibiotika:
- Přítomnost někoho β-laktamázy propůjčují rezistenci vůči b-laktamům.
- Produkce specifických enzymů, jako je amoniglukosid-3'-fosfotransferáza VI, deaktivuje amikacin.
- Přítomnost oxacilinázy OXA-51 hydrolyzuje peniciliny a karbapenemy.
- Přítomnost a nadměrná exprese refluxních pump, což jsou pumpy, které vylučují malé molekuly z buňky, kterým se podaří proniknout do cytoplazmy, čímž se sníží jejich citlivost na antibiotika..
Biofilmy generované A. baumannii změnit metabolismus mikroorganismů, snížit jejich citlivost na antibiotika, kromě toho vytvořit fyzickou bariéru proti velkým molekulám a zabránit dehydrataci bakterií.
Patologie
A. baumannii kolonizuje nového hostitele kontaktem s infikovanými lidmi nebo s kontaminovaným lékařským vybavením. Nejprve se tato bakterie váže na povrch kůže a sliznic. Aby se mohl reprodukovat, musí přežít antibiotika a inhibitory a podmínky těchto povrchů..
Zvýšení počtu bakterií na sliznicích, zejména při hospitalizaci v kontaktu s intravaskulárními katétry nebo endotracheálními trubicemi, může zvýšit riziko infekce dýchacích cest a krevního řečiště..
Nemocniční pneumonie je nejčastější z infekcí způsobených A. baumanii. Obvykle se uzavírají na jednotkách intenzivní péče u pacientů, kteří dostávají mechanicky asistované dýchání.
A. baumanii také to způsobilo velké problémy s infekcí u vojenského personálu s poválečným traumatem, konkrétně v Iráku a Afghánistánu. Konkrétně kvůli osteomyelitidě a infekcím měkkých tkání, které mohou způsobit nekrózu a celulitidu.
Existuje také riziko meningitidy z A. baumanii u pacientů zotavujících se z neurochirurgie.
Jednotlivci náchylní k infekcím A. baumanii zahrnout ty, kteří byli dříve podrobeni používání antibiotik, větších operací, popálenin, traumat, imunosuprese nebo použití invazivních zdravotnických prostředků, zejména mechanické ventilace, na jednotkách intenzivní péče.
Příznaky
Neexistuje žádná specifická symptomatologie infekcí A. baumanii. Každá z různých infekcí produkovaných touto bakterií má své vlastní charakteristické příznaky..
Obecně příznaky infekcí, které mohou zahrnovat A. baumanii nebo jiné oportunistické bakterie jako např Klebsiella pneumoniae Y Streptococcus pneumoniae, může zahrnovat horečku, zimnici, vyrážku, bolestivé močení, naléhavou potřebu častého močení, zmatenost nebo změny duševních stavů, nevolnost, bolest svalů, bolest na hrudi a kašel.
Léčba
Antibiotika k léčbě infekcí A. baumannii jsou extrémně omezené kvůli své velké schopnosti získávat rezistory a multirezistory. Z tohoto důvodu je důležité určit citlivost každého kmene na různá antibiotika, aby byla zaručena účinnost každé léčby..
Vzhledem k rezistenci na karbapenemy se uchýlilo k použití polymyxinů, konkrétně kolistinu, přestože má relativně nízký index rezistence a jeho vedlejší účinky na ledviny.
Kmeny rezistentní na kolistin však již byly detekovány. Jako alternativa k rezistenci na tato antibiotika byla použita kombinovaná léčba.
Reference
- Bergogne-Bérézin, E. & Towner, K.J.. Acinetobacter spp. jako nozokomiální patogeny: mikrobiologické, klinické a epidemiologické rysy. Clin Microbiol Rev, 9 (1996), str. 148-165.
- Fournier, P.E., Richet, H. (2006). Epidemiologie a kontrola Acinetobacter baumanii ve zdravotnických zařízeních. Clinical Infection Diseases, 42: 692-9.
- Hernández Torres, A., García Vázquez, E., Yagüe, G. &, Gómez Gómez, J. (2010) Acinetobacter baumanii Multirezistentní: současná klinická situace a nové perspektivy Revista Española de Quimioterapia, 23 (1): 12-19.
- Maragakis LL, Perl TM. Acinetobacter baumanii: Epidemiologie, antimikrobiální rezistence a možnosti léčby. Clin Infec Dis 2008; 46: 1254-63.
- McConnell, M.j., Actis, L. & Pachón, J. (2013) Acinetobacter baumannii: lidské infekce, faktory přispívající k patogenezi a zvířecí modely. FEMS Microbiology Reviews, 37: 130-155.
- Peleg, A.Y., Seifert, H. & Paterson, D.L. (2008). Acinetobacter baumannii: vznik úspěšného patogenu. Recenze klinické mikrobiologie, 21 (3): 538-82.
- Vanegas-Múnera, J.M., Roncancio-Villamil, G. & Jiménez-Quiceno, J.N. (2014). Acinetobacter baumannii: klinický význam, mechanismy rezistence a diagnóza. CES Medicine Magazine, 28 (2): 233-246.



Zatím žádné komentáře