
Vlastnosti, struktura a funkce domény SH2
The SH2 doména (Homologie Src 2) je vysoce konzervovaná proteinová doména ve vývoji a je přítomna ve více než 100 různých proteinech, z nichž nejvýznamnější je onkoprotein src, který se účastní procesu signální transdukce v buňce.
Funkce domény se váže na fosforylované tyrosinové sekvence na cílových proteinech; Toto spojení spouští řadu signálů, které regulují expresi genů. Tato doména byla také nalezena v enzymu tyrosin fosfatázy.
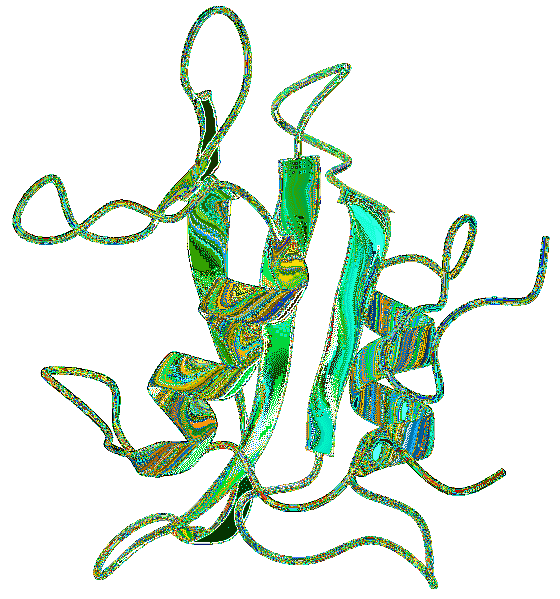
Domény SH2 se obecně nacházejí společně s dalšími doménami, které byly spojeny se signálními transdukčními cestami. Jednou z nejběžnějších interakcí je spojení s doménou SH2 a SH3, která se zdá být zapojena do regulace interakce se sekvencemi bohatými na prolin..
Proteiny mohou obsahovat jednu doménu SH2 nebo více než jednu, jako je například protein GAP a podjednotka p85 fosfoinositol 3-kináz..
Doména SH2 byla ve farmaceutickém průmyslu široce studována za účelem výroby léků pro boj s nemocemi, jako je rakovina, alergie, autoimunitní onemocnění, astma, AIDS, osteoporóza..
Rejstřík článků
- 1 Funkce
- 2 Struktura
- 3 funkce
- 4 Evoluce
- 5 Klinické důsledky
- 5.1 X-vázaný lymfoproliferativní
- 5.2 X-vázaná agamaglobulinemie
- 5.3 Noonanův syndrom
- 6 Reference
Vlastnosti
Doména SH2 se skládá z přibližně 100 aminokyselin připojených k katalytickým doménám. Nejviditelnějším příkladem jsou tyrosinkinázové enzymy, které jsou odpovědné za katalyzování přenosu fosfátové skupiny z ATP na aminokyselinové zbytky tyrosinu..
Dále byly domény SH2 hlášeny v nekatalytických doménách, jako jsou crk, grb2 / sem5 a nck..
SH2 domény jsou přítomny ve vyšších eukaryotech a bylo navrženo, že se také objevují v kvasinkách. Pokud jde o bakterie, v Escherichia coli byl nahlášen modul, který připomíná domény SH2.
Protein src je první objevenou tyrosinkinázou, která se při mutaci pravděpodobně podílí na regulaci aktivity kinázy a také na podpoře interakcí těchto proteinů s dalšími složkami v buňce.
Po objevení domén v proteinu scr byla doména SH2 identifikována u významného počtu vysoce rozmanitých proteinů, včetně proteinových tyrosin kináz a transkripčních faktorů..
Struktura
Struktura domény SH2 byla odhalena použitím technik, jako je rentgenová difrakce, krystalografie a NMR (nukleární magnetická rezonance), které nacházejí společné vzory v sekundární struktuře studovaných domén SH2..
SH2 doména má pět vysoce konzervovaných motivů. Obecná doména se skládá z jádrových β listů s malými sousedními částmi antiparalelních β listů, ohraničených dvěma α šroubovicemi..
Aminokyselinové zbytky na jedné straně listu a v aA N-koncové oblasti se podílejí na koordinaci vazby peptidů. Zbytek charakteristik proteinů je však mezi studovanými doménami velmi variabilní..
V terminální uhlíkové části se isoleucinový zbytek nachází ve třetí poloze a tvoří hydrofobní kapsu na povrchu domény SH2..
Důležitou charakteristikou je existence dvou regionů, z nichž každý má určitou funkci. Oblast mezi první a šroubovicí a β vrstvou je rozpoznávacím místem fosfotyrosinu.
Podobně oblast mezi β vrstvou a α šroubovicí koncového uhlíku tvoří oblast odpovědnou za interakci s koncovými uhlíkovými zbytky fosfotyrosinu.
Funkce
Funkcí domény SH2 je rozpoznání stavu fosforylace na aminokyselinových zbytcích tyrosinu. Tento jev je zásadní při signální transdukci, kdy je molekula umístěná mimo buňku rozpoznána receptorem na membráně a zpracována uvnitř buňky..
Transdukce signálu je nesmírně důležitá regulační událost, při které buňka reaguje na změny ve svém extracelulárním prostředí. K tomuto procesu dochází díky přenosu vnějších signálů obsažených v určitých molekulárních poslechech přes jeho membránu..
Fosforylace tyrosinu vede k postupné aktivaci interakcí protein-protein, což vede ke změně genové exprese nebo změně buněčné odpovědi.
Proteiny obsahující domény SH2 se účastní regulačních cest souvisejících s nezbytnými buněčnými procesy, jako je cytoskeletální přesmyk, homeostáza, imunitní reakce a vývoj..
Vývoj
Přítomnost domény SH2 byla hlášena u primitivního jednobuněčného organismu Monosiga brevicollis. Předpokládá se, že se tato doména vyvinula jako invariantní signalizační jednotka s výskytem fosforylace tyrosinu..
Spekuluje se, že rodové uspořádání domény sloužilo k nasměrování kináz na jejich substráty. S nárůstem složitosti v organismech tedy domény SH2 získaly v průběhu evoluce nové funkce, jako je alosterická regulace katalytické domény kináz..
Klinické důsledky
X-vázaný lymfoproliferativní
Bylo identifikováno, že některé mutované domény SH2 způsobují onemocnění. Mutace v doméně SH2 v SAP způsobují X-vázané lymfoproliferativní onemocnění, které způsobuje vysoké zvýšení citlivosti na určité viry a tím nekontrolovanou proliferaci B buněk..
K proliferaci dochází, protože mutace domén SH2 způsobuje poruchy signálních drah mezi B a T buňkami, což vede k virovým infekcím a nekontrolovanému růstu B buněk. Toto onemocnění má vysokou úmrtnost.
X-vázaná agamaglobulinémie
Podobně jsou mutace ve vzpěře v doméně SH2 Brutonovy proteinkinázy zodpovědné za stav zvaný agamaglobulinemie..
Tento stav je vázán na X, charakterizovaný nedostatkem B buněk a výrazným poklesem hladin imunoglobulinu..
Noonanův syndrom
A konečně, mutace v N-koncové oblasti SH2 domény v proteinové tyrosin fosfatáze 2 jsou příčinou Noonanova syndromu..
Tato patologie je charakterizována hlavně srdečními chorobami, nízkým vzrůstem v důsledku pomalejšího růstu a abnormalitami obličeje a kostí. Tento stav může navíc představovat mentální a psychomotorickou retardaci ve čtvrtině studovaných případů..
Reference
- Berg, J. M., Stryer, L. a Tymoczko, J. L. (2007). Biochemie. Obráceně.
- Filippakopoulos, P., Müller, S., & Knapp, S. (2009). Domény SH2: modulátory aktivity nereceptorové tyrosinkinázy. Aktuální názor na strukturní biologii, 19(6), 643-649.
- Kurochkina, N. (vyd.). (2015). Sh Domains: Struktura, mechanismy a aplikace. Springer.
- Sawyer, T. K. (1998). Homologie Src - 2 domény: Struktura, mechanismy a objevování léků. Věda o peptidech, 47(3), 243-261.
- Schlessinger, J. (1994). Signální proteiny SH2 / SH3. Aktuální názor na genetiku a vývoj, 4(1), 25-30.


Zatím žádné komentáře