
Symptomy, příčiny, léčba mitochondriálních nemocí
The mitochondriální nemoci jsou vysoce heterogenní skupinou poruch, které vznikají v důsledku dysfunkce mitochondriálního respiračního řetězce. Jsou výsledkem spontánních nebo zděděných mutací, ať už v mitochondriální DNA nebo v nukleární DNA.
Tyto mutace vedou ke změněným funkcím proteinů nebo molekul RNA (kyselina ribonukleová), které normálně sídlí v mitochondriích. Mitochondriální respirační řetězec je tvořen pěti komplexy (I, II, III, IV a V) a dvěma molekulami, které fungují jako článek; koenzym Q a cytochrom c.
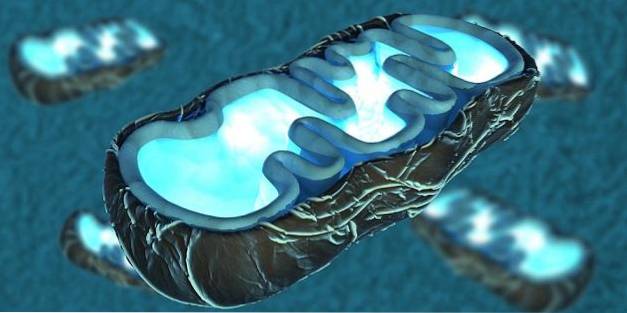
Široká škála změn v podmínkách mitochondriálního oxidačního metabolismu zahrnuje heterogenní podmínky pod názvem mitochondriální nemoci. Abychom však lépe pochopili, z čeho se tyto poruchy skládají, musíme vědět, co jsou mitochondrie.
Rejstřík článků
- 1 Vztah mitochondriálně-mitochondriální choroby
- 2 Prevalence
- 3 Nejčastější mitochondriální onemocnění
- 4 Příznaky
- 5 příčin
- 6 Diagnóza mitochondriálních onemocnění
- 6.1 Počáteční metabolická studie
- 6.2 Genetická studie
- 6.3 Klinické studie
- 7 Léčba
- 7.1 Obecná opatření
- 7.2 Farmakologická opatření
- 8 Předpověď
- 9 Odkazy
Vztah mitochondriálně-mitochondriální choroby
Mitochondrie jsou cytoplazmatické organely zapojené do oxidační fosforylace. Jsou odpovědné za vytváření více než 90% energie potřebné pro tělo k udržení života a podpoře růstu.
Když mitochondrie selžou, generuje se v buňce stále méně energie, což způsobuje poškození buněk a dokonce i smrt buňky. Pokud se tento proces opakuje v celém těle, začnou selhávat celé systémy a život člověka, který ho trpí, může být vážně ohrožen..
Toto onemocnění postihuje hlavně děti, ale nástup onemocnění u dospělých je stále častější..
Je známo, že každá lidská buňka obsahuje tisíce kopií mitochondriální DNA. Při narození jsou obvykle všechny identické, což se nazývá homoplazmie. Naproti tomu jedinci s mitochondriálními poruchami mohou skrývat směs mutované a divoké mitochondriální DNA v každé buňce, která se nazývá heteroplazmie..
Zatímco některé mitochondriální poruchy postihují pouze jeden orgán, mnoho dalších mitochondriálních poruch zahrnuje více orgánových systémů a často mají neurologické a myopatické rysy. Mitochondriální poruchy se mohou objevit v jakémkoli věku.
Prevalence
Z hlediska prevalence jsou mitochondriální poruchy častější, než se dříve myslelo, až do té míry, že jsou jednou z nejčastějších dědičných metabolických poruch..
Na základě dostupných údajů je konzervativní odhad prevalence mitochondriálních onemocnění 11,5 na 100 000 obyvatel..
Nejběžnější mitochondriální onemocnění
Protože mitochondrie plní tolik různých funkcí v různých tkáních, existují doslova stovky mitochondriálních onemocnění. Každá porucha vytváří spektrum příznaků a známek, které mohou být pro pacienty a lékaře v raných fázích diagnostiky matoucí..
Vzhledem ke složité interakci mezi stovkami genů a buněk, které musí spolupracovat, aby náš metabolický aparát fungoval hladce, je charakteristickým znakem mitochondriálních onemocnění, že identické mutace mitochondriální DNA mohou produkovat neidentická onemocnění..
Mezi nejčastější syndromy a příznaky mitochondriální patologie tedy patří:
- Alpers-Huttenlocherův syndrom: Je charakterizována hypotonií, záchvaty a selháním jater.
- Syndrom ataxické neuropatie: Charakterizovaná epilepsií, dyzartrií a / nebo myopatií.
- Chronická progresivní externí oftalmoplegie (CPEO): Vyskytuje se externí oftalmoplegie, bilaterální ptóza a mírná proximální myopatie.
- Kearns-Sayreův syndrom (KSS): Progresivní externí oftalmoplegie začínající před 20. rokem, pigmentová retinopatie, ataxie, myopatie, dysfagie, diabetes mellitus, hypoparatyreóza, demence.
- Pearsonův syndrom: Sideroblastická anémie v dětství, pancytopenie, exokrinní pankreatická nedostatečnost, renální tubulární defekty.
- Dětská myopatie a laktátová acidóza: Hypotonie v prvním roce života, potíže s krmením a dýcháním. Fatální forma může být spojena s kardiomyopatií a / nebo Toni-Fanconi-Debreovým syndromem.
- Leighův syndrom: Známky encefalopatie mozkových kmenů a mozkových kmenů s nástupem infantilního původu, neurologické onemocnění u matky v anamnéze nebo Leighův syndrom.
- Syndrom deplece mitochondriální DNA (MDS): Nástup v dětství a charakterizovaný svalovou slabostí a / nebo selháním jater.
- Neurogenní slabost s ataxií a rhinitis pigmentosa (NARP): Periferní neuropatie s nástupem dospělého nebo pozdního dětství, ataxie, pigmentová retinopatie.
- Mitochondriální encefalomyopatie s laktátovou acidózou a cévními mozkovými příhodami (syndrom MELAS): Epizody simulující mrtvice před 40 lety, záchvaty a / nebo demenci a laktátovou acidózu.
- Myoklonická epileptická myopatie se senzorickou ataxií (MEMSA): Charakterizovaná myopatií, záchvaty a cerebelární ataxií.
- Myoklonická epilepsie s otrhanými červenými vlákny (Merrf): Myoklonus, záchvaty, cerebelární ataxie, myopatie, demence, atrofie optiky a spasticita.
- Mitrochondriální neurogastrointestinální encefalopatie (MNGIE): Nástup před 20. rokem života, progresivní vnější oftalmoplegie, ptóza, slabost končetin a zažívací potíže.
- Leber (Lhon) dědičná optická neuropatie: Bilaterální subakutní bezbolestné zhoršení zraku. Průměrný věk nástupu po 24 letech. Vyšší prevalence u žen než u mužů v poměru 4: 1. Vyznačuje se dystonií a syndromy preexcitace srdce.
Příznaky
Příznaky mitochondriálních onemocnění jsou velmi rozmanité a závisí mimo jiné na tom, kde se poškození nachází.
Některé mitochondriální poruchy postihují pouze jeden orgán, ale většina zahrnuje více systémů. Mezi nejčastější obecné příznaky mitochondriální choroby patří:
- Porucha růstu
- Psychomotorická retardace
- Ptóza očních víček
- Externí oftalmoplegie
- Poruchy oka
- Proximální myopatie
- Nesnášenlivost cvičení
- Centrální nebo periferní hypotonie
- Kardiomyopatie
- Senzorická hluchota,
- Optická atrofie
- Pigmentární retinopatie
- Mellitus diabetes
- Gastrointestinální poruchy
- Malabsorpční syndrom
- Endokrinní poruchy
- Hematologické poruchy
Příznaky související s centrálním nervovým systémem často kolísají a zahrnují:
- Encefalopatie
- Záchvaty
- Demence
- Migréna
- Epizody podobné mrtvici
- Ataxie
- Spasticita
Příčiny
Mitochondriální poruchy mohou být způsobeny defekty v nukleární DNA nebo mitochondriální DNA. Nukleární genetické vady mohou být zděděny autozomálně dominantním nebo autozomálně recesivním způsobem. Poruchy mitochondriální DNA se přenášejí prostřednictvím mateřské dědičnosti.
Mitochondriální delece DNA se obvykle vyskytují de novo, a proto způsobují onemocnění pouze u jednoho člena rodiny.
Otec postiženého jedince není ohrožen patogenní variantou mitochondriální DNA, ale matka postiženého jedince má obecně patogenní variantu mitochondriální a může nebo nemusí mít příznaky.
Diagnóza mitochondriálních onemocnění
S více než 1000 jadernými geny kódujícími mitochondriální proteiny může být molekulární diagnostika náročná.
Z tohoto důvodu je diagnóza mitochondriálních onemocnění založena na klinickém podezření, naznačeném údaji z anamnézy, fyzickým vyšetřením a výsledky obecných doplňkových vyšetření. Později se provádějí specifické testy na mitochondriální dysfunkci.
Vyšetření obvykle nezbytná v procesu studia nemoci zahrnují:
- Vyšetření fundusu, které umožňuje pohled do oční bulvy k diagnostice nemoci.
- Elektroencefalografie (EEG).
- Sluchové evokované potenciály, somatosenzorické potenciály a vizuální evokované potenciály.
- Elektromyogram (EMG).
- Elektroneurografická studie, stejně jako neuroimagingové testy, jako je CT mozku, a zejména mozkové magnetické rezonance (MRI), mohou být velmi užitečné spektroskopické MRI.
Například bylo zjištěno, že bilaterální hyperintenzivní signály v bazálních jádrech jsou typické pro Leighův syndrom..
U syndromu MELAS jsou přítomny léze podobné infarktu v zadních mozkových hemisférách, zatímco u Kearn-Sayreho syndromu jsou vizualizovány difúzně abnormální signály z mozkové bílé hmoty..
Kalcifikace bazálních ganglií jsou běžné u syndromů MELAS a Kearn-Sayre.
Počáteční metabolická studie
Obvykle se také provádí počáteční metabolická studie k pozdějšímu provedení diagnostických konfirmačních testů, jako jsou morfologické a histoenzymatické studie, elektronová mikroskopie, biochemická studie a genetická studie, jejichž cílem je demonstrovat změny v mitochondriální DNA a v budoucnu také v jaderné DNA..
Genetická studie
Pokud jde o genetickou studii, bylo zjištěno, že u některých jedinců je klinický obraz charakteristický pro specifickou mitochondriální poruchu a diagnózu lze potvrdit identifikací patogenní varianty mitochondriální DNA
Místo toho u většiny jedinců to tak není a je zapotřebí strukturovanější přístup, který studuje vše od rodinné anamnézy, krevních testů a / nebo koncentrace laktátu v mozkomíšním moku až po studie neuroimagingu, hodnocení srdce a molekulárně genetické testování.
Klinické testy
A konečně, u mnoha jedinců, u kterých molekulárně genetické testování neposkytuje mnoho informací nebo nemůže potvrdit diagnózu, lze provést celou řadu různých klinických studií, například svalovou biopsii funkce dýchacího řetězce..
Léčba
Neexistuje žádná specifická léčebná léčba mitochondriálních onemocnění. Léčba mitochondriální choroby je do značné míry podpůrná, paliativní a může zahrnovat včasnou diagnostiku a léčbu diabetes mellitus, srdečního rytmu, korekci ptózy, výměnu nitroočních čoček za kataraktu a kochleární implantaci pro senzorineurální ztrátu sluchu.
Obecná opatření
Obecná opatření zahrnují:
- Zamezení tepelnému stresu (horečka nebo nízké teploty)
- Vyvarujte se intenzivního fyzického cvičení. Aerobní cvičení však může zlepšit kapacitu svalové energie.
- Vyhýbání se lékům, které potlačují mitochondriální dýchací řetězec (fenytoin, barbituráty), a také inhibitorům syntézy mitochondriálních proteinů (chloramfenikol, tetracykliny) nebo metabolismu karnitinu (kyselina valproová).
Farmakologická opatření
Mezi farmakologická opatření najdou se navzájem:
- Koenzym Q10 (ubichinon): Silný antioxidant, který přenáší elektrony z komplexů I a II na cytochrom C.
- Idebenon: Podobné jako CoQ10. Překračuje hematoencefalickou bariéru a má antioxidační sílu.
- Vitamíny: Jako riboflavin a sukcinát sodný. Léčba vitaminem K a C zlepšuje oxidační fosforylaci. U některých změn mitochondriálního respiračního řetězce byla hlášena izolovaná pozorování klinického zlepšení podáváním thiaminu, niacinamidu a riboflavinu, protože působí jako kofaktory v mitochondriálním transportním řetězci elektronů. Kyselina lipoová může být také účinná zvýšením buněčné syntézy ATP a usnadněním využití a oxidace glukózy..
- Kortikosteroidy a inhibitory monoaminooxidázy: Mohou být účinné, protože inhibují peroxidaci a chrání membrány.
- L-karnitin: Zlepšuje svalovou slabost, kardiomyopatii a příležitostně encefalopatii.
- L-tryptofan: Může příležitostně zlepšit myoklonus a ventilaci u některých pacientů s MERRF.
- Dichloracetát sodný: Inhibuje jaterní syntézu glukózy a stimuluje její použití v periferních tkáních, čímž zlepšuje oxidační metabolismus mozku. Mělo by se používat ve spojení s thiaminem.
Předpověď
Mitochondriální nemoci obvykle představují degenerativní procesy, i když v určitých případech mohou mít chronický stacionární průběh ve formě opakujících se neurologických projevů a dokonce vykazují spontánní zlepšení až do uzdravení, jak je tomu u benigního nedostatku COX..
Prognóza je obvykle lepší u čistých myopatických forem než u encefalopatických. Nemoc u dětí je obvykle agresivnější než u lidí, u nichž se projevuje jako dospělí.
Léčba obecně nedosahuje více než zpomalení přirozeného procesu, s některými výjimkami, mezi nimiž jsou primární procesy nedostatku CoQ10 nebo karnitinu.
Reference
- Chinnery, P. F. (2014). Přehled mitochondriálních poruch. Genové recenze,
- Arpa, J., Cruz-Martinez, A., Campos, Y., Gutierrez-Molina, M. a kol. (2003). Prevalence a progrese mitochondriálních onemocnění: studie 50 pacientů. Muscle Nerve, 28, 690-695.
- Eirís, J., Gómez, C., Blanco, M. O. & Castro, M. (2008). Mitochondriální nemoci. Terapeutické diagnostické protokoly AEP: Dětská neurologie, 15, 105-112.



Zatím žádné komentáře