
Paulingova stupnice elektronegativity a rozdílu energie

The Paulingova stupnice je libovolná stupnice používaná v chemii k vyjádření elektronegativita prvků. To je definováno jako tendence určitého atomu přitahovat elektrony v kombinaci s jiným atomem.
V tomto smyslu mají prvky s vysokou elektronegativitou tendenci snadno získávat elektrony. Jedná se o nekovy, zatímco pro jejich část, méně elektronegativní prvky, jako jsou kovy, je snazší vzdát se elektronů.
Proto, když člověk zná elektronegativitu prvku, má představu o typu vazby, kterou je schopen vytvořit v kombinaci s jiným. Uvidíme to na numerickém příkladu později..
S touto informací lze předvídat mnoho vlastností, které bude mít sloučenina, což je něco velmi užitečného v experimentální chemii a pro vědu o materiálech, kde se neustále vytvářejí nové sloučeniny..
Je však vhodné objasnit, že i přes to, jak je to důležité, neexistuje jediný způsob, jak určit elektronegativitu; Paulingova stupnice je pouze jedním z různých způsobů navrhovaných k jejímu nalezení, ačkoli je jedním z nejpoužívanějších.
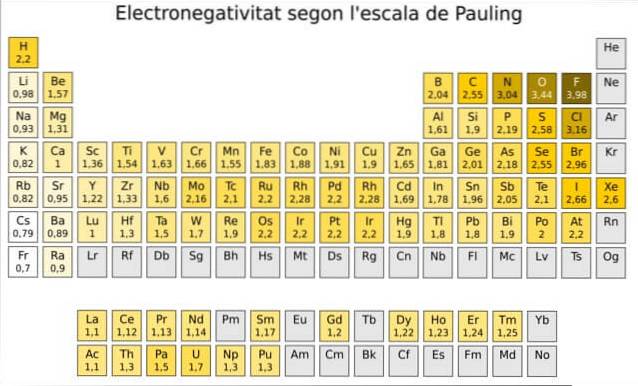
Ve skutečnosti je Paulingova libovolná stupnice, ve které je každému prvku v periodické tabulce přiřazena číselná hodnota, což odráží jeho elektronegativitu. Vidíme to na obrázku 1, kde máme elektronegativitu každého prvku, kterou přidělil dvojnásobný laureát Nobelovy ceny Linus Pauling (1901-1994) kolem roku 1939.
Rejstřík článků
- 1 Elektronegativita prvků
- 1.1 Elektronegativita v periodické tabulce
- 2 Rozdíl vazebné energie
- 2.1 Rovnice pro elektronegativitu
- 3 Příklad
- 3.1 Řešení
- 4 Odkazy
Elektronegativita prvků
Pauling společně s Donem M. Yostem zjistili hodnoty elektronegativity empiricky prostřednictvím experimentálních dat získaných měřením energií vazby..
Pauling přidělil prvku fluor - nahoře a napravo od tabulky na obrázku 1 - nejvyšší elektronegativitu s číslem 4,0. Když tedy fluor vytváří vazby, vykazuje nejvyšší tendenci přitahovat elektrony všech prvků..
Druhý je kyslík s 3,5 a třetí je dusík s 3,0. Oba jsou umístěny nahoře a napravo od stolu.
Na druhé straně, v opačném extrému, je nejméně elektronegativním prvkem cesium, jehož symbol je Cs, umístěný nalevo od tabulky, kterému Pauling přidělil číslo 0,7.
Elektronegativita v periodické tabulce
Obecně a jak je vidět na obrázku 1, elektronegativita - a ionizační energie - se v periodické tabulce zvyšuje zleva doprava. Obecný trend také naznačuje pokles při přechodu shora dolů.
Proto budeme mít v pravém horním rohu tabulky nejvíce elektronegativní prvky: fluor, kyslík, chlor, dusík. Nejméně elektronegativní - nebo nejelektropozitivnější, pokud chcete - najdete nalevo: lithium, sodík, draslík a další prvky skupiny 1 - sloupec zcela vlevo, což odpovídá alkalickým kovům a kovům alkalických zemin.-.
V každém sloupci klesá elektronegativita s rostoucím atomovým číslem prvku, s výjimkou přechodných kovů ve středu, které tento trend nenásledují..
Je důležité si uvědomit, že elektronegativita je relativní, není neměnnou vlastností každého prvku a měří se pouze s ohledem na vlastnosti ostatních prvků. Závisí to hodně na oxidačním stavu, takže stejný prvek může vykazovat různou elektronegativitu, v závislosti na typu sloučeniny, kterou tvoří..
Rozdíl vazebné energie

V chemii je vazba způsob, jakým se atomy, stejné nebo různé, spojují dohromady a tvoří molekuly. Mezi atomy se objevují síly, které je drží pohromadě stabilním způsobem.
Existuje několik typů odkazů, ale zde se uvažuje o dvou:
-Kovalentní, ve kterém atomy podobných elektronegativit sdílejí pár elektronů.
-Iontové, časté mezi atomy s různými elektronegativitami, ve kterých převládá elektrostatická přitažlivost.
Předpokládejme, že dva prvky A a B mohou navzájem tvořit molekuly, označené AA a BB. A že jsou také schopni spojit se a vytvořit sloučeninu AB, a to prostřednictvím nějakého typu vazby.
Díky účasti mezimolekulárních sil je ve vazbě energie. Například energie ve vazbě AA je EAA, ve vazbě BB je to EBB a nakonec ve sloučenině AB je to EAB.
Pokud by molekula AB byla vytvořena kovalentní vazbou, teoreticky je vazebná energie průměrem energií EAA a E.BB:
AAB = ½ (napřAA + ABB)
Pauling vypočítal EAB pro různé sloučeniny to experimentálně změřil a určil rozdíl mezi oběma hodnotami, které nazval Δ:
Δ = | (EAB) změřeno - (E.AB) teoretický | = | (E.AB) měřeno - ½ (E.AA + ABB) |
Pauling uvažoval takto: je-li Δ velmi blízké 0, znamená to, že elektronegativity obou prvků jsou podobné a vazba, která je spojuje, je kovalentní. Pokud ale Δ není malé, pak vazba mezi A a B není čistě kovalentní.
Čím větší je absolutní hodnota Δ, tím větší je rozdíl mezi elektronegativitou prvků A a B, a proto vazba, která je spojuje, bude iontového typu. Čtenář později najde příklad, ve kterém je možné pomocí výpočtu Δ určit typ vazby sloučeniny.
Rovnice pro elektronegativitu
Za předpokladu, že rozdíl v energiích je signálem, který odlišuje povahu vazby, Pauling provedl mnoho experimentů, které ho vedly k vytvoření empirického vyjádření relativních elektronegativit dvou prvků A a B, které tvoří molekulu..
Označením této elektronegativity jako χ (řecké písmeno „chi“) Pauling definoval Δ následovně:
Fdva· Δ = [χ (A) - χ (B)]dva
χ (A) - χ (B) = f√Δ = 0,102√Δ
Všimněte si, že Δ je kladná veličina. Faktor f = 0,102, který se objeví vynásobením druhé odmocniny Δ, je převodní faktor mezi kJ (kilojoulů) a eV (elektronvolt), obě jednotky energie.
Pokud se místo toho použijí kilokalorie a elektronvolty, je rozdíl v elektronegativitách vyjádřen podobným vzorcem, ale s f = 0,208:
χ (A) - χ (B) = 0,208√Δ
Pauling začal přidělením vodíku na hodnotu 2,1, což je předchozí hodnota, kterou získal chemik Robert Mulliken. Tento prvek si vybral jako výchozí bod, protože vytváří kovalentní vazby s mnoha dalšími..
Pomocí výše uvedené rovnice pokračoval v přiřazování relativních hodnot zbytku prvků. Uvědomil si tedy, že elektronegativita se zvyšuje při pohybu zleva doprava a shora dolů v periodické tabulce, jak je popsáno v předchozí části..
Příklad
Níže je uveden seznam prvků: N, J, Y a M a jejich příslušné elektronegativity Χ podle Paulingovy stupnice:
-N: Χ = 4,0
-J: Χ = 1.5
-Y: Χ = 0,9
-M: Χ = 1.6
Mezi následujícími sloučeninami vytvořenými:
YJ, YN, MN a JM
Uveďte ten s nejvyšším iontovým charakterem a ten, jehož povaha je kovalentní. Důvod pro vaši odpověď.
Řešení
Podle kritérií stanovených Paulingem bude sloučenina s největším iontovým charakterem sloučenina s největším rozdílem mezi elektronegativitami, a tedy s větší hodnotou Δ. Sloučenina s nejmenším energetickým rozdílem je složka s kovalentní vazbou.
Poté vypočítáme, kolik Δ má každá sloučenina, takto:
Kompozitní YJ
Δ = [χ (Y) - χ (J)]dva = (0,9 - 1,5)dva = 0,36
Složený YN
Δ = [χ (Y) - χ (N)]dva = (0,9 - 4,0)dva = 9,61
Kompozitní MN
Δ = [χ (M) - χ (N)]dva = (1,6 - 4,0)dva = 5,76
Kompozitní JM
Δ = [χ (J) - χ (M)]dva = (1,5 - 1,6)dva = 0,01
Z předchozích výsledků vyplývá, že iontovou sloučeninou je YN, jehož Δ = 9,61, zatímco kovalentní sloučeninou je JM, s Δ = 0,01.
Reference
- Chemistry Libretexts. Pauling Electronegativity. Obnoveno z: chem.libretexts.org.
- Zlatá kniha IUPAC. Elektronegativita. Obnoveno z: goldbook.iupac.org.
- Salas-Banuet, G. Nepochopená elektronegativita. Obnoveno z: scielo.org.
- Vědecké texty. Elektronegativita. Obnoveno z: paperscientificos.com.
- Whitten, K. 2010. Chemie. 9. Vyd. Brooks / Cole. Cengage Learning.
- Wikipedia. Kovalentní vazba. Obnoveno z: es.wikipedia.org.
- Wikipedia. Iontová vazba. Obnoveno z: es.wikipedia.org.


Zatím žádné komentáře