
Kvartérní struktura charakteristických proteinů
The kvartérní struktura bílkovin definuje prostorové vztahy mezi každou z jeho polypeptidových podjednotek spojených nekovalentními silami. V polymerních proteinech se každý z polypeptidových řetězců, které ho tvoří, nazývá podjednotky nebo protomery.
Proteiny mohou být tvořeny jedním (monomerním), dvěma (dimerními), několika (oligomerními) nebo mnoha protomery (polymerními). Tyto protomery mohou mít podobnou nebo velmi odlišnou molekulární strukturu. V prvním případě se říká, že jde o homotypické proteiny, a ve druhém případě o heterotypické.
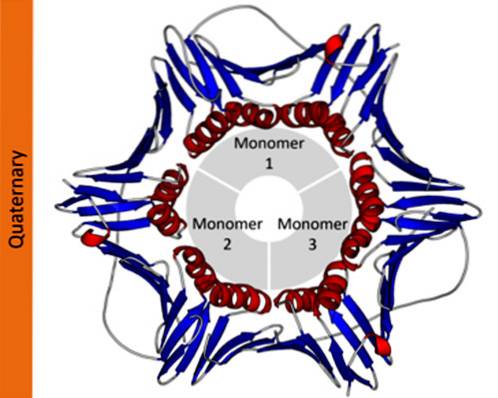
Ve vědecké notaci biochemici používají dolní indexová řecká písmena k popisu protomerního složení proteinů. Například tetramerní homotypický protein je označen jako a4, zatímco tetramerní protein složený ze dvou různých dimerů je označen jako αdvaβdva.
Rejstřík článků
- 1 Proteinová struktura
- 1.1 Primární struktura
- 1.2 Sekundární struktura
- 1.3 Terciární struktura
- 1.4 Kvartérní struktura
- 2 Stabilita kvartérní struktury
- 2.1 Hydrofobní interakce
- 2.2 Van der Waalsovy interakce
- 2.3 Interakce zatížení a zatížení
- 2.4 Vodíkové vazby
- 2.5 Interakce dipólů
- 3 Interakce mezi protomery
- 3.1 Homotypické interakce
- 3.2 Heterotypové interakce
- 4 Odkazy
Struktura bílkovin
Proteiny jsou složité molekuly, které nabývají různých trojrozměrných konfigurací. Tyto konfigurace jsou pro každý protein jedinečné a umožňují jim vykonávat velmi specifické funkce. Úrovně strukturní organizace proteinů jsou následující.
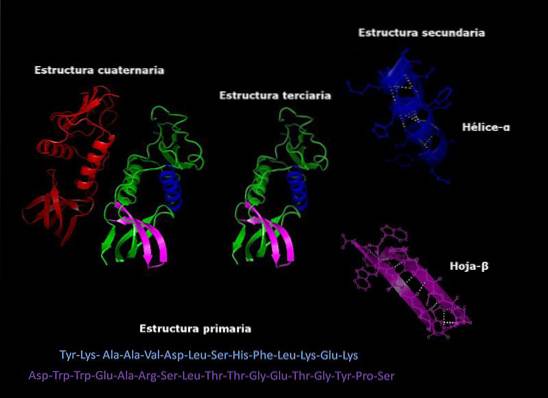
Primární struktura
Týká se sekvence, ve které jsou různé aminokyseliny uspořádány v polypeptidovém řetězci. Tato sekvence je dána sekvencí DNA, která kóduje uvedený protein.
Sekundární struktura
Většina proteinů není plně prodlouženým dlouhým řetězcem aminokyselin, ale spíše oblastmi, které jsou pravidelně skládány do šroubovic nebo listů. Toto skládání dostává název sekundární struktury.
Terciární struktura
Přeložené oblasti sekundární struktury mohou být zase složeny a sestaveny do kompaktnějších struktur. Tento poslední záhyb dává proteinu jeho trojrozměrný tvar..
Kvartérní struktura
V proteinech, které jsou tvořeny více než jednou podjednotkou, jsou kvartérní struktury prostorové vztahy, které existují mezi každou podjednotkou, které jsou spojeny nekovalentními vazbami..
Stabilita kvartérní struktury
Trojrozměrná struktura proteinů je stabilizována slabými nebo nekovalentními interakcemi. I když jsou tyto vazby nebo interakce mnohem slabší než normální kovalentní vazby, jsou četné a jejich kumulativní účinek je silný. Zde uvidíme některé z nejběžnějších interakcí.
Hydrofobní interakce
Některé aminokyseliny obsahují hydrofobní postranní řetězce. Když proteiny mají tyto aminokyseliny, skládání molekuly objednává tyto postranní řetězce směrem dovnitř proteinu a chrání je před vodou. Povaha různých postranních řetězců znamená, že různými způsoby přispívají k hydrofobnímu účinku..
Van der Waalsovy interakce
K těmto interakcím dochází, když se molekuly nebo atomy, které nejsou vázány kovalentními vazbami, dostanou příliš blízko k sobě, a proto se jejich nejvzdálenější elektronické orbitaly začnou překrývat..
V té chvíli se mezi těmito atomy vytvoří odpudivá síla, která roste velmi rychle, jak se blíží jejich centra. Jedná se o takzvané „van der Waalsovy síly“.
Interakce zatížení-zatížení
Jedná se o elektrostatickou interakci, která nastává mezi dvojicí nabitých částic. V proteinech dochází k tomuto typu interakce, a to jak kvůli čistému elektrickému náboji proteinu, tak kvůli individuálnímu náboji iontů v něm obsažených. Tento typ interakce se někdy nazývá solný most..
Vodíkové vazby
Vodíková vazba je vytvořena mezi atomem vodíku kovalentně navázaným na donorovou skupinu vodíkové vazby a dvojicí volných elektronů patřících do skupiny akceptoru vazby.
Tento typ vazby je velmi důležitý, protože vlastnosti mnoha molekul, včetně vlastností vody a biologických molekul, jsou do značné míry způsobeny vodíkovými vazbami. Sdílí vlastnosti kovalentních vazeb (elektrony jsou sdílené) a také nekovalentních interakcí (interakce náboj-náboj).
Dipólové interakce
V molekulách, včetně proteinů, které nepředstavují síťový náboj, může dojít k nerovnoměrnému uspořádání jejich vnitřních nábojů, přičemž jeden extrém je mírně zápornější než druhý. Toto je známé jako dipól.
Tento dipolární stav molekuly může být trvalý, ale může být také indukován. Dipóly mohou být přitahovány ionty nebo jinými dipóly. Pokud jsou dipóly trvalé, má interakce větší rozsah, než jaký nastává u indukovaných dipólů.
Kromě těchto nekovalentních interakcí některé oligomerní proteiny stabilizují svou kvartérní strukturu prostřednictvím typu kovalentní vazby, disulfidové vazby. Ty se vytvářejí mezi sulfhydrylovými skupinami cysteinů různých protomerů.
Disulfidové vazby také pomáhají stabilizovat sekundární strukturu proteinů, ale v tomto případě spojují cysteinylové zbytky ve stejném polypeptidu (intrapolypeptidové disulfidové vazby)..
Interakce mezi protomery
Jak je uvedeno výše, v proteinech, které jsou tvořeny několika podjednotkami nebo protomery, mohou být tyto podjednotky podobné (homotypické) nebo odlišné (heterotypické)..
Homotypické interakce
Podjednotky, které tvoří protein, jsou asymetrické polypeptidové řetězce. V homotypických interakcích se však tyto podjednotky mohou přidružit různými způsoby a dosáhnout tak různých typů symetrie..
Interagující skupiny každého protomeru jsou obvykle umístěny v různých pozicích, a proto se jim říká heterologní interakce. Heterologní interakce mezi různými podjednotkami se někdy vyskytují takovým způsobem, že každá podjednotka je zkroucena s ohledem na předchozí podjednotku a je schopna dosáhnout spirálovité struktury.
Při jiných příležitostech dochází k interakcím takovým způsobem, že definované skupiny podjednotek jsou uspořádány kolem jedné nebo více os symetrie, což je známé jako symetrie bodových skupin. Když existuje několik os symetrie, každá podjednotka se otáčí vzhledem ke svému sousedovi o 360 ° / n (kde n představuje počet os).
Mezi typy symetrie, které se získávají tímto způsobem, patří například spirálová, kubická a dvacetistěnná.
Když dvě podjednotky interagují přes binární osu, každá jednotka se otáčí o 180 ° vzhledem k druhé, kolem této osy. Tato symetrie je známá jako C symetriedva. V něm jsou interakční místa v každé podjednotce identická; v tomto případě nemluvíme o heterologní interakci, ale o isologické interakci.
Pokud je naopak asociace mezi dvěma složkami dimeru heterologní, získá se asymetrický dimer.
Heterotypové interakce
Interagující podjednotky v proteinu nejsou vždy stejné povahy. Existují proteiny, které se skládají z dvanácti nebo více různých podjednotek.
Interakce, které udržují stabilitu proteinu, jsou stejné jako u homotypických interakcí, ale obecně se získávají zcela asymetrické molekuly..
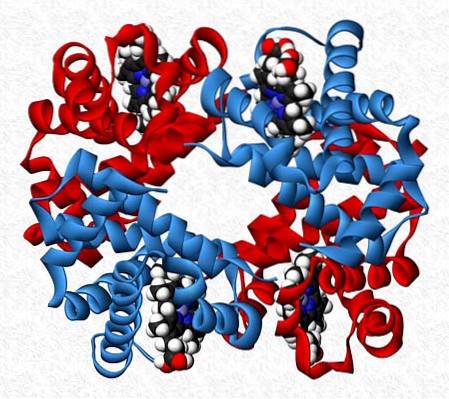
Hemoglobin je například tetramer, který má dva páry různých podjednotek (αdvaβdva).
Reference
- C.K. Mathews, K.E. van Holde & K.G. Ahern (2002). Biochemie. 3. vydání. Benjamin / Cummings Publishing Company, Inc..
- R.K. Murray, P. Mayes, D.C. Granner & V.W. Rodwell (1996). Harperova biochemie. Appleton & Lange
- J.M. Berg, J.L. Tymoczko a L. Stryer (2002). Biochemie. 5. vydání. W. H. Freeman and Company.
- J. Koolman a K.-H. Roehm (2005). Barevný atlas biochemie. 2. vydání. Thieme.
- A. Lehninger (1978). Biochemie. Ediciones Omega, S.A.
- L. Stryer (1995). Biochemie. W.H. Freeman and Company, New York.


Zatím žádné komentáře