
Struktura, funkce, zrání CD4 T lymfocytů
The CD4 T lymfocyty jsou typem T lymfocytů, který funguje hlavně jako „doplňková“ nebo „pomocná“ buňka během specifické nebo adaptivní imunitní odpovědi. Vyznačují se přítomností membránového receptoru známého jako „komplex receptorů T buněk“, zkráceně TCR (z angličtiny Přijímač T buněk). Existují však různé subpopulace T buněk, které jsou identifikovány přítomností dalších molekul membránových markerů..
Tyto molekuly jsou proteinové povahy a jsou známé jako součást „skupiny diferenciace“ nebo CD. Klastr diferenciace). T lymfocyty lze tedy rozdělit do dvou hlavních skupin: CD4 T buňky a CD8 T buňky..
Ty jsou také známé jako „cytotoxické T buňky“, protože při humorální imunitní odpovědi přímo zasahují do eliminace buněk napadených viry nebo intracelulárními mikroorganismy..
CD4 T lymfocyty jsou v literatuře populárně známé jako „pomocné T lymfocyty“, protože se účastní aktivace dalších lymfocytů imunitního systému: lymfocytů B. Jejich účast podporuje jak aktivaci, tak produkci a sekreci protilátek..
Rejstřík článků
- 1 Struktura
- 1.1 Typy CD4 T lymfocytů
- 2 funkce
- 2.1 Jako imunitní paměťové buňky
- 3 Zrání a aktivace
- 3.1 Jak probíhá aktivace?
- 3,2 programovaná buněčná smrt
- 4 Odkazy
Struktura
CD4 T buňky sdílejí strukturní rysy všech ostatních buněk lymfoidní linie. Mají prominentní jádro, které omezuje cytosol na úzký kruh mezi jeho plazmatickou membránou a jádrem..
Nemají příliš mnoho vnitřních organel, ale na elektronových mikrofotografiích se některé mitochondrie, malý Golgiho komplex, volné ribozomy a několik lysozomů podobaly.
Tyto buňky pocházejí z kostní dřeně od společného prekurzoru s jinými lymfoidními buňkami, jako jsou B buňky a buňky „natural killer“ (NK), stejně jako všechny ostatní hematopoetické buňky..
K jejich zrání a aktivaci však dochází mimo kostní dřeň, v orgánu známém jako brzlík, a mohou vykonávat své funkce v některých sekundárních lymfoidních orgánech, jako jsou mandle, slepé střevo a další..
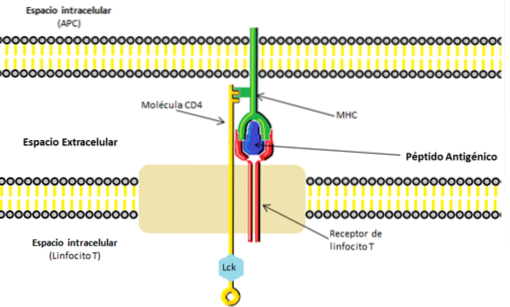
Od ostatních buněk lymfoidní linie se odlišují expresí specifických markerů, konkrétně „receptoru T-buněk“ (z angl. Přijímač T buněk). Tyto povrchové proteiny lze považovat za proteinové komplexy, které fungují hlavně při rozpoznávání antigenů, které jsou jim prezentovány..
Tyto proteiny jsou spojeny s dalším proteinovým komplexem známým jako CD3, který je nezbytný pro signalizaci, která probíhá během rozpoznávání antigenu..
Na druhé straně pomocné T lymfocyty exprimují na svém povrchu typ „markerové“ molekuly známé jako CD4, který stejně jako všechny molekuly diferenciačních skupin rozpoznává specifická místa receptorů „omezená“ molekulami MHC třídy II.
Typy CD4 T lymfocytů
V literatuře lze najít různé názvy různých typů T lymfocytů se značkami typu CD4, ale vyniká typ nomenklatury, který rozlišuje typ cytokinu, který jsou tyto buňky schopné produkovat..
Tímto způsobem bylo definováno několik tříd pomocných T lymfocytů, mezi nimiž vynikají TH1, TH2, TH9, TH17, TH22, THF a Tregs nebo regulační lymfocyty..
Lymfocyty TH1 vylučují interferon gama (IFN-γ), což je užitečný cytokin pro aktivaci dalších buněk imunitního systému známých jako makrofágy. Pomocné lymfocyty typu 2 (TH2) vylučují širokou škálu interleukinů, které podporují produkci protilátek.
Folikulární pomocné T lymfocyty nebo THF, které se nacházejí v lymfoidních folikulech, se účastní aktivace B buněk a také „pomáhají“ při produkci a sekreci protilátek vylučováním nadměrného množství cytokinů..
Další třída pomocných lymfocytů, regulační T lymfocyty nebo Tregs, reguluje velké množství buněčných funkcí prostřednictvím kontaktů buňka-buňka, exprese povrchových molekul a potenciace reakce na různé růstové faktory..
Pokud jde o vývoj těchto „podskupin“ CD4 T lymfocytů, různé studie ukázaly, že jsou odvozeny od stejného prekurzoru T buněk, to znamená, že nepocházejí ze samostatných linií, které jsou ohroženy před antigenní stimulací..
Naproti tomu diferenciace každého typu pomocných lymfocytů je ovlivněna mnoha aspekty mikroprostředí, kterým je prekurzorová buňka, o které se předpokládá, že je naivní, zralý CD4 T lymfocyt, stimulována cytokiny produkovanými makrofágy..
Funkce
CD4 T buňky fungují primárně jako pomocné buňky. Jedná se o buňky, které se aktivují a generují imunitní odpovědi proti infekcím, jakmile naleznou, rozpoznají a interagují s napadajícím antigenem..
Jejich schopnost rozpoznávat a vázat cizí antigeny je značně odlišná od schopnosti B buněk, protože ty jsou schopny rozpoznat rozpustné antigeny ve stavu „naivního stavu“ před jejich úplnou diferenciací..
Naproti tomu T lymfocyty (obecně) mohou rozpoznávat pouze peptidové antigeny připojené k jiným molekulám kódovaným geny rodiny proteinů známou jako „hlavní histokompatibilní komplex“ nebo MHC. Hlavní komplex histokompatibility) a toto se nazývá „omezení MHC“.
Existují alespoň tři třídy MHC proteinů a CD4 T buňky rozpoznávají antigeny prezentované v kontextu MHC třídy II..
Říká se jim pomocné buňky T nebo „pomocníci„Protože„ pomáhají “B buňkám, které se vyznačují produkcí protilátek závislých na T, to znamená, že potřebují přítomnost T lymfocytů.
Jeho základní odpovědnost spočívá v produkci rozpustných cytokinů, které se účastní různých imunologických procesů..
Jako imunitní paměťové buňky
Určitá sada diferencovaných zralých CD4 T buněk může žít delší dobu a poskytovat rychlejší odpověď, když organismus, ve kterém se nacházejí, čelí podruhé stejnému antigenu..
Tyto buňky, které se věnují „zapamatování“ si antigenů, které je aktivovaly a spustily jejich diferenciaci, se nazývají „paměťové T buňky“.
Zrání a aktivace
CD4 T buňky pocházejí z kostní dřeně a následně migrují do brzlíku, aby se diferencovaly a zraly. Progenitorové lymfoidní buňky T lymfocytů přítomných v brzlíku jsou známé jako „thymocyty“..
Thymocyty procházejí různými stadii zrání, ve kterých jsou postupně exprimovány membránové markery, které je charakterizují (předchozí odkaz byl na markery TCR a CD3).
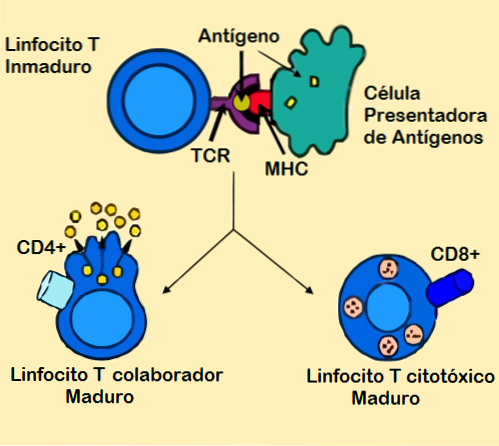
Během procesu zrání jsou vybírány pomocné T buňky, které rozpoznávají cizí antigeny, a ty, které rozpoznávají vlastní molekuly organismu, které je způsobují, jsou eliminovány. Jedná se o velmi důležitý ochranný mechanismus proti přítomnosti „samovolně reagujících“ buněk..
Jak probíhá aktivace?
Neaktivní T lymfocyty jsou v období mitotické stárnutí nebo, co je stejné, nedochází k aktivnímu dělení a jsou zastaveny ve fázi G0 buněčného cyklu.
Některé „doplňkové“ buňky známé jako buňky se účastní procesu aktivace. buňky prezentující antigen nebo APC (angličtiny Buňky prezentující antigen). Tyto buňky mají funkci „prezentovat“ antigeny navázané na proteiny MHC třídy II, které jsou selektivně rozpoznávány TCR na membráně CD4 T lymfocytů..
Během tohoto procesu, který probíhá v brzlíku, se lymfocyty diferencují na lymfoblasty a mění tvar a velikost. Lymfoblasty se mohou dělit a množit, čímž se znásobuje počet buněk v populaci.
Interakce mezi TCR receptorem (na povrchu CD4 T buňky) a antigenem vázaným na MHC třídy II (na povrchu APC buňky) tvoří komplex, který zajišťuje specifické rozpoznání.
Jakmile je prezentovaný antigen rozpoznán v kontextu MHC třídy II, jak CD4 lymfocyty, tak APC buňky začnou vylučovat cytokiny, které přispívají k aktivaci lymfocytů..
Když je lymfocyt aktivován, množí se a vytváří nové identické buňky, specifické pro daný antigen a které jsou ve „naivním“ nebo „naivním“ stavu.naivní", Který se nemění, dokud nesplní antigen, pro který byly" navrženy ".
Naprogramovaná buněčná smrt
Lidské tělo, stejně jako tělo mnoha savců, má schopnost produkovat stovky lymfocytárních buněk ve velmi krátkých časových obdobích..
Kromě toho, protože diferenciace T buňky zahrnuje náhodné přeskupení genů, které kódují rozpoznávací proteiny antigenů, které jsou jí prezentovány, existují stovky různých populací buněk schopných rozpoznávat různé „části“ stejného antigenu nebo různé antigeny.
Toto množství buněk implikuje určitá fyziologická nebezpečí, protože některé vzorce rozpoznávané membránovými receptory T buněk se mohly shodovat se vzory některých vlastních molekul..
Navíc ne všechny tyto buňky jsou určeny k okamžitému provádění svých funkcí, protože vyžadují interakci s definovaným antigenem..
Lymfocytové „homeostázy“ se tedy dosáhne v primárních lymfoidních orgánech, čímž se spustí naprogramované cesty buněčné smrti v těch buňkách, které nejsou nutné nebo které nediferencují a úplně nedospějí..
Reference
- Abbas, A., Murphy, K., & Sher, A. (1996). Funkční rozmanitost pomocných T lymfocytů. Příroda, 383, 787-793.
- Herec, J. K. (2014). Základní koncepty imunologie pro interdisciplinární aplikace. London: Academic Press.
- Bottomly K. (1988). Funkční dichotomie v CD4 + T lymfocytech. Imunologie dnes, 9(9), 268-274.
- Cavanagh, M. (n.d.). Aktivace T-buněk. Britská společnost pro imunologii.
- Reinherz, E., Haynes, B., Nadles, L. a Bernstein, I. (1986). Psaní leukocytů II. Lidské T lymfocyty (Sv. 1). Springer.
- Smith-Garvin, J. E., Koretzky, G. a & Jordan, M. S. (2009). Aktivace T buněk. Annu. Rev. Immunol., 27, 591-619.



Zatím žádné komentáře