
Struktura dusitanu sodného (NaNO2), vlastnosti, použití, rizika

The dusitan sodný je krystalická anorganická pevná látka vytvořená sodným iontem Na+ a nitritový iont NOdva-. Jeho chemický vzorec je NaNOdva. Je to bílá krystalická pevná látka, která má tendenci absorbovat vodu z prostředí, to znamená, že je hygroskopická.
V přítomnosti vzduchu pomalu oxiduje na dusičnan sodný NaNO3. Má oxidační vlastnosti (oxiduje jiné sloučeniny) a také redukční vlastnosti (oxiduje se jinými sloučeninami).

Je přítomen v lidském těle přirozeně a používá se jako konzervační prostředek pro uzená masa a uzené ryby, protože brání růstu škodlivých mikroorganismů.
Má důležité použití při nouzové léčbě otravy kyanidem, protože snižuje toxický a letální účinek této sloučeniny. Musí však být podáván s velkou opatrností a nefunguje ve všech případech.
Bylo zjištěno, že může zabránit očním infekcím způsobeným kontaminací kontaktních čoček mikroorganismy. Některé studie naznačují, že jeho konzumace s jídlem může způsobit rakovinu, ale odhaduje se, že tomu lze zabránit požitím vitaminu C v těchto potravinách.
Rejstřík článků
- 1 Struktura
- 2 Názvosloví
- 3 Vlastnosti
- 3.1 Fyzický stav
- 3,2 Molekulová hmotnost
- 3.3 Teplota tání
- 3.4 Bod varu
- 3.5 Hustota
- 3.6 Rozpustnost
- 3,7 pH
- 3.8 Další vlastnosti
- 4 Získání
- 4.1 Přítomnost v těle
- 5 použití
- 5.1 V potravinářském průmyslu
- 5.2 Jako nouzové ošetření při otravě kyanidem
- 5.3 Pro dilataci krevních cév
- 5.4 Proti některým parazitům
- 5.5 Aby nedošlo k poškození orgánů
- 5.6 Aby se zabránilo infekcím v důsledku používání kontaktních čoček
- 5.7 V různých použitích
- 6 Rizika nebo nepříjemnosti
- 7 Reference
Struktura
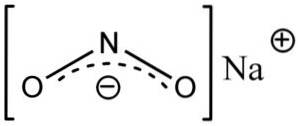
Dusitan sodný je tvořen sodným kationtem Na+ a dusitanový anion NOdva-.
V dusitanovém aniontu NOdva- dusík má valenci +3 a kyslík -2, z tohoto důvodu má anion jediný globální záporný náboj.
Dusitanový anion Čdva- má úhlovou strukturu, to znamená, že vazby dusíku (N) s atomy kyslíku (O) tvoří úhel.
Nomenklatura
- Dusitan sodný
- Dusitan sodný
- Sodná sůl kyseliny dusité.
Vlastnosti
Fyzický stav
Nažloutle bílá krystalická pevná látka. Ortorombické krystaly.
Molekulární váha
68,995 g / mol
Bod tání
271 ° C
Bod varu
Nevřídí se. Rozkládá se nad 320 ° C
Hustota
2,17 g / cm3 při 20 ° C
Rozpustnost
Rozpustný ve vodě: 84,8 g / 100 g vody při 25 ° C. Mírně rozpustný v ethanolu. Středně rozpustný v methanolu. Málo rozpustný v diethyletheru.
pH
Jeho vodné roztoky jsou alkalické a mají pH přibližně 9. Je to proto, že kyselina dusitá je slabá kyselina, která nemá tendenci disociovat, takže iont NOdva- zkuste vzít proton H+ vody za vzniku HNOdva, což vede k tvorbě OH iontů- které produkují zásaditost.
NEdva- + HdvaO → HNOdva + Ach-
Další vlastnosti
Dusitan sodný NaNOdva v přítomnosti vzduchu pomalu oxiduje na dusičnan sodný NaNO3. Je to hygroskopická pevná látka, protože absorbuje vodu z okolního prostředí.
Má oxidační vlastnosti (může oxidovat další sloučeniny) a také redukční vlastnosti (může být oxidován jinými sloučeninami).
Pokud přijde do styku s materiály, jako je dřevo, papír nebo textil, může to způsobit nebezpečné vznícení..
U kyselin dochází k jeho rozkladu za vzniku směsi hnědých toxických plynů oxidů dusíku (NOX).
Získávání
Lze jej získat zahřátím dusičnanu sodného NaNO3 s olověným Pb:
Starší bratr3 + Pb → NaNOdva + PbO
Přítomnost v těle
Dusitanový anion je přirozeně přítomen v krvi a tkáních, protože se tvoří v důsledku oxidace NO..
Aplikace
V potravinářském průmyslu
Používá se k marinování masa, protože působí jako prostředek pro zachování barvy a chuti a jako konzervační prostředek, protože reguluje růst mikroorganismů, přičemž se zejména vyhýbá vývoji Clostridium botulinum způsobující botulismus.
Dusitan sodný v mase reaguje s hemoglobinem v červených krvinkách nebo červených krvinkách v této potravině. Používá se také u uzených ryb.

Jako nouzové ošetření při otravě kyanidem
Dusitan sodný se používá k léčbě akutní otravy kyanidem. Je to protijed na tento závažný problém.
Jeho působení je způsobeno skutečností, že upřednostňuje tvorbu methemoglobinu (typ hemoglobinu) v krvi, který zachycuje kyanidové ionty a neuvolňuje je, a tak jim brání v uvolňování do buněk, čímž jsou méně toxické.
V případě otravy kyanidem se nitrit sodný aplikuje intravenózně, přičemž tvorba methemoglobinu trvá přibližně 12 minut. I přes toto zpoždění nabízí ochranu díky vazodilatačnímu účinku..
Pro dilataci krevních cév
Používá se k léčbě plicní arteriální hypertenze, protože působí dilatací krevních cév, čímž snižuje krevní tlak. Odhaduje se, že tento účinek je způsoben skutečností, že se transformuje na oxid dusnatý NO, který působí uvolněním měkkých svalů.
Příčiny jeho účinnosti jsou však stále předmětem studia..
Proti některým parazitům
Někteří vědci zjistili, že dusitan sodný inhibuje růst a množení střevních parazitů Blastocystis hominis i když je rezistentní na jiné léky.
NaNO bylo nalezenodva generuje smrt tohoto parazita apoptózou, což je druh sebevraždy parazitické buňky. Dusitan sodný způsobuje, že střevní buňky produkují NO, což se v tomto procesu jeví jako důležité.
Aby nedošlo k poškození orgánů
Podle některých studií je dusitan silným inhibitorem poškození srdce a jater při ischemických procesech (snížený průtok krve v části těla). Předpokládá se, že to je způsobeno skutečností, že se jedná o biologickou rezervu NO.
Byl vyvozen závěr, že jej lze použít k prevenci poškození orgánů po obnovení průtoku krve, který byl přerušen infarktem, vysoce rizikovou operací břicha nebo transplantací orgánu..
Aby se zabránilo infekcím při nošení kontaktních čoček
NaNO bylo nalezenodva zabraňuje tvorbě filmů patogenních mikroorganismů Zlatý stafylokok Y Pseudomonas aeruginosa o kontaktních čočkách.

V různých použitích
Dusitan sodný se používá k výrobě barviv, léků a různých organických sloučenin.
Slouží také jako inhibitor koroze u univerzálních tuků.
Rizika nebo nepříjemnosti
Jedním z problémů při používání dusitanu sodného při otravě kyanidem je to, že způsobuje závažné kardiovaskulární poruchy u dětí..
Nedoporučuje se pro oběti požáru, kde dochází k současné expozici jak kyanidu, tak oxidu uhelnatému (CO). CO snižuje schopnost krve přenášet kyslík, takže podávání NaNOdva by zhoršilo stav s nízkým obsahem kyslíku v krvi pacienta.
Inhalační dusitan sodný je dráždivý a toxický, může poškodit kardiovaskulární systém a centrální nervový systém. Kromě toho je škodlivý pro životní prostředí.
Dusitan sodný požitý s jídlem může být škodlivý. Dusitany po zasažení žaludku reagují s určitými sloučeninami za vzniku nitrosaminů, které mohou způsobit rakovinu.
Těmto reakcím se lze vyhnout v přítomnosti vitaminu C..
Podle určitých konzultovaných zdrojů je riziko konzumace dusitanů uzeným masem nebo rybami minimální, protože dusitany jsou přirozeně přítomny ve slinách.
Zdroje naznačují, že toto riziko je také minimální ve srovnání s velkými výhodami konzumace potravin bez škodlivých mikroorganismů.
Reference
- Bhattacharya, R. a Flora, S.J.S. (2015). Kyanidová toxicita a její léčba. In Handbook of Toxicology of Chemical Warfare Agents (Second Edition). Obnoveno ze sciencedirect.com.
- NÁS. Národní lékařská knihovna. (2019). Dusitan sodný. Obnoveno z: pubchem.ncbi.nlm.nih.gov.
- Kim, D.J. et al. (2017). Antibiofilmová účinnost oxidu dusnatého na měkké kontaktní čočky. BMC Ophthalmol 17, 206 (2017). Obnoveno z bmcophthalmol.biomedcentral.com.
- Ramis-Ramos, G. (2003). Antioxidanty. Syntetické antioxidanty. In Encyclopedia of Food Sciences and Nutrition (Second Edition). Obnoveno ze sciencedirect.
- Barozzi Seabra, A. a Durán, N. (2017). Dárci oxidu dusnatého pro léčbu zanedbávaných nemocí. U dárců oxidu dusnatého. Obnoveno ze sciencedirect.com.
- Duranski, M.R. et al. (2005). Cytoprotektivní účinky dusitanů během in vivo ischemie-reperfuze srdce a jater. J Clin Invest 2005; 115 (5): 1232-1240. Obnoveno z ncbi.nlm.nih.gov.
- Cotton, F. Albert a Wilkinson, Geoffrey. (1980). Pokročilá anorganická chemie. Čtvrté vydání. John Wiley & Sons.



Zatím žádné komentáře