
Vlastnosti endotermické reakce, rovnice a příklady

A endotermická reakce Je to ten, který se musí uskutečnit, musí absorbovat energii ve formě tepla nebo záření ze svého okolí. Obecně, ale ne vždy, je lze rozpoznat podle poklesu teploty v jejich okolí; nebo naopak potřebují zdroj tepla, jako je například zdroj získaný hořícím plamenem.
Absorpce energie nebo tepla je to, co mají všechny endotermické reakce společné; jejich povaha i transformace jsou velmi různorodé. Kolik tepla by měli absorbovat? Odpověď závisí na jeho termodynamice: teplotě, při které k reakci dochází spontánně.

Například jednou z nejtypičtějších endotermických reakcí je změna stavu z ledu na kapalnou vodu. Led musí absorbovat teplo, dokud jeho teplota nedosáhne přibližně 0 ° C; při této teplotě se jeho tavení stává spontánním a led bude absorbovat, dokud se úplně neroztaví.
V horkých prostorách, například na břehu pláže, jsou teploty vyšší, a proto led rychleji absorbuje teplo; to znamená, že se taje rychleji. Tání ledovců je příkladem nežádoucí endotermické reakce.
Proč se to děje takhle? Proč se led nemůže jevit jako horká pevná látka? Odpověď spočívá v průměrné kinetické energii molekul vody v obou státech a v tom, jak vzájemně interagují prostřednictvím svých vodíkových vazeb..
V kapalné vodě mají její molekuly větší volnost pohybu než v ledu, kde ve svých krystalech stacionárně vibrují. Aby se molekuly mohly pohybovat, musí absorbovat energii takovým způsobem, aby jejich vibrace narušily silné směrové vodíkové vazby v ledu..
Z tohoto důvodu led absorbuje teplo, aby se roztavil. Aby mohl existovat „horký led“, musely by být vodíkové vazby neobvykle silné, aby se roztavily při teplotě výrazně nad 0 ° C..
Rejstřík článků
- 1 Charakteristika endotermické reakce
- 1,1 ΔH> 0
- 1.2 Ochlazují své okolí
- 2 Rovnice
- 3 Příklady běžných endotermických reakcí
- 3.1 Odpařování suchého ledu
- 3.2 Pečení chleba nebo vaření jídla
- 3.3 Opalování
- 3.4 Reakce tvorby atmosférického dusíku a ozonu
- 3.5 Elektrolýza vody
- 3.6 Fotosyntéza
- 3.7 Roztoky některých solí
- 3.8 Tepelné rozklady
- 3.9 Chlorid amonný ve vodě
- 3.10 Triosíran sodný
- 3.11 Automobilové motory
- 3.12 Vroucí kapaliny
- 3.13 Vaření vejce
- 3.14 Vaření jídla
- 3.15 Ohřev jídla v mikrovlnné troubě
- 3.16 Lisování skla
- 3.17 Spotřeba svíčky
- 3.18 Čištění horkou vodou
- 3.19 Tepelná sterilizace potravin a jiných předmětů
- 3.20 Boj proti infekcím s horečkou
- 3.21 Odpařování vody
- 4 Odkazy
Vlastnosti endotermické reakce
Změna stavu není správně chemická reakce; Stává se však totéž: produkt (kapalná voda) má vyšší energii než reaktant (led). Toto je hlavní charakteristika endotermické reakce nebo procesu: produkty jsou energetičtější než reaktanty.
I když je to pravda, neznamená to, že produkty musí být nutně nestabilní. V případě, že ano, endotermická reakce již není spontánní za všech podmínek teploty nebo tlaku..
Zvažte následující chemickou rovnici:
A + Q => B
Kde Q představuje teplo, obvykle vyjádřené v jednotkách joule (J) nebo kalorií (cal). Protože A absorbuje teplo Q a přeměňuje se na B, říká se, že jde o endotermickou reakci. B má tedy více energie než A a musí absorbovat dostatek energie, aby dosáhlo své transformace.
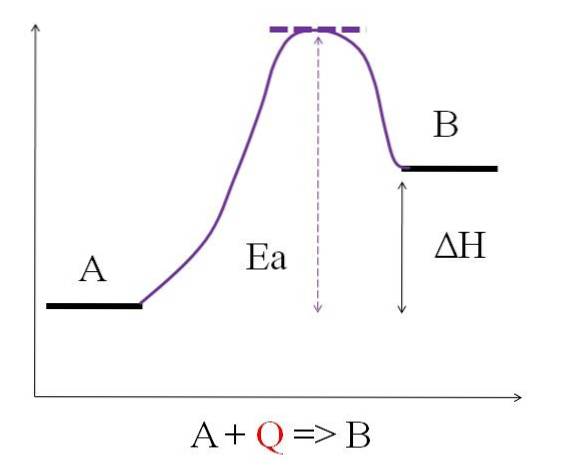
Jak je vidět na výše uvedeném diagramu, A má méně energie než B. Množství tepla Q absorbovaného A je takové, že překonává aktivační energii (energii potřebnou k dosažení fialového vrcholu s tečkovanou střechou). Rozdíl v energii mezi A a B je známý jako entalpie reakce, ΔH.
ΔH> 0
Všechny endotermické reakce mají výše uvedený diagram společný, protože produkty jsou energetičtější než reaktanty. Proto je energetický rozdíl mezi nimi, ΔH, vždy pozitivní (HProdukt-HČinidlo > 0). Jelikož je to pravda, k zajištění této energetické potřeby musí existovat absorpce tepla nebo energie z okolí..
A jak jsou takové výrazy interpretovány? Při chemické reakci se vazby vždy rozbijí, aby se vytvořily nové. K jejich rozbití je nezbytná absorpce energie; to je, je to endotermický krok. Mezitím tvorba vazeb implikuje stabilitu, jedná se tedy o exotermický krok..
Když vytvořené vazby neposkytují stabilitu srovnatelnou s množstvím energie potřebné k rozbití starých vazeb, jedná se o endotermickou reakci. To je důvod, proč je zapotřebí další energie k podpoře rozbíjení nejstabilnějších vazeb v reaktantech..
Na druhou stranu v exotermních reakcích dochází k opačnému: uvolňuje se teplo a ΔH je < 1 (negativo). Aquí los productos son más estables que los reactivos, y el diagrama entre A y B cambia de forma; ahora B se ubica por debajo de A, y la energía de activación es menor.
Chladí své okolí
Ačkoli to neplatí pro všechny endotermické reakce, některé z nich způsobují snížení teploty v jejich okolí. Je to proto, že absorbované teplo pochází odněkud. V důsledku toho, pokud by se přeměna A a B prováděla uvnitř nádoby, ochladila by se.
Čím endotermnější reakce, tím chladnější bude nádoba a její okolí. Některé reakce jsou dokonce schopné vytvořit tenkou vrstvu ledu, jako by vyšly z ledničky..
Existují však reakce tohoto typu, které neochladí jejich okolí. Proč? Protože okolní teplo je nedostatečné; to znamená, že neposkytuje potřebné Q (J, cal), které je zapsáno v chemických rovnicích. Proto se jedná o vstup ohně nebo ultrafialového záření..
Mezi těmito dvěma scénáři může dojít k malé záměně. Na jedné straně je teplo z okolí dostatečné na to, aby reakce probíhala spontánně, a je pozorováno ochlazení; a na druhé straně je zapotřebí více tepla a používá se efektivní metoda ohřevu. V obou případech se stane totéž: energie je absorbována.
Rovnice
Jaké jsou relevantní rovnice v endotermické reakci? Jak již bylo vysvětleno, ΔH musí být kladné. Při výpočtu se nejprve zváží následující chemická rovnice:
aA + bB => cC + dD
Kde A a B jsou reaktanty a C a D jsou produkty. Malá písmena (a, b, c a d) jsou stechiometrické koeficienty. Pro výpočet ΔH této obecné reakce se použije následující matematický výraz:
ΔHprodukty- ΔHČinidla = ΔHrxn
Můžete pokračovat přímo nebo provést výpočty samostatně. Pro ΔHprodukty je třeba vypočítat následující součet:
c ΔHFC + d ΔHFD
Kde ΔHF je entalpie tvorby každé látky zapojené do reakce. Podle konvence mají látky v jejich nejstabilnějších formách ΔHF= 0. Například molekuly Odva a Hdva, nebo pevný kov, mají ΔHF= 0.
Stejný výpočet je nyní proveden pro reaktanty, ΔHČinidla:
a ΔHFA + b ΔHFB
Ale protože rovnice říká, že ΔHČinidla musí být odečteno od ΔHprodukty, pak výše uvedený součet musí být vynásoben -1. Takže máš:
c ΔHFC + d ΔHFD - (a ΔHFA + b ΔHFB)
Pokud je výsledkem tohoto výpočtu kladné číslo, pak jde o endotermickou reakci. A pokud je test negativní, jedná se o exotermickou reakci.
Příklady běžných endotermických reakcí
Odpařování suchého ledu

Každý, kdo někdy viděl ty bílé výpary vycházející ze zmrzlinového vozíku, byl svědkem jednoho z nejběžnějších příkladů endotermické „reakce“..
Kromě některých zmrzlin byly tyto páry, které se uvolňují z bílých pevných látek, nazývaných suchý led, také součástí scénářů, které vytvářejí účinek mlhy. Tento suchý led není nic jiného než pevný oxid uhličitý, který se při absorpci teploty a před vnějším tlakem začne sublimovat.
Experimentem pro dětské publikum by bylo naplnění a utěsnění vaku suchým ledem. Po chvíli se nakonec nafoukne kvůli COdva plynný, který generuje práci nebo tlačí vnitřní stěny vaku proti atmosférickému tlaku.
Pečení chleba nebo vaření jídla

Pečení chleba je příkladem chemické reakce, protože nyní dochází k chemickým změnám způsobeným teplem. Každý, kdo ucítil vůni čerstvě upečeného chleba, ví, že dochází k endotermické reakci.
Těsto a všechny jeho přísady potřebují teplo v peci k provedení všech transformací, které jsou nezbytné k tomu, aby se staly chlebem a vykazovaly své typické vlastnosti..
Kromě chleba je kuchyně plná příkladů endotermických reakcí. Kdokoli vaří, jedná s nimi denně. Vaření těstovin, změkčení jader, ohřívání kukuřičných zrn, vaření vajec, koření masa, pečení dortu, vaření čaje, ohřívání sendvičů; každá z těchto činností jsou endotermické reakce.
Opalování

Jakkoli se mohou zdát jednoduché a běžné, sluneční koupele, které požívají někteří plazi, jako jsou želvy a krokodýli, spadají do kategorie endotermických reakcí. Želvy absorbují teplo ze slunce, aby regulovaly svoji tělesnou teplotu.
Bez slunce udržují teplo vody, aby se zahřály; který končí ochlazením vody ve vašich rybnících nebo nádržích na ryby.
Reakce tvorby atmosférického dusíku a ozonu

Vzduch se skládá hlavně z dusíku a kyslíku. Během elektrických bouří se uvolňuje taková energie, že může rozbít silné vazby, které drží atomy dusíku pohromadě v molekule N.dva:
Ndva + NEBOdva + Q => 2NO
Na druhou stranu může kyslík absorbovat ultrafialové záření a stát se ozonem; allotrope kyslíku, který je ve stratosféře velmi prospěšný, ale škodlivý pro život na úrovni země. Reakce je:
3Odva + v => 2O3
Kde v znamená ultrafialové záření. Mechanismus za touto jednoduchou rovnicí je velmi složitý.
Elektrolýza vody
Elektrolýza využívá elektrickou energii k oddělení molekuly na její formující se prvky nebo molekuly. Například při elektrolýze vody vznikají dva plyny: vodík a kyslík, každý v různých elektrodách:
2HdvaO => 2Hdva + NEBOdva
Stejnou reakci může podstoupit i chlorid sodný:
2NaCl => 2Na + Cldva
V jedné elektrodě uvidíte tvorbu kovového sodíku a ve druhé nazelenalé bubliny chloru.
Fotosyntéza

Rostliny a stromy potřebují absorbovat sluneční světlo jako zdroj energie k syntéze svých biomateriálů. K tomu používá CO jako surovinu.dva a voda, která se během dlouhé řady kroků přemění na glukózu a další cukry. Kromě toho se tvoří kyslík, který se uvolňuje z listů.
Roztoky některých solí
Pokud je chlorid sodný rozpuštěn ve vodě, nedojde ke znatelné změně vnější teploty sklenice nebo nádoby..
Některé soli, jako je chlorid vápenatý, CaCldva, zvýšit teplotu vody jako produkt velké hydratace iontů Ca.dva+. A další soli, jako je dusičnan amonný nebo chlorid, NH4NE3 a NH4Cl, snižte teplotu vody a ochlaďte její okolí.
V učebnách se domácí experimenty obvykle provádějí rozpuštěním některých z těchto solí, aby se prokázalo, co je to endotermická reakce..
Pokles teploty je způsoben hydratací iontů NH4+ není upřednostňován proti rozpuštění krystalického uspořádání jeho solí. V důsledku toho soli absorbují teplo z vody, aby umožnily solvataci iontů..
Další chemická reakce, kterou je obvykle velmi běžné prokázat, je následující:
Ba (OH)dva8HdvaO + 2NH4NE3 => Ba (č3)dva + 2NH3 +10HdvaNEBO
Všimněte si množství vytvořené vody. Smícháním obou pevných látek se získá vodný roztok Ba (NO3)dva, vůně čpavku a pokles teploty tak, že doslova zmrzne vnější povrch nádoby.
Tepelné rozklady
Jedním z nejběžnějších tepelných rozkladů je hydrogenuhličitan sodný, NaHCO3, vyrábět COdva a voda při zahřátí. Mnoho pevných látek, včetně uhličitanů, se často rozpadá a uvolňuje COdva a odpovídající oxid. Například rozklad uhličitanu vápenatého je následující:
Zloděj3 + Q => CaO + COdva
Totéž se děje s uhličitany hořčíku, stroncia a baria.
Je důležité si uvědomit, že tepelný rozklad se liší od spalování. V prvním případě nedochází k vznícení nebo se uvolňuje teplo, zatímco ve druhém; to znamená, že spalování je exotermická reakce, i když potřebuje, aby došlo k počátečnímu zdroji tepla nebo k němu došlo spontánně.
Chlorid amonný ve vodě
Když se ve zkumavce rozpustí ve vodě malé množství chloridu amonného (NH4CI), zkumavka se ochladí než dříve. Během této chemické reakce je teplo absorbováno z prostředí.
Triosíran sodný
Když krystaly thiosíranu sodného (NadvaSdvaNEBO3.5HdvaO), běžně nazývaný škytavka, se rozpouští ve vodě, dochází k ochlazení.
Automobilové motory
Při spalování benzínu nebo nafty v motorech automobilů, nákladních vozidel, traktorů nebo autobusů vzniká mechanická energie, která se využívá při oběhu těchto vozidel.
Vroucí kapaliny
Zahřátím kapaliny získává energii a přechází do plynného stavu.
Uvařte vejce
Když se aplikuje teplo, vaječné proteiny jsou denaturovány a tvoří pevnou strukturu, která je obvykle přijímána..
Vaří jídlo
Obecně platí, že vždy, když se vaří teplem, aby se změnily vlastnosti jídla, dochází k endotermickým reakcím.
Tyto reakce způsobují, že jídlo měkne, vytváří tvárnou hmotu, uvolňuje složky, které obsahuje, mimo jiné..
Ohřívání jídla v mikrovlnné troubě
Mikrovlnným zářením molekuly vody v potravinách absorbují energii, začnou vibrovat a zvyšují teplotu jídla.
Lisování skla
Absorpce tepla sklem činí jeho klouby pružnými, což usnadňuje jeho tvar.
Spotřeba svíčky
Svíčkový vosk se taví tím, že absorbuje teplo z plamene a mění svůj tvar.
Čištění horkou vodou
Při použití horké vody k čištění předmětů znečištěných mastnotou, jako jsou hrnce nebo oděvy, se tuk stane tekutějším a snáze se odstraní.
Tepelná sterilizace potravin a jiných předmětů
Při ohřívání předmětů nebo potravin také mikroorganismy, které obsahují, zvyšují svoji teplotu.
Když je dodáváno velké množství tepla, dochází k reakcím uvnitř mikrobiálních buněk. Mnoho z těchto reakcí, jako je rozbití vazeb nebo denaturace proteinů, nakonec mikroorganismy zabije.
Bojujte s infekcemi horečkou
Když dojde k horečce, je to proto, že tělo produkuje potřebné teplo k zabíjení bakterií a virů, které způsobují infekce a vytvářejí nemoci..
Pokud je generovaného tepla hodně a vysoká horečka, jsou ovlivněny také buňky těla a existuje riziko smrti.
Odpařování vody
Když se voda odpaří a promění se v páru, je to kvůli teplu, které přijímá z prostředí. Protože každá molekula vody přijímá tepelnou energii, její vibrační energie se zvyšuje do bodu, kdy se může volně pohybovat a vytvářet páru..
Reference
- Whitten, Davis, Peck a Stanley. (2008). Chemie. (8. vydání). Učení CENGAGE.
- Wikipedia. (2018). Endotermický proces. Obnoveno z: en.wikipedia.org
- Helmenstine, Anne Marie, Ph.D. (27. prosince 2018). Příklady endotermické reakce. Obnoveno z: thoughtco.com
- Khan Academy. (2019). Endotermický vs. exotermické reakce. Obnoveno z: khanacademy.org
- Serm Murmson. (2019). Co se děje na molekulární úrovni během endotermické reakce? Hearst Seattle Media. Obnoveno z: education.seattlepi.com
- QuimiTube. (2013). Výpočet entalpie reakce z entalpií formace. Obnoveno z: quimitube.com
- Quimicas.net (2018). Příklady endotermické reakce. Obnoveno z:
chemistry.net.



Zatím žádné komentáře