
Vlastnosti atomu uhlíku, struktura, hybridizace

The atom uhlíku je to možná nejdůležitější a symbolický ze všech prvků, protože díky němu je možná existence života. Uzavírá v sobě nejen několik elektronů nebo jádro s protony a neutrony, ale také hvězdný prach, který končí začleněn a tvoří živé bytosti.
Stejně tak se atomy uhlíku nacházejí v zemské kůře, i když ne v hojném množství srovnatelném s kovovými prvky, jako je železo, uhličitany, oxid uhličitý, olej, diamanty, sacharidy atd., Jsou součástí jejích fyzikálních a chemických projevů.
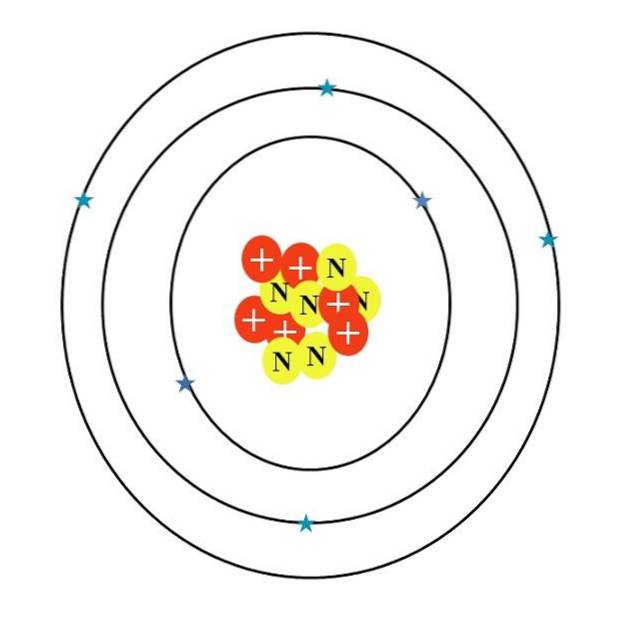
Jaký je ale atom uhlíku? První nepřesná skica je ta, která je vidět na obrázku výše, jejíž charakteristiky jsou popsány v následující části.
Atomy uhlíku procházejí atmosférou, mořem, podloží, rostlinami a jakýmikoli živočišnými druhy. Jeho velká chemická rozmanitost je způsobena vysokou stabilitou jeho vazeb a způsobem, jakým jsou uspořádány v prostoru. Na jedné straně tedy existuje měkký a mazací grafit; a na druhé straně diamant, jehož tvrdost předčí tvrdost mnoha materiálů.
Pokud by atom uhlíku neměl vlastnosti, které ho charakterizují, organická chemie by neexistovala úplně. Někteří vizionáři v tom vidí nové materiály budoucnosti prostřednictvím designu a funkcionalizace jejich alotropních struktur (uhlíkové nanotrubice, grafen, fullereny atd.).
Rejstřík článků
- 1 Vlastnosti atomu uhlíku
- 2 Struktura
- 3 Hybridizace
- 3,1 sp3
- 3,2 sp2 a sp
- 4 Klasifikace
- 4.1 Primární
- 4.2 Sekundární
- 4.3 Terciární
- 4.4 Čtvrtletní
- 5 použití
- 5.1 Jednotka atomové hmotnosti
- 5.2 Uhlíkový cyklus a životnost
- 5,3 13C NMR spektroskopie
- 6 Reference
Vlastnosti atomu uhlíku
Atom uhlíku je symbolizován písmenem C. Jeho atomové číslo Z je 6, proto má šest protonů (červené kruhy se symbolem „+“ v jádře). Kromě toho má šest neutronů (žluté kruhy s písmenem „N“) a nakonec šest elektronů (modré hvězdy).
Součet hmotností jeho atomových částic dává průměrnou hodnotu 12,0107 u. Atom na obrázku však odpovídá izotopu uhlíku 12 (12C), který se skládá z d. Jiné izotopy, jako např 13C a 14C, méně hojný, se liší pouze počtem neutronů.
Pokud tedy byly tyto izotopy nakresleny 13C by měl další žlutý kruh a 14C, další dva. To logicky znamená, že se jedná o těžší atomy uhlíku..
Kromě toho, jaké další vlastnosti lze v tomto ohledu zmínit? Je čtyřmocný, to znamená, že může tvořit čtyři kovalentní vazby. Nachází se ve skupině 14 (IVA) periodické tabulky, konkrétněji v bloku p.
Je to také velmi univerzální atom, schopný vazby s téměř všemi prvky periodické tabulky; zejména sám se sebou, tvoří lineární, rozvětvené a laminární makromolekuly a polymery.
Struktura
Jaká je struktura atomu uhlíku? Chcete-li odpovědět na tuto otázku, musíte nejprve přejít na jeho elektronickou konfiguraci: 1sdva2 sdva2 strdva nebo [He] 2 sdva2 strdva.
Proto existují tři orbitaly: 1sdva, 2sdva a 2pdva, každý se dvěma elektrony. To je také vidět na obrázku výše: tři prsteny se dvěma elektrony (modré hvězdy), každý (nezaměňujte prsteny za oběžné dráhy: jsou to orbitaly).
Mějte však na paměti, že dvě hvězdy mají tmavší odstín modré barvy než zbývající čtyři. Proč? Protože první dva odpovídají vnitřní vrstvě 1 sdva nebo [He], který se přímo nepodílí na tvorbě chemických vazeb; zatímco elektrony vnějšího pláště, 2s a 2p, ano.
Orbitály s a p nemají stejný tvar, takže ilustrovaný atom nesouhlasí s realitou; kromě velké disproporce vzdálenosti mezi elektrony a jádrem, která by měla být stokrát větší.
Struktura atomu uhlíku se proto skládá ze tří orbitalů, kde se elektrony „taví“ do rozmazaných elektronických mraků. A mezi jádrem a těmito elektrony je vzdálenost, která odhaluje obrovské „vakuum“ uvnitř atomu..
Hybridizace
Již bylo zmíněno, že atom uhlíku je čtyřmocný. Podle jeho elektronické konfigurace jsou jeho 2s elektrony spárovány a 2p elektrony spárovány:
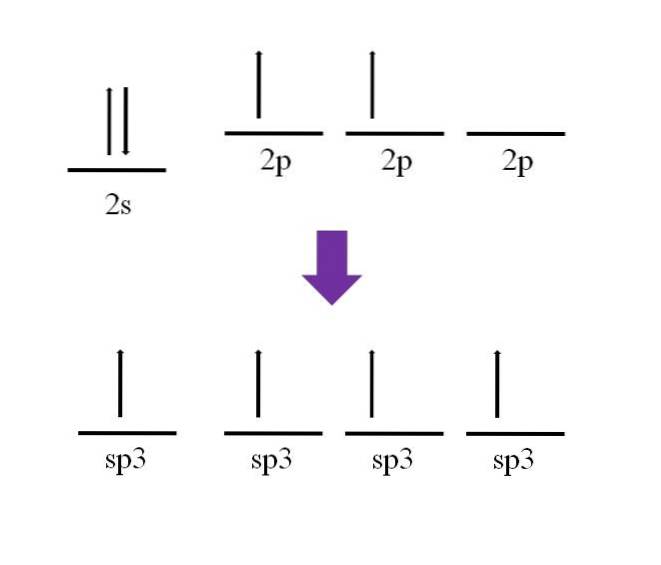
K dispozici je jeden p orbitál, který je prázdný a naplněný dalším elektronem na atomu dusíku (2 p3).
Podle definice kovalentní vazby je nutné, aby každý atom přispíval k tvorbě elektronu; je však vidět, že v základní stav atomu uhlíku má pouze dva nepárové elektrony (jeden v každé 2p oběžné dráze). To znamená, že v tomto stavu jde o dvojmocný atom, a proto tvoří pouze dvě vazby (-C-).
Jak je tedy možné, aby atom uhlíku vytvořil čtyři vazby? K tomu musíte podporovat elektron z orbitálu 2 s na orbitál 2p s vyšší energií. Toto je hotové, výsledné čtyři orbitaly jsou degenerovat; jinými slovy, mají stejnou energii nebo stabilitu (všimněte si, že jsou vyrovnány).
Tento proces je znám jako hybridizace a díky němu má atom uhlíku nyní čtyři sp orbitaly3 s jedním elektronem za vzniku čtyř vazeb. To je způsobeno jeho charakteristikou čtyřmocnosti.
sp3
Když má atom uhlíku sp hybridizaci3, orientuje své čtyři hybridní orbitaly na vrcholy čtyřstěnu, což je jeho elektronická geometrie.
Lze tedy identifikovat uhlík sp3 protože tvoří pouze čtyři jednoduché vazby, jako v molekule metanu (CH4). A kolem toho lze pozorovat čtyřboké prostředí.
Překrytí sp orbitalů3 je tak efektivní a stabilní, že jednoduchá vazba C-C má entalpii 345,6 kJ / mol. To vysvětluje, proč existují nekonečné karbonátové struktury a nesmírné množství organických sloučenin. Kromě toho mohou atomy uhlíku vytvářet další typy vazeb.
spdva a sp
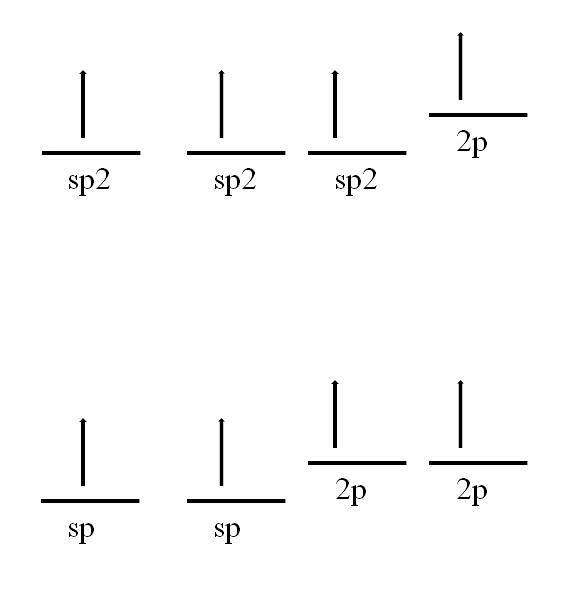
Atom uhlíku je také schopen přijmout další hybridizace, které mu umožní vytvořit dvojnou nebo dokonce trojnou vazbu.
V hybridizaci spdva, jak je vidět na obrázku, existují tři sp orbitalydva zdegenerovaný a orbitál 2p zůstává nezměněn nebo „čistý“. Se třemi sp orbitálydva Uhel 120 ° od sebe tvoří tři kovalentní vazby, které kreslí elektronickou geometrii trigonální roviny; zatímco s orbitálem 2p, kolmým na další tři, tvoří vazbu π: -C = C-.
V případě sp hybridizace existují dva sp orbitaly vzdálené 180 ° od sebe tak, že vykreslují lineární elektronickou geometrii. Tentokrát mají dva čisté 2p orbitaly, kolmé na sebe, které umožňují uhlíku tvořit trojné vazby nebo dvě dvojné vazby: -C≡C- nebo ·· C = C = C ·· (centrální uhlík má sp hybridizaci ).
Všimněte si, že vždy (obecně), pokud jsou přidány vazby kolem uhlíku, bude zjištěno, že počet se rovná čtyřem. Tato informace je nezbytná při kreslení Lewisových struktur nebo molekulárních struktur. Atom uhlíku tvořící pět vazeb (= C≡C) je teoreticky a experimentálně nepřípustný.
Klasifikace
Jak jsou klasifikovány atomy uhlíku? Více než klasifikace podle vnitřních charakteristik ve skutečnosti závisí na molekulárním prostředí. To znamená, že v molekule lze jeho atomy uhlíku klasifikovat podle následujícího.
Hlavní
Primární uhlík je takový, který je vázán pouze na jeden další uhlík. Například molekula etanu, CH3-CH3 Skládá se ze dvou vázaných primárních uhlíků. To signalizuje konec nebo začátek uhlíkového řetězce.
Sekundární
Je to jeden, který je spojen se dvěma uhlíky. Pro molekulu propanu tedy CH3-CHdva-CH3, střední atom uhlíku je sekundární (methylenová skupina, -CHdva-).
Terciární
Terciární uhlíky se liší od ostatních, protože z nich vycházejí větve hlavního řetězce. Například 2-methylbutan (také nazývaný isopentan), CH3-CH(CH3) -CHdva-CH3 má terciární uhlík zvýrazněný tučně.
Kvartérní
A konečně, kvartérní uhlíky, jak naznačuje jejich název, jsou spojeny se čtyřmi dalšími atomy uhlíku. Molekula neopentanu, C(CH3)4 má kvartérní atom uhlíku.
Aplikace
Jednotka atomové hmotnosti
Průměrná atomová hmotnost 12C se používá jako standardní měřítko pro výpočet hmotností ostatních prvků. Vodík tedy váží jednu dvanáctinu tohoto izotopu uhlíku, který se používá k definování toho, co je známé jako atomová hmotnostní jednotka u.
Ostatní atomové hmotnosti lze tedy srovnávat s hmotami atomu 12C a 1H. Například hořčík (24Mg) váží přibližně dvojnásobek hmotnosti atomu uhlíku a 24krát více než atom vodíku.
Uhlíkový cyklus a život
Rostliny absorbují COdva v procesu fotosyntézy uvolňovat kyslík do atmosféry a působit jako plíce rostlin. Když zemřou, přemění se na dřevěné uhlí, které po spálení znovu uvolňuje COdva. Jedna část se vrací k rostlinám, ale druhá končí na mořských lůžkách a vyživuje mnoho mikroorganismů.
Když mikroorganismy zemřou, pevná látka, která zůstane ve svém biologickém rozkladu, se usadí a po milionech let se přemění na ropu..
Když lidstvo používá tento olej jako alternativní zdroj energie ke spalování uhlí, přispívá k uvolňování více COdva (a další nežádoucí plyny).
Na druhou stranu život používá atomy uhlíku z hloubi nitra. To je způsobeno stabilitou jeho vazeb, která mu umožňuje vytvářet řetězce a molekulární struktury, které tvoří makromolekuly stejně důležité jako DNA..
NMR spektroskopie 13C
The 13C, i když je to v mnohem menším poměru než v 12C, jeho množství je dostatečné k objasnění molekulárních struktur pomocí uhlíkové 13 nukleární magnetické rezonanční spektroskopie.
Díky této analytické technice je možné určit, které atomy obklopují 13C a ke kterým funkčním skupinám patří. Lze tedy určit uhlíkovou kostru jakékoli organické sloučeniny..
Reference
- Graham Solomons T.W., Craig B.Fryhle. Organická chemie. Miny. (10. vydání.) Wiley Plus.
- Blake D. (4. května 2018). Čtyři charakteristiky uhlíku. Obnoveno z: sciencing.com
- Royal Society of Chemistry. (2018). Uhlí. Převzato z: rsc.org
- Pochopení evoluce. (s.f.). Cesta atomu uhlíku. Obnoveno z: evolution.berkeley.edu
- Encyklopedie Britannica. (14. března 2018). Uhlí. Obnoveno z: britannica.com
- Pappas S. (29. září 2017). Fakta o uhlíku. Obnoveno z: livescience.com



Zatím žádné komentáře