
Struktura, vlastnosti a použití oxidu berylnatého (BeO)

The oxid berylnatý (BeO) je keramický materiál, který má kromě své vysoké pevnosti a elektrického odporu tak vysokou kapacitu vedení tepla, že tvoří součást jaderných reaktorů, dokonce v této poslední vlastnosti překonává kovy..
Kromě užitečnosti jako syntetického materiálu jej lze nalézt také v přírodě, i když je vzácný. Manipulace s ním musí být prováděna opatrně, protože má schopnost vážně poškodit lidské zdraví.
V moderním světě bylo pozorováno, jak vědci sdružení s technologickými společnostmi prováděli výzkum s cílem vyvinout pokročilé materiály pro zcela specializované aplikace, jako jsou ty, které splňují polovodičové materiály a materiály pro letecký průmysl..
Výsledkem toho byl objev látek, které nám díky svým mimořádně užitečným vlastnostem a vysoké odolnosti poskytly příležitost posunout se v čase vpřed, což nám umožňuje posunout naši technologii na vyšší úroveň..
Rejstřík článků
- 1 Chemická struktura
- 2 Vlastnosti
- 2.1 Elektrická vodivost
- 2.2 Tepelná vodivost
- 2.3 Optické vlastnosti
- 2.4 Zdravotní rizika
- 3 použití
- 3.1 Elektronické aplikace
- 3.2 Jaderné aplikace
- 3.3 Další aplikace
- 4 Odkazy
Chemická struktura
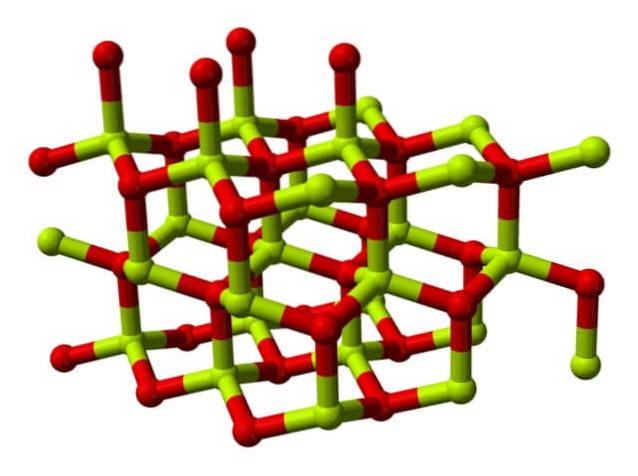
Molekula oxidu berylnatého (nazývaná také „Berilia“) Je tvořen atomem berylia a atomem kyslíku, které jsou koordinovány v čtyřboké orientaci, a krystalizuje do hexagonálních krystalických struktur zvaných wurtzity..
Tyto krystaly mají čtyřboká centra, která jsou obsazena Bedva+ mědva-. Při vysokých teplotách se struktura oxidu berylnatého stává tetragonální..
Získání oxidu berylnatého se dosahuje třemi způsoby: kalcinací uhličitanu berylnatého, dehydratací hydroxidu berylnatého nebo zapálením kovového berylia. Oxid berylnatý vytvořený při vysokých teplotách má inertní charakter, ale může být rozpuštěn různými sloučeninami.
BeCO3 + Teplo → BeO + COdva (Kalcinace)
Být (OH)dva → BeO + HdvaO (dehydratace)
2 Be + Odva → 2 BeO (zapalování)
Nakonec může být oxid berylnatý odpařen a v tomto stavu se objeví ve formě rozsivkových molekul..
Vlastnosti
Oxid berylnatý se v přírodě vyskytuje jako bromelit, bílý minerál nacházející se v některých komplexních ložiscích manganu a železa, ale nejčastěji se vyskytuje v jeho syntetické formě: bílá amorfní pevná látka, která se vyskytuje jako prášek..
Také nečistoty zachycené během výroby dávají vzorku oxidu různé barvy..
Jeho bod tání je umístěn při 2507 ° C, jeho bod varu je 3900 ° C a má hustotu 3,01 g / cm3.
Stejným způsobem je jeho chemická stabilita značně vysoká, reaguje pouze s vodní párou při teplotách blízkých 1 000 ° C a odolává procesům redukce uhlíku a útokům roztavených kovů při vysokých teplotách..
Kromě toho je jeho mechanická pevnost slušná a lze ji vylepšit designem a výrobou vhodnou pro komerční použití..
Elektrická vodivost
Oxid berylnatý je extrémně stabilní keramický materiál, a proto má poměrně vysoký elektrický odpor, což z něj činí jeden z nejlepších elektrických izolačních materiálů spolu s oxidem hlinitým..
Z tohoto důvodu se tento materiál běžně používá pro specializovaná vysokofrekvenční elektrická zařízení..
Tepelná vodivost
Oxid berylnatý má velkou výhodu, pokud jde o jeho tepelnou vodivost: je známý jako druhý nejlepší tepelně vodivý materiál mezi nekovy a je na druhém místě za diamantem, což je podstatně dražší a vzácnější materiál..
U kovů pouze měď a stříbro přenášejí teplo lépe vedením než oxid berylnatý, což z něj činí velmi žádaný materiál..
Díky svým vynikajícím tepelně vodivým vlastnostem se tato látka podílí na výrobě žáruvzdorných materiálů.
Optické vlastnosti
Díky svým krystalickým vlastnostem se oxid berylnatý používá k aplikaci transparentního materiálu na ultrafialové záření v určitých plochých obrazovkách a fotovoltaických článcích..
Podobně lze vyrobit velmi kvalitní krystaly, takže se tyto vlastnosti zlepšují v závislosti na použitém výrobním procesu..
Zdravotní rizika
Oxid berylnatý je sloučenina, se kterou je třeba zacházet velmi opatrně, protože má především karcinogenní vlastnosti, které jsou spojeny s nepřetržitým vdechováním prachu nebo par z tohoto materiálu..
Malé částice v těchto oxidových fázích ulpívají na plicích a mohou vést k tvorbě nádorů nebo onemocnění známému jako berylióza..
Berylliosis je onemocnění se střední úmrtností, které způsobuje neúčinné dýchání, kašel, úbytek hmotnosti a horečku a tvorbu granulomů v plicích nebo jiných postižených orgánech..
Existují také zdravotní rizika z přímého kontaktu oxidu berylnatého s pokožkou, protože je žíravý a dráždivý a může způsobit poškození povrchu kůže a sliznic. Při práci s tímto materiálem musí být chráněny dýchací cesty a ruce, zejména v práškové formě..
Aplikace
Použití oxidu berylnatého se dělí hlavně na tři: elektronické, jaderné a další aplikace..
Elektronické aplikace
Schopnost přenášet teplo na vysoké úrovni a jeho dobrá elektrická rezistence způsobily, že oxid berylnatý je velmi užitečný jako chladič..
Jeho použití bylo doloženo jak v obvodech vysokokapacitních počítačů, tak i v zařízeních, která zpracovávají vysoké proudy elektřiny..
Oxid berylnatý je transparentní pro rentgenové záření a mikrovlnné záření, proto se kromě antén, komunikačních systémů a mikrovlnných trub používá také v oknech proti těmto typům záření..
Jaderné aplikace
Jeho schopnost zmírňovat neutrony a udržovat svou strukturu pod radiačním bombardováním vedla k tomu, že se oxid berylnatý podílel na konstrukci jaderných reaktorů a lze jej také použít ve vysokoteplotních plynem chlazených reaktorech..
Další aplikace
Nízká hustota oxidu berylnatého vyvolala zájem o letecký a vojenský technologický průmysl, protože může představovat variantu s nízkou hmotností v raketových motorech a neprůstřelných vestách..
Nakonec byl nedávno použit jako žáruvzdorný materiál při tavení kovů v metalurgickém průmyslu..
Reference
- PubChem. (s.f.). Oxid berylnatý. Citováno z pubchem.ncbi.nlm.nih.gov
- Reade. (s.f.). Beryllia / Oxid berylnatý (BeO). Obnoveno z reade.com
- Research, C. (s.f.). Oxid berylnatý - Beryllia. Obnoveno z azom.com
- Services, N. J. (s.f.). Oxid berylnatý. Obnoveno z nj.gov
- Wikipedia. (s.f.). Oxid berylnatý. Citováno z en.wikipedia.org



Zatím žádné komentáře