
Ketogeneze tělesných typů, syntéza a degradace
The ketogeneze Jedná se o proces, kterým se získává acetoacetát, β-hydroxybutyrát a aceton, které se společně nazývají ketonová tělíska. Tento složitý a jemně regulovaný mechanismus probíhá v mitochondriích, z katabolismu mastných kyselin.
K získání ketonových těl dochází, když je tělo vystaveno vyčerpávajícímu období půstu. Ačkoli jsou tyto metabolity většinou syntetizovány v jaterních buňkách, nacházejí se jako důležitý zdroj energie v různých tkáních, jako jsou kosterní svaly a v srdečních a mozkových tkáních..
Β-Hydroxybutyrát a acetoacetát jsou metabolity používané jako substráty v srdečním svalu a kůře ledvin. V mozku se ketolátky stávají důležitými zdroji energie, když tělo vyčerpalo zásoby glukózy.
Rejstřík článků
- 1 Obecná charakteristika
- 2 Druhy a vlastnosti ketonových tělísek
- 3 Syntéza ketonových tělísek
- 3.1 Podmínky pro ketogenezi
- 3.2 Mechanismus
- 3.3 β-oxidace a ketogeneze spolu souvisejí
- 3.4 Regulace β-oxidace a její vliv na ketogenezi
- 4 Degradace
- 5 Lékařský význam ketonových tělísek
- 5.1 Diabetes mellitus a akumulace ketolátek
- 6 Reference
Obecná charakteristika
Ketogeneze je považována za velmi důležitou fyziologickou funkci nebo metabolickou cestu. Obecně tento mechanismus probíhá v játrech, i když bylo prokázáno, že jej lze provést v jiných tkáních schopných metabolizovat mastné kyseliny.
Tvorba ketonových tělísek je hlavní metabolickou derivací acetyl-CoA. Tento metabolit se získává metabolickou cestou známou jako β-oxidace, což je degradace mastných kyselin.
Dostupnost glukózy v tkáních, kde dochází k β-oxidaci, určuje metabolický osud acetyl-CoA. V konkrétních situacích jsou oxidované mastné kyseliny zaměřeny téměř výhradně na syntézu ketonových těl..
Druhy a vlastnosti ketonových tělísek
Hlavním ketonovým tělem je acetoacetát nebo kyselina acetoctová, která se syntetizuje hlavně v jaterních buňkách. Ostatní molekuly, které tvoří ketolátky, jsou odvozeny od acetoacetátu.
Redukce kyseliny acetoctové vede ke vzniku D-β-hydroxybutyrátu, druhého ketonového těla. Aceton je sloučenina, která se obtížně odbourává a je produkována spontánní dekarboxylační reakcí acetoacetátu (nevyžaduje tedy zásah žádného enzymu), pokud je v krvi přítomen ve vysokých koncentracích.
Označení ketonových tělísek bylo zavedeno konvencí, protože přísně vzato β-hydroxybutyrát nemá ketonovou funkci. Tyto tři molekuly jsou rozpustné ve vodě, což usnadňuje jejich transport v krvi. Jeho hlavní funkcí je dodávat energii určitým tkáním, jako je kosterní a srdeční sval.
Enzymy podílející se na tvorbě ketonových tělísek jsou hlavně v buňkách jater a ledvin, což vysvětluje, proč jsou tato dvě místa hlavním producentem těchto metabolitů. K jeho syntéze dochází výhradně a výhradně v mitochondriální matrici buněk.
Jakmile jsou tyto molekuly syntetizovány, procházejí do krevního řečiště a přecházejí do tkání, které je vyžadují, kde jsou degradovány na acetyl-CoA..
Syntéza ketonových tělísek
Podmínky pro ketogenezi
Metabolický osud acetyl-CoA z β-oxidace závisí na metabolických požadavcích těla. To oxiduje na COdva a HdvaNebo cyklem kyseliny citronové nebo syntézou mastných kyselin, pokud je metabolismus lipidů a sacharidů v těle stabilní.
Když tělo potřebuje tvorbu sacharidů, oxaloacetát se používá k výrobě glukózy (glukoneogeneze) místo zahájení cyklu kyseliny citronové. K tomu dochází, jak již bylo zmíněno, když má tělo určitou neschopnost získat glukózu, v případech, jako je prodloužené hladovění nebo přítomnost cukrovky.
Díky tomu se acetyl-CoA vzniklý oxidací mastných kyselin používá k výrobě ketonových tělísek..
Mechanismus
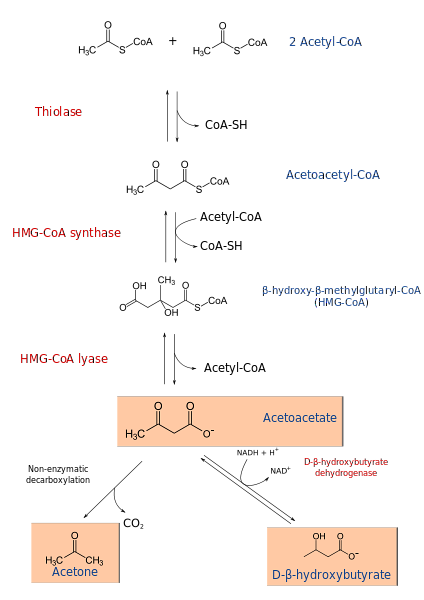
Proces ketogeneze začíná z produktů β-oxidace: acetacetyl-CoA nebo acetyl-CoA. Když je substrátem acetyl-CoA, první krok spočívá v kondenzaci dvou molekul, reakci katalyzované acetyl-CoA transferázou, za vzniku acetacetyl-CoA.
Acetacetyl-CoA kondenzuje s třetím acetyl-CoA působením HMG-CoA syntázy za vzniku HMG-CoA (β-hydroxy-β-methylglutaryl-CoA). HMG-CoA je degradován na acetoacetát a acetyl-CoA působením HMG-CoA lyázy. Tímto způsobem se získá první ketonové tělo.
Acetoacetát se redukuje na β-hydroxybutyrát působením β-hydroxybutyrátu dehydrogenázy. Tato reakce závisí na NADH.
Hlavním ketonovým tělem acetoacetátu je β-keto kyselina, která prochází neenzymatickou dekarboxylací. Tento proces je jednoduchý a produkuje aceton a COdva.
Tato série reakcí tedy vede ke vzniku ketonových tělísek. Tyto látky, které jsou rozpustné ve vodě, lze snadno transportovat krevním oběhem, aniž by bylo nutné je zakotvit do struktury albuminu, jako je tomu v případě mastných kyselin, které jsou nerozpustné ve vodném prostředí..
Β-oxidace a ketogeneze spolu souvisejí
Metabolismus mastných kyselin produkuje substráty pro ketogenezi, takže tyto dvě cesty jsou funkčně příbuzné.
Acetoacetyl-CoA je inhibitor metabolismu mastných kyselin, protože zastavuje aktivitu acyl-CoA dehydrogenázy, která je prvním enzymem beta-oxidace. Kromě toho také inhibuje acetyl-CoA transferázu a HMG-CoA syntázu.
Enzym HMG-CoA syntáza, podřízený CPT-I (enzym podílející se na produkci acylkarnitinu při β-oxidaci), hraje důležitou regulační roli při tvorbě mastných kyselin.
Regulace β-oxidace a její vliv na ketogenezi
Krmení organismů reguluje komplexní soubor hormonálních signálů. Sacharidy, aminokyseliny a lipidy spotřebované ve stravě se ukládají ve formě triacylglycerolů v tukové tkáni. Inzulin, anabolický hormon, se podílí na syntéze lipidů a tvorbě triacylglycerolů.
Na mitochondriální úrovni je β-oxidace řízena vstupem a účastí některých substrátů v mitochondriích. Enzym CPT I syntetizuje Acyl Carnitin z cytosolického Acyl CoA.
Když je tělo krmeno, aktivuje se acetyl-CoA karboxyláza a citrát zvyšuje hladiny CPT I, zatímco jeho fosforylace klesá (reakce závisí na cyklickém AMP).
To způsobí akumulaci malonyl CoA, který stimuluje syntézu mastných kyselin a blokuje jejich oxidaci, čímž brání vytváření marného cyklu..
V případě hladovění je aktivita karboxylázy velmi nízká, protože byly sníženy hladiny enzymu CPT I a byl také fosforylován, což aktivuje a podporuje oxidaci lipidů, což následně umožní tvorbu ketolátek prostřednictvím acetyl- CoA.
Degradace
Ketonová těla difundují z buněk, kde byla syntetizována, a jsou transportována do periferních tkání krevním řečištěm. V těchto tkáních mohou být oxidovány cyklem trikarboxylových kyselin.
V periferních tkáních je β-hydroxybutyrát oxidován na acetoacetát. Následně je přítomný acetoacetát aktivován působením enzymu 3-ketoacyl-CoA transferázy.
Sukcinyl-CoA působí jako dárce CoA tím, že se přeměňuje na sukcinát. K aktivaci acetoacetátu dochází, aby se zabránilo přeměně sukcinyl-CoA na cyklus v kyselině citronové na sukcinát, s vázanou syntézou GTP působením sukcinyl-CoA syntázy.
Výsledný acetoacetyl-CoA prochází thiolytickým rozkladem za vzniku dvou molekul acetyl-CoA, které jsou začleněny do cyklu trikarboxylové kyseliny, lépe známého jako Krebsův cyklus..
V jaterních buňkách chybí 3-ketoacyl-CoA transferáza, což brání aktivaci tohoto metabolitu v těchto buňkách. Tímto způsobem je zaručeno, že ketonová tělíska neoxidují v buňkách, kde byla vytvořena, ale že mohou být přenesena do tkání, kde je vyžadována jejich aktivita..
Lékařský význam ketonových tělísek
V lidském těle mohou vysoké koncentrace ketonů v krvi způsobit zvláštní stavy zvané acidóza a ketonémie..
Výroba těchto metabolitů odpovídá katabolismu mastných kyselin a sacharidů. Jednou z nejčastějších příčin patologického stavu ketogeneze je vysoká koncentrace fragmentů dikarbonátu octového, které nejsou degradovány oxidační cestou trikarboxylových kyselin..
V důsledku toho dochází ke zvýšení hladin ketolátek v krvi nad 2 až 4 mg / 100 N a jejich přítomnosti v moči. To má za následek narušení přechodného metabolismu těchto metabolitů..
Některé poruchy hypofyzárních neuroglandulárních faktorů, které regulují degradaci a syntézu ketonových tělísek, spolu s poruchami metabolismu uhlovodíků jsou příčinou stavu hyperketonémie..
Diabetes mellitus a akumulace ketolátek
Diabetes mellitus (typ 1) je endokrinní onemocnění, které způsobuje zvýšenou produkci ketolátek. Nedostatečná produkce inzulínu znemožňuje transport glukózy do svalů, jater a tukové tkáně, a tím se hromadí v krvi.
Buňky v nepřítomnosti glukózy zahajují proces glukoneogeneze a rozkladu tuků a bílkovin, aby obnovily svůj metabolismus. V důsledku toho se snižují koncentrace oxaloacetátu a zvyšuje se oxidace lipidů..
Poté dochází k akumulaci acetyl-CoA, který v nepřítomnosti oxaloacetátu nemůže sledovat dráhu kyseliny citronové, což způsobuje vysokou produkci ketonových tělísek, charakteristických pro toto onemocnění..
Akumulace acetonu je detekována jeho přítomností v moči a dechu lidí s tímto onemocněním a je ve skutečnosti jedním ze symptomů, které naznačují projev tohoto onemocnění.
Reference
- Blázquez Ortiz, C. (2004). Ketogeneze v astrocytech: charakterizace, regulace a možná cytoprotektivní role (Doktorská disertační práce, Complutense University of Madrid, publikační služba).
- Devlin, T. M. (1992). Učebnice biochemie: s klinickými korelacemi.
- Garrett, R. H. a Grisham, C. M. (2008). Biochemie. Thomson Brooks / Cole.
- McGarry, J. D., Mannaerts, G. P. a Foster, D. W. (1977). Možná úloha malonyl-CoA v regulaci oxidace jaterních mastných kyselin a ketogeneze. Žurnál klinické studie, 60(1), 265-270.
- Melo, V., Ruiz, V. M. a Cuamatzi, O. (2007). Biochemie metabolických procesů. Reverte.
- Nelson, D. L., Lehninger, A. L. a Cox, M. M. (2008). Lehningerovy principy biochemie. Macmillana.
- Pertierra, A. G., Gutiérrez, C. V. a další, C. M. (2000). Základy metabolické biochemie. Redakční Tébar.
- Voet, D. a Voet, J. G. (2006). Biochemie. Panamerican Medical Ed..



Zatím žádné komentáře