
Struktura oxidu siřičitého (SO2), vlastnosti, použití, rizika

The oxid siřičitý je plynná anorganická sloučenina tvořená sírou (S) a kyslíkem (O), jejíž chemický vzorec je SOdva. Je to bezbarvý plyn s dráždivým a dusivým zápachem. Kromě toho je rozpustný ve vodě a tvoří kyselé roztoky. Sopky ho během erupcí vypuzují do atmosféry.
Je součástí biologického a geochemického cyklu síry, ale produkuje se ve velkém množství určitými lidskými činnostmi, jako je rafinace ropy a spalování fosilních paliv (například uhlí nebo nafty)..

SOdva je to redukční činidlo, které umožňuje papírové buničině zůstat bílá po bělení jinými sloučeninami. Slouží také k odstranění stop chlóru ve vodě, která byla ošetřena touto chemikálií.
Používá se k konzervování některých druhů potravin, k dezinfekci nádob, kde se vyrábí kvašení hroznové šťávy k výrobě vína nebo ječmene k výrobě piva..
Používá se také jako fungicid v zemědělství k získání kyseliny sírové, jako rozpouštědlo a jako meziprodukt při chemických reakcích..
SOdva přítomný v atmosféře je škodlivý pro mnoho rostlin, ve vodě působí na ryby a je také jedním z těch, kteří jsou zodpovědní za „kyselý déšť“, který koroduje materiály vytvořené lidmi.
Rejstřík článků
- 1 Struktura
- 2 Názvosloví
- 3 Vlastnosti
- 3.1 Fyzický stav
- 3,2 Molekulová hmotnost
- 3.3 Teplota tání
- 3.4 Bod varu
- 3.5 Hustota
- 3.6 Rozpustnost
- 3,7 pH
- 3.8 Chemické vlastnosti
- 3.9 Vodné roztoky SO2
- 3.10 Další vlastnosti
- 4 Získání
- 5 Přítomnost v přírodě
- 6 použití
- 6.1 Při výrobě kyseliny sírové
- 6.2 Ve zpracovaném potravinářském průmyslu
- 6.3 Jako rozpouštědlo a činidlo
- 6.4 Jako redukční činidlo
- 6.5 V různých aplikacích
- 7 Účinky endogenního SO2
- 8 Rizika
- 8.1 Ekotoxicita
- 8.2 Účinky požití s jídlem
- 9 Odkazy
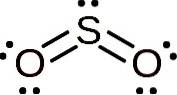
Struktura
Molekula oxidu siřičitého je symetrická a tvoří úhel. Úhel je způsoben SOdva Má pár osamělých elektronů, tj. Elektrony, které netvoří vazbu s žádným atomem, ale jsou volné.
Nomenklatura
- Oxid siřičitý
- Anhydrid síry
- Oxid siřičitý.
Vlastnosti
Fyzický stav
Bezbarvý plyn.
Molekulární váha
64,07 g / mol
Bod tání
-75,5 ° C
Bod varu
-10,05 ° C
Hustota
Plyn: 2,26 při 0 ° C (ve vztahu ke vzduchu, tj. Hustota vzduchu = 1). To znamená, že je těžší než vzduch..
Kapalina: 1,4 až -10 ° C (vzhledem k vodě, tj. Hustota vody = 1).
Rozpustnost
Rozpustný ve vodě: 17,7% při 0 ° C; 11,9% při 15 ° C; 8,5% při 25 ° C; 6,4% při 35 ° C.
Rozpustný v ethanolu, diethyletheru, acetonu a chloroformu. Je méně rozpustný v nepolárních rozpouštědlech.
pH
Vodné roztoky SOdva jsou kyselé.
Chemické vlastnosti
SOdva je to silné redukční a oxidační činidlo. V přítomnosti vzduchu a katalyzátoru oxiduje na SO3.
SWdva + NEBOdva → SO3
Osamělé páry elektronů někdy způsobují, že se chová jako Lewisova báze, jinými slovy, může reagovat se sloučeninami, kde chybí atom, který chybí elektrony.
Pokud OSdva je ve formě plynu a suchý nenapadá železo, ocel, měď-nikl nebo slitiny nikl-chrom-železo. Pokud je však v kapalném nebo mokrém stavu, způsobuje korozi těchto kovů..
SOdva kapalina s 0,2% vody nebo více vytváří silnou korozi na železo, mosaz a měď. Je korozivní pro hliník.
Je-li kapalina, může také napadnout některé plasty, gumy a povlaky.
Vodné roztoky SOdva
SOdva je velmi rozpustný ve vodě. Dlouho se uvažovalo o tom, že ve vodě tvoří kyselinu sírovou HdvaSW3, ale existence této kyseliny nebyla prokázána.
V OS řešeníchdva ve vodě nastávají následující rovnováhy:
SWdva + HdvaO ⇔ SOdva.HdvaNEBO
SWdva.HdvaO ⇔ HSO3- + H3NEBO+
HSO3- + HdvaO ⇔ SO3dva- + H3NEBO+
Kde HSO3- je hydrogensiřičitanový iont a SO3dva- je siřičitanový ion. Siřičitanový ion SO3dva- nastává hlavně při přidání alkálie k roztoku SOdva.
Vodné roztoky SOdva mají redukční vlastnosti, zejména pokud jsou zásadité.
Další vlastnosti
- Je extrémně tepelně stabilní, dokonce až do 2 000 ° C.
- Není hořlavý.
Získávání
SOdva Získává se spalováním síry (S) ve vzduchu, i když se také tvoří malé množství SO3.
S + Odva → SOdva
Může být také vyroben zahříváním různých sulfidů ve vzduchu, spalováním pyritových minerálů a minerálů obsahujících sulfidy..
V případě pyritu železa se po oxidaci získá oxid železitý (iii) a SO.dva:
4 FeSdva + 11 O.dva → 2 FedvaNEBO3 + 8 SOdva↑
Přítomnost v přírodě
SOdva Je uvolňován do atmosféry aktivitou sopek (9%), ale je také způsoben jinými přírodními aktivitami (15%) a lidskou činností (76%).
Výbušné sopečné erupce způsobují významné každoroční výkyvy nebo variace SOdva v atmosféře. Odhaduje se, že 25% SOdva emitované sopkami je odplaveno deštěm před dosažením stratosféry.
Přírodní zdroje jsou nejhojnější a jsou způsobeny biologickým cyklem síry.
V městských a průmyslových oblastech převládají lidské zdroje. Hlavní lidskou činností, která ho produkuje, je spalování fosilních paliv, jako je uhlí, benzín a nafta. Dalšími lidskými zdroji jsou ropné rafinerie, chemické závody a výroba plynu.

U savců se generuje endogenně, tj. V těle zvířat a lidí v důsledku metabolismu aminokyselin obsahujících síru (S), zejména L-cysteinu..
Aplikace
Při výrobě kyseliny sírové
Jedna z nejdůležitějších aplikací operačního systémudva je při získávání kyseliny sírové HdvaSW4.
2 SOdva + 2 hdvaO + Odva → 2 HdvaSW4
Ve zpracovaném potravinářském průmyslu
Oxid siřičitý se používá jako konzervační prostředek a stabilizátor potravin, jako prostředek regulující vlhkost a jako modifikátor chuti a textury v některých jedlých výrobcích..
Používá se také k dezinfekci zařízení, která přicházejí do styku s potravinami, fermentačních zařízení, jako jsou například v pivovarech a vinařstvích, nádobách na potraviny atd..
Umožňuje konzervovat ovoce a zeleninu, zvyšuje jejich trvanlivost, zabraňuje ztrátě barvy a chuti a pomáhá při zadržování vitaminu C (kyselina askorbová) a karotenů (prekurzory vitaminu A)..

Používá se k konzervování vína, protože ničí bakterie, houby a nežádoucí kvasinky. Používá se také ke sterilizaci a prevenci tvorby nitrosaminů v pivu..

Používá se také k máčení kukuřičných zrn, k bělení řepného cukru a jako antimikrobiální látka při výrobě kukuřičného sirupu s vysokým obsahem fruktózy..
Jako rozpouštědlo a činidlo
Bylo široce používáno jako nevodné rozpouštědlo. Ačkoli se nejedná o ionizující rozpouštědlo, je užitečné jako bezprotonové rozpouštědlo pro určité analytické aplikace a chemické reakce..
Používá se jako rozpouštědlo a činidlo v organické syntéze, meziprodukt při výrobě dalších sloučenin, jako je oxid chloričitý, acetylchlorid a při sulfonaci olejů..
Jako redukční činidlo
Používá se jako redukční činidlo, i když není tak silné, a v alkalickém roztoku se tvoří siřičitanový ion, což je energetičtější redukční činidlo..
V různých aplikacích
SOdva používá se také:
- V zemědělství jako fungicid a konzervační prostředek na hrozny po sklizni.
- K výrobě hydrosulfitů.
- K bělení buničiny a papíru, protože umožňuje stabilizaci buničiny po bělení peroxidem vodíku HdvaNEBOdva; SOdva působí zničením HdvaNEBOdva zbytek a tím udržovat jas buničiny, protože HdvaNEBOdva může způsobit obrácení jasu.
- K bělení textilních vláken a proutěných předmětů.
- K úpravě vody, protože eliminuje zbytkový chlór, který zůstává po chloraci pitné vody, odpadní vody nebo průmyslové vody.
- Při rafinaci minerálů a kovů jako redukční činidlo pro železo během zpracování minerálů.
- V rafinaci ropy k zachycení kyslíku a zpomalení koroze a jako extrakční rozpouštědlo.
- Jako antioxidant.
- Jako alkalický neutralizátor při výrobě skla.
- V lithiových bateriích jako oxidační činidlo.
Účinky OSdva endogenní
Některé studie odhalily, že SOdva endogenní nebo produkované samotným tělem má příznivý účinek na kardiovaskulární systém, včetně regulace srdeční funkce a relaxace cév.
Když se SO vytváří v těledva se stává jeho deriváty hydrogensiřičitanem HSO3- a siřičitan SO3dva-, které působí vazo-relaxační účinek na tepny.
SOdva endogenně snižuje hypertenzi, předchází rozvoji aterosklerózy a chrání srdce před poškozením myokardu. Má také antioxidační účinek, potlačuje zánět a apoptózu (programovaná buněčná smrt).
Z těchto důvodů se předpokládá, že může jít o možnou novou terapii kardiovaskulárních onemocnění..
Rizika
- Vystavení SOdva plynné mohou vést k popáleninám očí, kůže, hrdla a sliznic, poškození průdušek a plic.
- Některé studie uvádějí, že existuje potenciální riziko poškození genetického materiálu savčích a lidských buněk.
- Je korozivní. Není hořlavý.
Ekotoxicita
Oxid siřičitý je nejběžnějším znečišťujícím plynem v atmosféře, zejména v městských a průmyslových oblastech..
Jeho přítomnost v atmosféře přispívá k takzvanému „kyselému dešti“, který je škodlivý pro vodní organismy, ryby, suchozemskou vegetaci a korozi pro materiály vyrobené člověkem..

SOdva je toxický pro ryby. Zelené rostliny jsou extrémně citlivé na SOdva atmosférický. Vojtěška, bavlna, ječmen a pšenice jsou poškozeny při nízké úrovni prostředí, zatímco brambory, cibule a kukuřice jsou mnohem odolnější.
Účinky požití s jídlem
I když je neškodný pro zdravé lidi, při použití v koncentracích doporučených autorizovanými zdravotnickými agenturami, SOdva může vyvolat astma u citlivých lidí, kteří ho konzumují s jídlem.
Potraviny, které jej obvykle obsahují, jsou sušené ovoce, umělé nealkoholické nápoje a alkoholické nápoje.
Reference
- NÁS. Národní lékařská knihovna. (2019). Oxid siřičitý. Obnoveno z pubchem.ncbi.nlm.nih.gov.
- Huang, Y. a kol. (2016). Endogenní oxid siřičitý: nový člen rodiny benzotransmiterů v kardiovaskulárním systému. Oxid Med Cell Longev. 2016; 2016: 8961951. Obnoveno z ncbi.nlm.nih.gov.
- Cotton, F. Albert a Wilkinson, Geoffrey. (1980). Pokročilá anorganická chemie. Čtvrté vydání. John Wiley & Sons.
- Windholz, M. a kol. (redaktoři) (1983). Index společnosti Merck. Encyclopedia of Chemicals, Drugs, and Biologicals. Desáté vydání. Merck & CO., Inc..
- Pan, X. (2011). Oxidy síry: zdroje, expozice a účinky na zdraví. Účinky oxidů síry na zdraví. In Encyclopedia of Environmental Health. Obnoveno ze sciencedirect.com.
- Tricker, R. a Tricker, S. (1999). Znečišťující látky a kontaminující látky. Oxid siřičitý. In Environmentální požadavky na elektromechanická a elektronická zařízení. Obnoveno ze sciencedirect.com.
- Bleam, W. (2017). Acidobazická chemie. Oxidy síry. In Soil and Environmental Chemistry (Druhé vydání). Obnoveno ze sciencedirect.com.
- Freedman, B.J. (1980). Oxid siřičitý v potravinách a nápojích: jeho použití jako konzervační látky a jeho účinek na astma. Br J Dis Chest. 1980; 14 (2): 128-34. Obnoveno z ncbi.nlm.nih.gov.
- Craig, K. (2018). Recenze chemie, používání pesticidů a osudu oxidu siřičitého v životním prostředí, jak se používají v Kalifornii. In Recenze znečištění životního prostředí a toxikologie. Svazek 246. Obnoveno z odkazu.springer.com.



Zatím žádné komentáře