
Vlastnosti, typy a názvosloví glykosidových vazeb
The glykosidové vazby Jsou to kovalentní vazby, které se vyskytují mezi cukry (uhlohydráty) a jinými molekulami, což mohou být jiné monosacharidy nebo jiné molekuly rozmanité povahy. Tyto vazby umožňují existenci mnoha základních složek po celý život, a to nejen při tvorbě rezervních paliv a strukturních prvků, ale také molekul nesoucích informace nezbytné pro buněčnou komunikaci..
Tvorba polysacharidů zásadně závisí na vytvoření glykosidových vazeb mezi volnými alkoholovými nebo hydroxylovými skupinami jednotlivých monosacharidových jednotek..
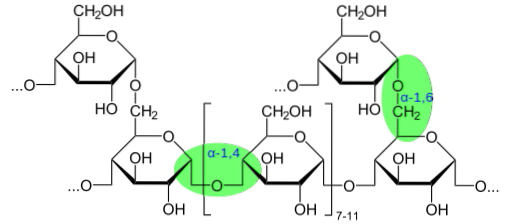
Některé složité polysacharidy však obsahují modifikované cukry, které jsou připojeny k malým molekulám nebo skupinám, jako je amino, sulfát a acetyl, prostřednictvím glukosidových vazeb a které nemusí nutně zahrnovat uvolnění molekuly vody kondenzační reakcí. Tyto modifikace jsou velmi běžné u glykanů přítomných v extracelulární matrici nebo glykokalyxu..
Glykosidové vazby se vyskytují v mnoha buněčných kontextech, včetně spojení skupiny polárních hlav některých sfingolipidů, základních složek buněčných membrán mnoha organismů a tvorby glykoproteinů a proteoglykanů..
Důležité polysacharidy, jako je celulóza, chitin, agar, glykogen a škrob, by nebyly možné bez glykosidových vazeb. Podobně je pro aktivitu mnoha proteinů nanejvýš důležitá glykosylace proteinů, ke které dochází v endoplazmatickém retikulu a v Golgiho komplexu.
Četné oligo- a polysacharidy fungují jako zásobníky glukózy, jako strukturní složky nebo jako adheziva pro připojení buněk v tkáních..
Vztah mezi glykosidovými vazbami v oligosacharidech je analogický vztahu mezi peptidovými vazbami v polypeptidech a fosfodiesterovými vazbami v polynukleotidech, s tím rozdílem, že existuje větší rozmanitost glykosidových vazeb.
Rejstřík článků
- 1 Funkce
- 1.1 Tvorba glykosidové vazby
- 1.2 Hydrolýza glykosidové vazby
- 1.3 Rozmanitost
- 2 druhy
- 2.1 O-glukosidové vazby
- 2.2 N-glukosidové vazby
- 2.3 Jiné typy glykosidových vazeb
- 3 Názvosloví
- 4 Odkazy
Vlastnosti
Glykosidové vazby jsou mnohem rozmanitější než jejich analogy v proteinech a nukleových kyselinách, protože v zásadě se jakékoli dvě molekuly cukru mohou navzájem spojovat mnoha způsoby, protože mají více skupin -OH, které se mohou podílet na tvorbě vazby.
Kromě toho izomery monosacharidů, tj. Jedna ze dvou orientací, které může mít hydroxylová skupina v cyklické struktuře vzhledem k anomernímu uhlíku, poskytují další úroveň diverzity..
Izomery mají různé trojrozměrné struktury i různé biologické aktivity. Celulóza a glykogen se skládají z opakujících se jednotek D-glukózy, ale liší se typem glykosidové vazby (α1-4 pro glykogen a β1-4 pro celulózu), a proto mají odlišné vlastnosti a funkce..
Stejně jako mají polypeptidy polaritu s N- a C- koncem a polynukleotidy mají 5 'a 3' konce, mají oligo- nebo polysacharidy polaritu definovanou redukujícími a neredukujícími konci.
Redukční konec má volné anomerní centrum, které nevytváří glykosidovou vazbu s jinou molekulou, čímž si zachovává chemickou reaktivitu aldehydu.
Glykosidová vazba je nejpružnější oblastí oligo- nebo polysacharidové skupiny, protože strukturní sedlová konformace jednotlivých monosacharidů je relativně tuhá..
Tvorba glykosidové vazby
Glykosidová vazba může spojovat dvě molekuly monosacharidů prostřednictvím anomerního uhlíku jedné a hydroxylové skupiny druhé. To znamená, že hemiacetalová skupina jednoho cukru reaguje s alkoholovou skupinou druhého za vzniku acetalu.
Obecně k tvorbě těchto vazeb dochází kondenzačními reakcemi, kdy se s každou vytvořenou vazbou uvolňuje molekula vody..
V některých reakcích však kyslík neopouští molekulu cukru jako vodu, ale jako součást difosfátové skupiny uridindifosfátového nukleotidu..
Reakce, které vedou ke vzniku glykosidových vazeb, jsou katalyzovány třídou enzymů známých jako glykosyltransferázy. Vznikají mezi kovalentně modifikovaným cukrem přidáním fosfátové skupiny nebo nukleotidu (například glukóza-6-fosfát, UDP-galaktóza), který se váže na rostoucí polymerní řetězec..
Hydrolýza glykosidové vazby
Glykosidové vazby lze snadno hydrolyzovat v mírně kyselém prostředí, ale jsou docela odolné vůči zásaditému prostředí..
Enzymatická hydrolýza glykosidových vazeb je zprostředkována enzymy známými jako glykosidázy. Mnoho savců nemá tyto enzymy pro degradaci celulózy, takže nejsou schopni extrahovat energii z tohoto polysacharidu, přestože jsou základním zdrojem vlákniny.
Například přežvýkavci, jako jsou krávy, mají ve střevech bakterie, které produkují enzymy schopné degradovat přijímanou celulózu, což jim umožňuje využívat energii konzervovanou v rostlinných tkáních..
Enzym lysozym produkovaný v slzách oka a některými bakteriálními viry je schopen ničit bakterie díky své hydrolytické aktivitě, která narušuje glykosidovou vazbu mezi N-acetylglukosaminem a N-acetylmuramovou kyselinou v buněčné stěně bakterií..
Rozmanitost
Oligosacharidy, polysacharidy nebo glykany jsou velmi rozmanité molekuly, a to díky mnoha způsobům, kterými se monosacharidy mohou vázat dohromady a vytvářet struktury vyššího řádu.
Tato rozmanitost je založena na skutečnosti, jak je uvedeno výše, že cukry mají hydroxylové skupiny, které umožňují různé vazebné oblasti, a že mezi dvěma možnými stereoizomery může dojít k vazbám, pokud jde o anomerní uhlík cukru (a nebo p)..
Mohou se tvořit glykosidové vazby mezi cukrem a jakoukoli hydroxy sloučeninou, jako jsou alkoholy nebo aminokyseliny.
Kromě toho může monosacharid tvořit dvě glykosidické vazby, takže může sloužit jako bod rozvětvení a zavádět potenciální složitost struktury glykanů nebo polysacharidů v buňkách..
Typy
Pokud jde o typy glykosidových vazeb, lze rozlišit dvě kategorie: glykosidické vazby mezi monosacharidy, které tvoří oligo- a polysacharidy, a glykosidické vazby, které se vyskytují v glykoproteinech nebo glykolipidech, což jsou proteiny nebo lipidy s částmi sacharidů.
O-glukosidové vazby
O-glykosidové vazby se vyskytují mezi monosacharidy, jsou tvořeny reakcí mezi hydroxylovou skupinou jedné molekuly cukru a anomerním uhlíkem jiné.
Disacharidy jsou jedním z nejběžnějších oligosacharidů. Polysacharidy mají více než 20 monosacharidových jednotek spojených lineárně a někdy mají více větví..
V disacharidech, jako je maltóza, laktóza a sacharóza, je nejběžnější glykosidovou vazbou O-glukosidový typ. Tyto vazby se mohou vyskytovat mezi uhlíky a -OH izomerních forem α nebo β..
Tvorba glukosidových vazeb v oligo- a polysacharidech bude záviset na stereochemické povaze cukrů, které jsou spojeny, a také na jejich počtu atomů uhlíku. Obecně platí, že u cukrů se 6 uhlíky se mezi uhlíky 1 a 4 nebo 1 a 6 vyskytují lineární vazby.
Existují dva hlavní typy O-glykosidy, které jsou v závislosti na nomenklatuře definovány jako α a β nebo 1,2-cis a 1.2-trans-glykosidy.
Zbytky 1,2-cis glykosylované, a-glykosidy pro D-glukózu, D-galaktózu, L-fukózu, D-xylózu nebo p-glykosidy pro D-manózu, L-arabinózu; stejně jako 1,2-trans (β-glykosidy pro D-glukózu, D-galaktózu a α-glykosidy pro D-manózu atd.), mají velký význam pro mnoho přírodních složek.
O-glykosylace
Jednou z nejběžnějších posttranslačních modifikací je glykosylace, která spočívá v přidání sacharidové části k rostoucímu peptidu nebo proteinu. Muciny, sekreční proteiny, mohou obsahovat velké množství oligosacharidových řetězců spojených O-glukosidovými vazbami..
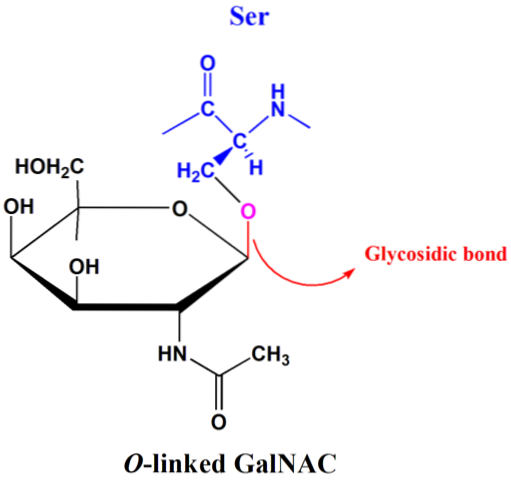
Proces O-glykosylace probíhá v Golgiho komplexu eukaryot a spočívá ve vazbě proteinů na sacharidovou část prostřednictvím glykosidové vazby mezi skupinou -OH aminokyselinového zbytku serinu nebo threoninu a anomerního uhlíku..
Bylo také pozorováno vytváření těchto vazeb mezi sacharidy a hydroxyprolinovými a hydroxylysinovými zbytky a s fenolickou skupinou tyrosinových zbytků..
N-glykosidové vazby
N-glykosidové vazby jsou nejčastější mezi glykosylovanými proteiny. N-glykosylace se vyskytuje hlavně v endoplazmatickém retikulu eukaryot, s následnými modifikacemi, které mohou nastat v komplexu Golgi.
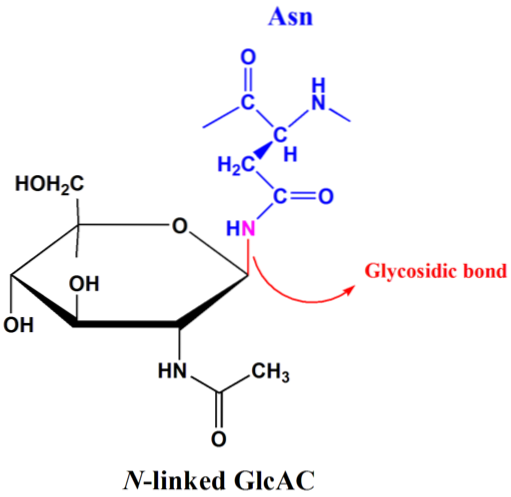
N-glykosylace závisí na přítomnosti konsensuální sekvence Asn-Xxx-Ser / Thr. Glykosidová vazba nastává mezi amidovým dusíkem postranního řetězce asparaginových zbytků a anomerním uhlíkem cukru, který se váže na peptidový řetězec..
Tvorba těchto vazeb během glykosylace závisí na enzymu známém jako oligosacaryltransferáza, který přenáší oligosacharidy z dolicholfosfátu na amidový dusík zbytků asparaginu..
Jiné typy glykosidových vazeb
S-glukosidové vazby
Vyskytují se také mezi bílkovinami a sacharidy, byly pozorovány mezi peptidy s N-koncovými cysteiny a oligosacharidy. Peptidy s tímto typem vazby byly původně izolovány z proteinů v lidské moči a erytrocytů vázaných na glukózové oligosacharidy..
C-glukosidové vazby
Byly poprvé pozorovány jako posttranslační modifikace (glykosylace) v tryptofanovém zbytku v RNáze 2 přítomné v lidské moči a v RNáze 2 erytrocytů. Manóza se váže na uhlík v poloze 2 indolového jádra aminokyseliny prostřednictvím C-glukosidové vazby.
Nomenklatura
Termín glykosid se používá k popisu jakéhokoli cukru, jehož anomerní skupina je nahrazena skupinou -OR (O-glykosidy), -SR (thioglykosidy), -SeR (selenoglykosidy), -NR (N-glykosidy nebo glukosaminy) nebo dokonce -CR (C-glukosidy).
Mohou být pojmenovány třemi různými způsoby:
(1) nahrazení terminálu „-o“ názvu odpovídající cyklické formy monosacharidu řetězcem „-ido“ a před zapsáním jiného názvu substituentu R jako jiného slova.
(2) použití výrazu „glykosyloxy“ jako předpony názvu monosacharidu.
(3) použití výrazu NEBO-glykosyl, N-glykosyl, S-glykosyl nebo C-glykosyl jako předpona názvu hydroxy sloučeniny.
Reference
- Bertozzi, C. R., a Rabuka, D. (2009). Strukturální základ rozmanitosti glykanu. In A. Varki, R. Cummings, & J. Esko (Eds.), Základy glykobiologie (2. vyd.). New York: Cold Spring Harbor Laboratory Press. Citováno z www.ncbi.nlm.nih.gov
- Biermann, C. (1988). Hydrolýza a další štěpení glykosidových vazeb v polysacharidech. Pokroky v chemii sacharidů a biochemii, 46, 251-261.
- Demchenko, A. V. (2008). Příručka chemické glykosylace: Pokroky ve stereoselektivitě a terapeutické relevanci. Wiley-VCH.
- Lodish, H., Berk, A., Kaiser, C. A., Krieger, M., Bretscher, A., Ploegh, H.,… Martin, K. (2003). Molekulární buněčná biologie (5. vydání). Freeman, W. H. & Company.
- Nelson, D. L. a Cox, M. M. (2009). Lehningerovy principy biochemie. Edice Omega (5. vydání).
- Nomenklatura sacharidů (doporučení 1996). (devatenáctset devadesát šest). Citováno z www.qmul.ac.uk
- Soderberg, T. (2010). Organická chemie s biologickým důrazem, svazek I. Fakulta chemie (Sv. 1). Minnesota: University of Minnesota Morris Digital Well. Citováno z www.digitalcommons.morris.umn.edu
- Taylor, C. M. (1998). Glykopeptidy a glykoproteiny: zaměření na glykosidové vazby. Čtyřstěn, 54, 11317-11362.



Zatím žádné komentáře