
Erytroblasty, co to jsou, erytropoéza, související patologie
The erytroblasty jsou to prekurzorové buňky erytrocytů obratlovců. Pokles koncentrace kyslíku v tkáních podpoří dělení buněk v těchto buňkách, což povede ke vzniku zralých erytrocytů. Soubor všech těchto událostí je znám jako erytropoéza.
Během erytropoézy se zvyšuje syntéza hemoglobinu. Bohatý protein v erytrocytech, který zprostředkovává dodávku kyslíku do tkání a detoxikaci oxidu uhličitého z tkání, což je buněčně toxický odpadní produkt buněčného dýchání.
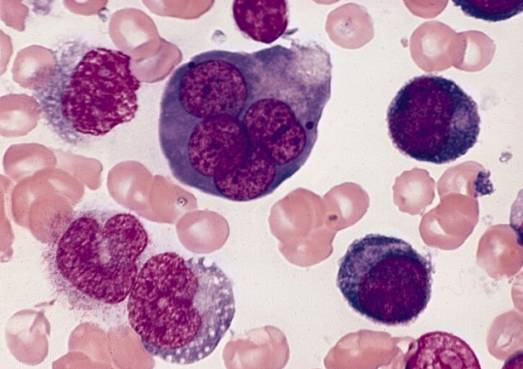
Chyby v procesu diferenciace erytroblastů vedou k souboru krevních patologií, které se společně nazývají megaloblastické anémie.
Rejstřík článků
- 1 Co jsou to erytrocyty?
- 2 Co jsou to erytroblasty?
- 3 Co je to erytropoéza?
- 4 Diferenciace erytroblastů na erytrocyty
- 5 Diferenciace buněk
- 6 Patologie spojené s chybami v diferenciaci erytroblastů
- 7 Reference
Co jsou erytrocyty?
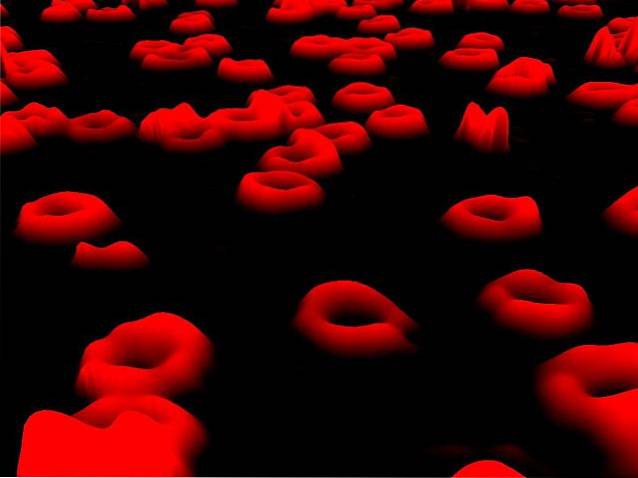
Mají charakteristickou morfologii podobnou bikonkávním diskům a jejich hlavní funkcí je provádět transport kyslíku (O2) do různých tkání těla, zároveň je detoxikuje od oxidu uhličitého (CO2) produkovaného během buněčných procesů. dýchání..
Tato výměna CO2 za O2 je možná, protože v těchto buňkách se nachází velké množství charakteristického červeného proteinu zvaného hemoglobin, schopného interakce s oběma chemickými látkami prostřednictvím hemové skupiny přítomné v jejich struktuře..
Zvláštností těchto buněk u savců s ohledem na zbytek obratlovců je nedostatek jádra a cytoplazmatických organel. Během počátečních fází produkce v raných fázích embryonálního vývoje však bylo pozorováno, že buněčné prekurzory, ze kterých pocházejí, představují přechodné jádro.
To není překvapivé vzhledem k tomu, že raná stadia vývoje embryí jsou obvykle podobná u všech obratlovců, přičemž se liší pouze stádia, která narušují větší diferenciaci..
Co jsou to erytroblasty?
Erytroblasty jsou buňky, které způsobí vznik zralých erytrocytů poté, co podstoupí po sobě jdoucí události buněčné diferenciace..
Tyto prekurzorové buňky pocházejí ze společného myeloidního předka v kostní dřeni obratlovců jako nukleované buňky, opatřené jádry a buněčnými organelami..
Změny v obsahu jeho cytoplazmy a v přeskupení cytoskeletu vyvrcholí tvorbou erytrocytů připravených k oběhu. Tyto změny reagují na podněty prostředí, které svědčí o poklesu kyslíku v tkáních, a tedy o poptávce po produkci erytrocytů..
Co je erytropoéza?
Erytropoéza je termín používaný k definování procesu, kterým probíhá produkce a vývoj červených krvinek, nezbytný k udržení přívodu kyslíku do různých orgánů a tkání..
Tento proces je jemně regulován působením erytropoetinu (EPO), hormonu syntézy ledvin, který je zase modulován koncentracemi kyslíku dostupnými v tkáních..
Nízké koncentrace kyslíku v tkáních indukují syntézu EPO hypoxií indukovatelným transkripčním faktorem (HIF-1), který stimuluje proliferaci erytrocytů vazbou na receptory EpoR přítomné na prekurzorových buňkách erytrocytů.
U savců se erytropoéza provádí ve dvou fázích, které se nazývají primitivní erytropoéza a definitivní erytropoéza..
První se vyskytuje v žloutkovém vaku během embryonálního vývoje, což vede k velkým nukleárním erytroblastům, zatímco druhý se vyskytuje v játrech plodu a pokračuje v kostní dřeni po druhém měsíci těhotenství a vytváří menší enukleované erytrocyty..
Další proteiny, jako je antipoptotický cytokin Bcl-X, jehož transkripce je regulována transkripčním faktorem GATA-1, také pozitivně ovlivňují proces erytropoézy. Kromě toho je také nezbytný přísun železa, vitaminu B12 a kyseliny listové.
Diferenciace erytroblastů na erytrocyty
V procesu definitivní erytropoézy se erytrocyty tvoří v kostní dřeni z nediferencovaných progenitorových buněk nebo běžných myeloidních progenitorů schopných vytvářet další buňky, jako jsou granulocyty, monocyty a krevní destičky..
Tato buňka musí přijímat příslušné extracelulární signály, aby narušila její diferenciaci směrem k erytroidní linii..
Jakmile je tento závazek získán, začíná sled diferenciačních událostí, které začínají tvorbou pronormoblastu, známého také jako proerythroblast. Velká prekurzorová buňka erytroblastu s jádrem.
Následně proerythroblast zažije progresivní pokles objemu jaderných buněk doprovázený zvýšením syntézy hemoglobinu. Všechny tyto změny se vyskytují pomalu, jak tato buňka prochází různými buněčnými stádii: bazofilní erytroblast nebo normoblast, polychromatický erytroblast a ortochromatický erytroblast.
Proces je zakončen celkovou ztrátou jádra i organel přítomných v ortochromatickém erytroblastu, které vytvářejí zralý erytrocyt.
Aby toho konečně dosáhl, musí ten projít stádiem retikulocytů, enukleovanou buňkou, která ve své cytoplazmě stále obsahuje organely a ribozomy. Úplné odstranění jádra a organel se provádí exocytózou.
Zralé erytrocyty opouštějí kostní dřeň do krevního řečiště, kde zůstávají v oběhu přibližně 120 dní, než je pohltí makrofágy. Erytropoéza je tedy proces, který probíhá nepřetržitě po celý život organismu..
Buněčná diferenciace
Jak erytoblasty postupují směrem k úplné diferenciaci na zralý erytrocyt, procházejí mnohonásobnými změnami v cytoskeletu i v expresi proteinů buněčné adheze..
Aktinové mikrofilamenta depolymerizují a je sestaven nový cytoskeleton na bázi spektrinu. Spektrin je protein periferní membrány umístěný na cytoplazmatické ploše, který interaguje s ankyrinem, proteinem, který zprostředkovává vazbu cytoskeletu s transmembránovým proteinem Band 3.
Tyto změny v cytoskeletu a v expresi Epo receptorů, stejně jako mechanismy, které je modulují, jsou zásadní pro zrání erytroidů..
To je způsobeno skutečností, že zprostředkovávají vytváření interakcí mezi erytroblasty a buňkami přítomnými v mikroprostředí kostní dřeně, což usnadňuje přenos signálů nezbytných k zahájení a ukončení diferenciace..
Jakmile je diferenciace dokončena, nastanou nové změny, které upřednostňují ztrátu adheze buněk k dřeni a jejich uvolnění do krevního řečiště, kde budou plnit svou funkci..
Patologie spojené s chybami v diferenciaci erytroblastů
Chyby během diferenciace erytroblastů v kostní dřeni vedou ke vzniku krevních patologií, jako jsou megaloblastické anémie. Ty pocházejí z nedostatků v zásobě vitaminu B12 a folátů nezbytných k podpoře diferenciace erytroblastů..
Termín megaloblastický označuje velkou velikost, které dosahují erytroblasty a dokonce i erytrocyty jako produkt neúčinné erytropoézy charakterizované defektní syntézou DNA.
Reference
- Ferreira R, Ohneda K, Yamamoto M, funkce Philipsen S. GATA1, paradigma transkripčních faktorů při hematopoéze. Molekulární a buněčná biologie. 2005; 25 (4): 1215-1227.
- Kingsley PD, Malik J, Fantauzzo KA, Palis J. Primární erytroblasty odvozené ze žloutkového vakulátu během embryogeneze savců. Krev (2004); 104 (1): 19-25.
- Konstantinidis DG, Pushkaran S, Johnson JF, Cancelas JA, Manganaris S, Harris CE, Williams AE, Zheng Y, Kalfa TA. Signalizace a cytoskeletální požadavky v erytroblastové enukleaci. Krev. (2012); 119 (25): 6118-6127.
- Migliaccio AR. Enukleace erytroblastů. Haematologica. 2010; 95: 1985-1988.
- Shivani Soni, Shashi Bala, Babette Gwynn, Kenneth E, Luanne L, Manjit Hanspal. Absence erytroblastového makrofágového proteinu (Emp) vede k selhání jaderného protlačování erytroblastů. Žurnál biologické chemie. 2006; 281 (29): 20181-20189.
- Skutelsky E, Danon D. Elektronová mikroskopická studie jaderné eliminace z pozdního erytroblastu. J Cell Biol. 1967; 33 (3): 625-635.
- Tordjman R, Delaire S, Plouet J, Ting S, Gaulard P, Fichelson S, Romeo P, Lemarchandel V. Erythroblasty jsou zdrojem angiogenních faktorů. Blood (2001); 97 (7): 1968-1974.



Zatím žádné komentáře