
Vlastnosti mikroskopického měřítka, počítání částic, příklady
The mikroskopické měřítko Je to ten, který se používá k měření velikostí a délek, které nelze vidět pouhým okem a které jsou kratší než jeden milimetr. Od nejvyšší po nejnižší jsou mikroskopické váhy v metrickém systému:
- Milimetr (1 mm), což je jedna desetina centimetru nebo tisícina metru. V tomto měřítku máme jednu z největších buněk v těle, kterou je vajíčko, jehož velikost je 1,5 mm.
- Desetina milimetru (0,1 mm). Toto je měřítko tloušťky nebo průměru lidského vlasu.
- Mikrometr nebo mikron (1 μm = 0,001 mm). V tomto měřítku jsou rostlinné a živočišné buňky a bakterie.
Rostlinné buňky jsou řádově 100 μm. Živočišné buňky jsou desetkrát menší, řádově 10 μm; zatímco bakterie jsou 10krát menší než zvířecí buňky a jsou řádově 1 μm.
Rejstřík článků
- 1 nanoměřítko
- 2 Nástroje pro mikroskopické pozorování
- 3 Mikroskopické vlastnosti
- 3.1-Matter je obrovská prázdnota
- 4 Jak počítat částice v mikroskopickém měřítku?
- 4.1 - Příklad 1
- 4,2 - Příklad 2
- 5 Reference
Nano měřítko
Existují měření dokonce menší než mikroskopické měřítko, ale nejsou běžně používána, s výjimkou některých speciálních kontextů. Zde jsou některá z nejdůležitějších nanometrických měření:
- Nanometr (1 ηm = 0,001 μm = 0,000001 mm) je miliontina milimetru. V tomto měřítku jsou některé viry a molekuly. Viry jsou řádově 10ηm a molekuly řádově 1ηm.
- Angstrom (1Å = 0,1ηm = 0,0001μm = 10-7mm). Toto měření tvoří měřítko nebo velikost atomu.
- Fantomometr (1 fm = 0,00001 A = 0,000001ηm = 10-12mm). Toto je měřítko atomových jader, která jsou mezi 10 000 a 100 000krát menšími než atom. Navzdory své malé velikosti však jádro koncentruje 99,99% atomové hmoty.
- Atomové jádro má menší měřítka, protože jsou tvořena částicemi, jako jsou protony a neutrony. Ale je toho víc: tyto částice jsou zase tvořeny základnějšími částicemi, jako jsou kvarky..
Nástroje pro mikroskopické pozorování
Pokud jsou objekty mezi milimetrovou a mikrometrickou stupnicí (1 mm - 0,001 mm), lze je pozorovat optickým mikroskopem.
Pokud se však objekty nebo struktury nacházejí mezi nanometry a angstromy, budou zapotřebí elektronové mikroskopy nebo nanoskop..
V elektronové mikroskopii se místo světla používají vysokoenergetické elektrony, které mají mnohem kratší vlnovou délku než světlo. Nevýhodou elektronového mikroskopu je, že do něj není možné umístit živé vzorky, protože pracuje ve vakuu..
Nanoskop místo toho používá laserové světlo a oproti elektronové mikroskopii má tu výhodu, že je možné prohlížet a zaznamenávat struktury a molekuly v živé buňce..
Nanotechnologie je technologie, s jejíž pomocí se vyrábějí obvody, struktury, součásti a dokonce i motory v měřítcích, které přecházejí z nanometru do atomového měřítka.
Mikroskopické vlastnosti
Ve fyzice je v první aproximaci studováno chování hmoty a systémů z makroskopického hlediska. Z tohoto paradigmatu je hmota nekonečně dělitelným kontinuem; a tento úhel pohledu je platný a vhodný pro mnoho situací v každodenním životě.
Některé jevy v makroskopickém světě však lze vysvětlit, pouze pokud jsou brány v úvahu mikroskopické vlastnosti hmoty..
Z mikroskopického hlediska je brána v úvahu molekulární a atomová struktura hmoty. Na rozdíl od makroskopického přístupu existuje v tomto měřítku zrnitá struktura s mezerami a mezerami mezi molekulami, atomy a dokonce i uvnitř nich..
Další charakteristikou z mikroskopického hlediska ve fyzice je, že část hmoty, bez ohledu na to, jak malá, je složena z enormního počtu částic oddělených od sebe navzájem a v nepřetržitém pohybu..
-Hmota je obrovská prázdnota
V malém kousku hmoty je vzdálenost mezi atomy enormní ve srovnání s jejich velikostí, ale zase jsou atomy enormní ve srovnání s jejich vlastními jádry, kde je koncentrováno 99,99% hmoty..
To znamená, že kousek hmoty v mikroskopickém měřítku je obrovské vakuum s koncentracemi atomů a jader, které zabírají malý zlomek celkového objemu. V tomto smyslu je mikroskopické měřítko podobné astronomickému měřítku..
Od makroskopických objektů až po objev atomu
První chemici, kteří byli alchymisty, si uvědomili, že materiály mohou být dvou typů: čistý nebo složený. Tak došlo k myšlence chemických prvků.
Prvními objevenými chemickými prvky bylo sedm antických kovů: stříbro, zlato, železo, olovo, cín, měď a rtuť. Postupem času bylo objeveno více do té míry, že byly nalezeny látky, které se nedaly rozložit na jiné.
Poté byly prvky klasifikovány podle jejich vlastností a charakteristik v kovech a nekovech. Všichni, kteří měli podobné vlastnosti a chemickou afinitu, byli seskupeni do stejného sloupce, a tak vznikla periodická tabulka prvků..
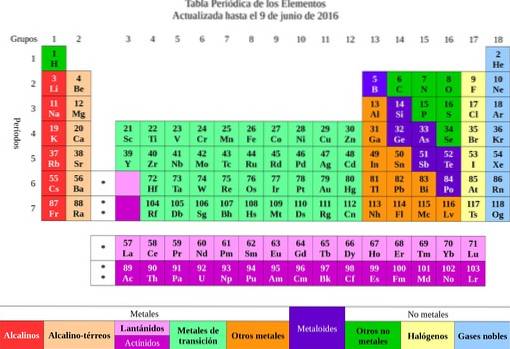
Z prvků byla předána myšlenka atomů, slovo, které znamená nedělitelné. Krátce nato si vědci uvědomili, že atomy skutečně mají strukturu. Atomy měly navíc dva typy elektrického náboje (kladný a záporný).
Subatomární částice
V Rutherfordových experimentech, ve kterých bombardoval atomy tenké zlaté desky částicemi alfa, byla odhalena struktura atomu: malé pozitivní jádro obklopené elektrony.
Atomy byly nadále bombardovány stále více energetickými částicemi a stále se to děje, aby se v menším a menším měřítku rozluštila tajemství a vlastnosti mikroskopického světa..
Tímto způsobem bylo dosaženo standardního modelu, ve kterém je stanoveno, že skutečné elementární částice jsou ty, z nichž jsou složeny atomy. Atomy zase dávají vzniknout prvkům, ty sloučeninám a všem známým interakcím (kromě gravitace). Celkem existuje 12 částic.
Tyto základní částice mají také svoji periodickou tabulku. Existují dvě skupiny: fermionické částice s ½ spinem a bosonické částice. Za interakce jsou odpovědné bosony. Fermionů je 12 a jsou to ty, které dávají vznik protonům, neutronům a atomům.
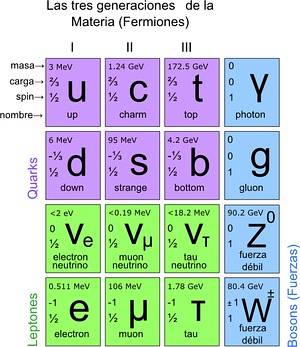
Jak počítat částice v mikroskopickém měřítku?
V průběhu času chemici objevovali relativní hmotnosti prvků z přesných měření v chemických reakcích. Lze tedy například určit, že uhlík je 12krát těžší než vodík..
Vodík byl také určen jako nejlehčí prvek, takže tomuto prvku byla přiřazena relativní hmotnost 1.
Na druhou stranu chemici požadovali znát počet částic zapojených do reakce, aby žádné činidlo neskončilo nebo nechybělo. Například molekula vody vyžaduje dva atomy vodíku a jeden atom kyslíku..
Z těchto předchůdců se zrodil koncept krtka. Krtek jakékoli látky je stálý počet částic ekvivalentní její molekulové nebo atomové hmotnosti v gramech. Bylo tedy stanoveno, že 12 gramů uhlíku má stejný počet částic jako 1 gram vodíku. Toto číslo je známé jako Avogadro číslo: 6,02 x 10 ^ 23 částic.
-Příklad 1
Vypočítejte, kolik atomů zlata je v 1 gramu zlata.
Řešení
Je známo, že zlato má atomovou hmotnost 197. Tyto údaje lze najít v periodické tabulce a naznačují, že atom zlata je 197krát těžší než jeden z vodíku a 197/12 = 16 416krát těžší než uhlík..
Krtek zlata má 6,02 × 10 ^ 23 atomů a má atomovou hmotnost vyjádřenou v gramech, tj. 197 gramů.
V jednom gramu zlata je 1/197 molů zlata, tj. 6,02 × 10 ^ 23 atomů / 197 = 3,06 x10 ^ 23 atomů zlata.
-Příklad 2
Určete počet molekul uhličitanu vápenatého (CaCO3), které jsou ve 150 gramech této látky. Řekněte také, kolik atomů vápníku, kolik uhlíku a kolik kyslíku obsahuje tato sloučenina.
Řešení
První věcí je určit molekulovou hmotnost uhličitanu vápenatého. Periodická tabulka ukazuje, že vápník má molekulovou hmotnost 40 g / mol, uhlík 12 g / mol a kyslík 16 g / mol..
Pak molekulová hmotnost (CaCO3) bude :
40 g / mol + 12 g / mol + 3 x 16 g / mol = 100 g / mol
Každých 100 gramů uhličitanu vápenatého je 1 mol. Takže ve 150 gramech odpovídají 1,5 molu.
Každý mol uhličitanu má 6,02 x 10 ^ 23 molekul uhličitanu, takže v 1,5 molu uhličitanu je 9,03 x 10 ^ 23 molekul.
Stručně řečeno, ve 150 gramech uhličitanu vápenatého jsou:
- 9,03 x 10 ^ 23 molekul uhličitanu vápenatého.
- Atomy vápníku: 9,03 x 10 ^ 23 .
- Také 9,03 x 10 ^ 23 atomů uhlíku
- A konečně, 3 x 9,03 x 10 ^ 23 atomů kyslíku = 27,09 x 10 ^ 23 atomů kyslíku.
Reference
- Aplikovaná biologie. Jaká jsou mikroskopická měření? Obnoveno z: youtube.com
- Chemická výchova. Makroskopická, submikroskopická a symbolická znázornění hmoty. Obnoveno z: scielo.org.mx.
- García A. Interaktivní kurz fyziky. Makro stavy, mikrostavy. Teplota, entropie. Obnoveno z: sc.ehu.es
- Mikroskopická struktura hmoty. Obnoveno z: alipso.com
- Wikipedia. Mikroskopická úroveň. Obnoveno z: wikipedia.com

Zatím žádné komentáře