
Voltametrie, z čeho se skládá, typy a aplikace
The voltametrie Jedná se o elektroanalytickou techniku, která určuje informace o chemické látce nebo analytu z elektrických proudů generovaných změnou aplikovaného potenciálu. To znamená, že aplikovaný potenciál E (V) a čas (t) jsou nezávislé proměnné; zatímco aktuální (A), závislá proměnná.
Chemické látky musí být obvykle elektroaktivní. Co to znamená? To znamená, že musí ztratit (oxidovat) nebo získat (snížit) elektrony. Aby mohla reakce začít, musí pracovní elektroda dodávat potřebný potenciál teoreticky určený Nernstovou rovnicí.
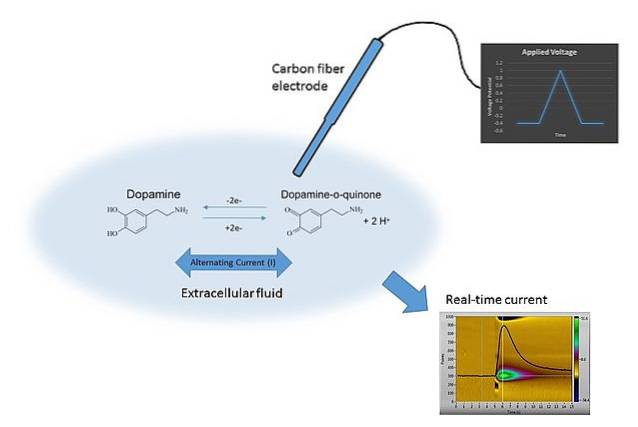
Příklad voltametrie lze vidět na obrázku výše. Elektroda v obraze je vyrobena z uhlíkových vláken, která jsou ponořena do rozpouštěcího média. Dopamin neoxiduje a tvoří dvě karbonylové skupiny C = O (pravá strana chemické rovnice), pokud není použit správný potenciál.
Toho je dosaženo skenováním E s různými hodnotami, omezenými mnoha faktory, jako je roztok, přítomné ionty, stejná elektroda a dopamin..
Změnou E v čase se získají dva grafy: první E v t (modrý trojúhelník) a druhý odpověď C vs t (žlutá). Jeho formy jsou charakteristické pro stanovení dopaminu za podmínek experimentu..
Rejstřík článků
- 1 Co je to voltametrie??
- 1,1 voltametrická vlna
- 1.2 Přístrojové vybavení
- 2 druhy
- 2.1 Pulzní voltametrie
- 2.2 Redisoluční voltametrie
- 3 Aplikace
- 4 Odkazy
Co je voltametrie?
Voltametrii vyvinul díky vynálezu techniky polarografie nositel Nobelovy ceny za chemii z roku 1922 Jaroslav Heyrovsky. V něm se elektroda kapky rtuti (EGM) neustále obnovuje a polarizuje.
Analytické nedostatky této metody byly v té době vyřešeny použitím a návrhem dalších mikroelektrod. Ty se enormně liší materiálem, od uhlíku, ušlechtilých kovů, diamantů a polymerů, až po jejich design, disky, válce, plechy; a také způsobem, jakým interagují s řešením: stacionární nebo rotující.
Všechny tyto podrobnosti jsou zamýšleny pro upřednostnění polarizace elektrody, která způsobuje úbytek registrovaného proudu známého jako mezní proud (i1). To je úměrné koncentraci analytu a poloviční účinnosti E (E1/2) dosáhnout poloviny uvedeného proudu (tj1/2) je charakteristický pro tento druh.
Poté určení hodnot E1/2 na křivce, kde proud získaný s variací E, volal voltamperogram, lze identifikovat přítomnost analytu. To znamená, že každý analyt bude mít za podmínek experimentu svou vlastní hodnotu E.1/2.
Voltametrická vlna
Ve voltametrii pracujete s mnoha grafy. První z nich je křivka E vs t, která umožňuje sledování rozdílů aplikovaného potenciálu v závislosti na čase.
Současně však elektrický obvod zaznamenává hodnoty C produkované analytem ztrátou nebo získáváním elektronů v blízkosti elektrody..
Protože je elektroda polarizovaná, může z ní do roztoku difundovat méně analytu. Například pokud je elektroda kladně nabitá, druh X- bude přitahován k tomu a půjde k němu pouhou elektrostatickou přitažlivostí.
Ale X- Nejste sami: ve vašem prostředí jsou přítomny další ionty. Některé kationty M+ mohou se dostat elektrodě do cesty uzavřením do „shluků“ kladných nábojů; a podobně, N anionty- se mohou zachytit kolem elektrody a zabránit X- Dostal jsem se k němu.
Součet těchto fyzikálních jevů způsobí ztrátu proudu, což lze pozorovat na křivce C vs E a jeho tvaru podobném tvaru S, který se nazývá sigmoidní tvar. Tato křivka je známá jako voltametrická vlna..
Instrumentace
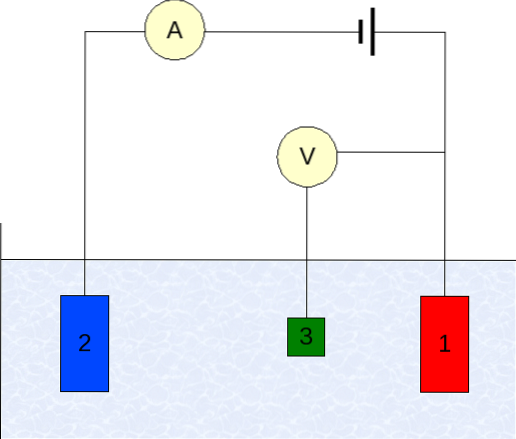
Přístrojové vybavení voltametrie se liší podle analytu, rozpouštědla, typu elektrody a aplikace. Převážná většina z nich je však založena na systému složeném ze tří elektrod: jedné pro pracovní (1), pomocné (2) a referenční (3)..
Hlavní použitou referenční elektrodou je kalomelová elektroda (ECS). To společně s pracovní elektrodou umožňuje stanovit rozdíl potenciálů ΔE, protože potenciál referenční elektrody zůstává během měření konstantní..
Na druhé straně pomocná elektroda má na starosti řízení náboje, který prochází do pracovní elektrody, aby se udržovala v přijatelných hodnotách E. Nezávislá proměnná, rozdíl aplikovaného potenciálu, je proměnná získaná sečtením potenciálů pracovní a referenční elektrody..
Typy

Obrázek výše ukazuje graf E vs t, nazývaný také potenciální vlna pro voltametrii lineárního tažení..
Je vidět, že jak čas plyne, potenciál se zvyšuje. Toto tažení zase generuje křivku odezvy nebo voltampérogram C vs E, jejichž tvar bude sigmoidní. Přijde bod, kdy bez ohledu na to, jak moc se E zvýší, nedojde k žádnému zvýšení proudu.
Z tohoto grafu lze odvodit další typy voltametrie. Jak? Úprava potenciální vlny E vs t prostřednictvím náhlých potenciálních pulzů podle určitých vzorců. Každý vzor je spojen s typem voltametrie a zahrnuje svou vlastní teorii a experimentální podmínky..
Pulzní voltametrie
V tomto typu voltametrie jsou směsi dvou nebo více analytů, jejichž hodnoty E lze analyzovat1/2 jsou si velmi blízcí. Analytik s E.1/2 0,04 V lze identifikovat ve společnosti jiného s E1/2 0,05V. V případě lineární zatáčkové voltametrie musí být rozdíl větší než 0,2 V.
Proto existují vyšší citlivost a nižší detekční limity; tj. analyty lze stanovit při velmi nízkých koncentracích.
Vlny potenciálů mohou mít vzory podobné schodům, šikmým schodům a trojúhelníkům. Ten odpovídá cyklické voltametrii (CV pro jeho zkratku v angličtině, první obrázek).
V CV se potenciál E aplikuje v jednom směru, kladném nebo záporném, a poté se při určité hodnotě E v čase t použije stejný potenciál znovu, ale v opačném směru. Při studiu generovaných voltamperogramů maxima odhalují přítomnost prostředníků v chemické reakci.
Redisoluční voltametrie
Může to být anodického nebo katodického typu. Skládá se z elektrodepozice analytu na rtuťové elektrodě. Pokud je analytem kovový iont (například Cddva+), vytvoří se amalgám; a pokud je to anion, (jako MoO4dva-) nerozpustná rtuťová sůl.
Poté se aplikují pulzy potenciálů ke stanovení koncentrace a identity elektrolyticky vyloučených druhů. Amalgám je tedy znovu rozpuštěn, jako soli rtuti.
Aplikace
-K určení koncentrace rozpuštěných kovů v tekutině se používá voltametrie anodické redisoluce.
-Umožňuje studium kinetiky redoxních nebo adsorpčních procesů, zvláště když jsou elektrody upraveny tak, aby detekovaly konkrétní analyt.
-Jeho teoretický základ byl použit pro výrobu biosenzorů. S nimi lze určit přítomnost a koncentraci biologických molekul, bílkovin, tuků, cukrů atd..
-Nakonec detekuje účast zprostředkovatelů v reakčních mechanismech.
Reference
- González M. (22. listopadu 2010). Voltametrie. Obnoveno z: quimica.laguia2000.com
- Gómez-Biedma, S., Soria, E., & Vivó, M… (2002). Elektrochemická analýza. Journal of Biological Diagnosis, 51 (1), 18-27. Obnoveno z scielo.isciii.es
- Chemie a věda. (18. července 2011). Voltametrie. Obnoveno z: laquimicaylaciencia.blogspot.com
- Quiroga A. (16. února 2017). Cyklická voltametrie. Obnoveno z: chem.libretexts.org
- Samuel P. Kounaves. (s.f.). Voltametrické techniky. [PDF]. Tufts University. Obnoveno z: brown.edu
- Den R. & Underwood A. Kvantitativní analytická chemie (páté vydání). PEARSON Prentice Hall.


Zatím žádné komentáře