
Fáze, funkce a inhibitory oxidační fosforylace
The oxidační fosforylace je proces, při kterém jsou molekuly ATP syntetizovány z ADP a Pi (anorganický fosfát). Tento mechanismus provádějí bakterie a eukaryotické buňky. V eukaryotických buňkách probíhá fosforylace v mitochondriální matrici nefotosyntetických buněk.
Produkce ATP je řízena přenosem elektronů z koenzymů NADH nebo FADHdva do O.dva. Tento proces představuje nejvyšší produkci energie v buňce a je odvozen z rozkladu sacharidů a tuků..
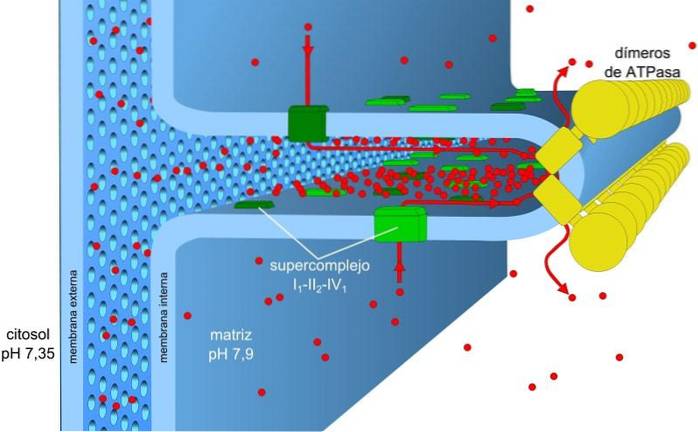
Energie uložená v náboji a gradienty pH, známé také jako hybná síla protonu, umožňují tento proces uskutečnit. Protonový gradient, který je generován, způsobuje, že vnější část membrány má kladný náboj v důsledku koncentrace protonů (H+) a mitochondriální matice je záporná.
Rejstřík článků
- 1 Kde dochází k oxidační fosforylaci?
- 1.1 Elektrárna s články
- 2 fáze
- 2.1 Elektronový dopravní řetězec
- 2.2 Succinate CoQ reduktáza
- 2.3 Spojka nebo energetická transdukce
- 2.4 Chemosmotická vazba
- 2.5 Syntéza ATP
- 3 Produkty
- 4 funkce
- 5 Řízení oxidační fosforylace
- 5.1 Koordinovaná kontrola produkce ATP
- 5.2 Kontrola akceptorem
- 5.3 Oddělovací prostředky
- 5.4 Inhibitory
- 6 Reference
Kde dochází k oxidační fosforylaci?
Procesy přenosu elektronů a oxidační fosforylace jsou spojeny s membránou. U prokaryot se tyto mechanismy provádějí přes plazmatickou membránu. V eukaryotických buňkách se asociují s mitochondriální membránou.
Počet mitochondrií nalezených v buňkách se liší v závislosti na typu buňky. Například u savců chybí erytrocyty tyto organely, zatímco jiné typy buněk, jako jsou svalové buňky, jich mohou mít až miliony..
Mitochondriální membrána se skládá z jednoduché vnější membrány, poněkud složitější vnitřní membrány a mezi nimi mezimembránový prostor, kde se nachází mnoho enzymů závislých na ATP.
Vnější membrána obsahuje protein nazývaný porin, který tvoří kanály pro jednoduchou difúzi malých molekul. Tato membrána je zodpovědná za udržování struktury a tvaru mitochondrií.
Vnitřní membrána má vyšší hustotu a je bohatá na bílkoviny. Je také nepropustný pro molekuly a ionty, takže k jeho překročení potřebují mezimembránové proteiny, aby je transportovaly..
Uvnitř matrice se táhnou záhyby vnitřní membrány, které vytvářejí hřebeny, které jí umožňují mít velkou plochu v malém objemu.
Buňková elektrárna
Mitochondrie je považována za centrálního producenta buněčné energie. Obsahuje enzymy zapojené do procesů cyklu kyseliny citronové, oxidaci mastných kyselin a redoxní enzymy a proteiny pro transport elektronů a fosforylaci ADP.
Za protonovou hybnou sílu je odpovědný gradient koncentrace protonu (gradient pH) a gradient náboje nebo elektrický potenciál ve vnitřní membráně mitochondrií. Nízká propustnost vnitřní membrány pro ionty (jiné než H+) umožňuje mitochondriím mít stabilní gradient napětí.
Elektronický transport, čerpání protonů a získávání ATP probíhají současně v mitochondriích, a to díky protonové hybné síle. Gradient pH udržuje kyselé podmínky v intermembráně a mitochondriální matrici za alkalických podmínek.
Za každé dva elektrony přenesené do Odva asi 10 protonů je čerpáno přes membránu a vytváří elektrochemický gradient. Energie uvolněná v tomto procesu se vyrábí postupně průchodem elektronů transportním řetězcem.
Fáze
Energie uvolněná během oxidačně-redukčních reakcí NADH a FADHdva je značně vysoká (kolem 53 kcal / mol pro každý pár elektronů), takže pro použití při výrobě molekul ATP musí být vyrobena postupně s průchodem elektronů transportéry.
Ty jsou uspořádány do čtyř komplexů umístěných na vnitřní mitochondriální membráně. Vazba těchto reakcí na syntézu ATP se provádí v pátém komplexu.
Elektronový dopravní řetězec
NADH přenáší dvojici elektronů, které vstupují do komplexu I elektronového transportního řetězce. Elektrony se přenášejí na flavin mononukleotid a poté na transportér železo-síra na ubichinon (koenzym Q). Tento proces uvolňuje velké množství energie (16,6 kcal / mol).
Ubichinon transportuje elektrony přes membránu do komplexu III. V tomto komplexu procházejí elektrony cytochromy b a c1 díky transportéru železa a síry.
Elektrony procházejí z komplexu III do komplexu IV (cytochrom c oxidáza) a jeden po druhém se přenášejí v cytochromu c (protein periferní membrány). V komplexu IV procházejí elektrony dvojicí iontů mědi (Cunadva+), následovaný cytochromem cna, pak k dalšímu páru iontů mědi (Cubdva+) a z toho na cytochrom a3.
Nakonec jsou elektrony přeneseny do Odva který je posledním akceptorem a tvoří molekulu vody (HdvaO) pro každou dvojici přijatých elektronů. Přechod elektronů z komplexu IV na Odva Generuje také velké množství volné energie (25,8 kcal / mol).
Succinate CoQ reduktáza
Komplex II (sukcinát CoQ reduktáza) přijímá pár elektronů z cyklu kyseliny citronové oxidací molekuly sukcinátu na fumarát. Tyto elektrony jsou přeneseny do FAD a poté procházejí skupinou železo-síra do ubichinonu. Z tohoto koenzymu přecházejí do komplexu III a sledují dříve popsanou cestu.
Energie uvolněná při reakci přenosu elektronů na FAD nestačí k protonům protékající membránou, takže v tomto kroku řetězce nevzniká žádná protonová hybná síla, a proto FADH poskytuje méně H+ že NADH.
Vazba nebo přenos energie
Energie generovaná v procesu elektronového transportu popsaného výše musí být schopná být použita k výrobě ATP, reakce katalyzované enzymem ATP syntáza nebo komplex V. Zachování této energie je známé jako energetická vazba a mechanismus byl obtížné charakterizovat.
Bylo popsáno několik hypotéz popisujících tuto energetickou transdukci. Nejlépe přijímanou hypotézou je chemiosmotická vazba, popsaná níže..
Chemosmotická vazba
Tento mechanismus navrhuje, aby energie použitá pro syntézu ATP pocházela z protonového gradientu v buněčných membránách. Tento proces zasahuje do mitochondrií, chloroplastů a bakterií a je spojen s transportem elektronů.
Komplexy I a IV transportu elektronů fungují jako protonové pumpy. Ty procházejí konformačními změnami, které jim umožňují pumpovat protony do mezimembránového prostoru. V komplexu IV jsou pro každý pár elektronů dva protony odčerpány z membrány a další dva zůstávají v matrici a tvoří HdvaNEBO.
Ubichinon v komplexu III přijímá protony z komplexů I a II a uvolňuje je ven z membrány. Komplexy I a III umožňují průchod čtyř protonů pro každou dvojici transportovaných elektronů.
Mitochondriální matice má nízkou koncentraci protonů a negativní elektrický potenciál, zatímco mezimembránový prostor představuje inverzní podmínky. Tok protonů touto membránou představuje elektrochemický gradient, který uchovává energii potřebnou (± 5 kcal / mol na proton) pro syntézu ATP..
ATP syntéza
Enzym ATP syntetáza je pátým komplexem zapojeným do oxidační fosforylace. Je zodpovědný za využití energie elektrochemického gradientu za vzniku ATP.
Tento transmembránový protein se skládá ze dvou složek: F0 a F1. Složka F0 umožňuje návrat protonů do mitochondriální matice fungující jako kanál a F1 katalyzuje syntézu ATP pomocí ADP a Pi, pomocí energie uvedeného návratu.
Proces syntézy ATP vyžaduje strukturální změnu F1 a montáž komponentů F0 a F1. Translokace protonů přes F0 způsobuje konformační změny ve třech podjednotkách F1, což mu umožňuje působit jako motor otáčení a řídí tvorbu ATP.
Podjednotka, která je zodpovědná za vazbu ADP s Pi přechází ze slabého stavu (L) do aktivního stavu (T). Když se vytvoří ATP, druhá podjednotka přejde do otevřeného stavu (O), který umožňuje uvolnění této molekuly. Po vydání ATP přejde tato podjednotka z otevřeného stavu do neaktivního stavu (L).
ADP a P molekulyi vázat na podjednotku, která prošla ze stavu O do stavu L..
produkty
Elektronový transportní řetězec a fosforylace produkují molekuly ATP. Oxidace NADH produkuje asi 52,12 kcal / mol (218 kJ / mol) volné energie.
Celková reakce na oxidaci NADH je:
NADH + 1⁄2 O.dva +H+ ↔ HdvaO + NAD+
Přenos elektronů z NADH a FADHdva dochází prostřednictvím různých komplexů, což umožňuje, aby se změna volné energie ΔG ° dělila na menší energetické „pakety“, které jsou spojeny se syntézou ATP.
Oxidace jedné molekuly NADH generuje syntézu tří molekul ATP. Zatímco oxidace molekuly FADHdva páry k syntéze dvou ATP.
Tyto koenzymy pocházejí z procesů glykolýzy a cyklu kyseliny citrónové. U každé degradované molekuly glukózy nakonec produkují 36 nebo 38 molekul ATP, v závislosti na umístění buněk. 36 ATP se produkuje v mozku a kosterním svalu, zatímco 38 ATP se produkuje ve svalové tkáni..
Funkce
Všechny organismy, jednobuněčné i mnohobuněčné, potřebují ve svých buňkách minimální energii k provádění procesů v nich a zase k udržení životně důležitých funkcí v celém organismu..
Metabolické procesy vyžadují energii. Většina využitelné energie se získává štěpením sacharidů a tuků. Tato energie je odvozena z procesu oxidační fosforylace.
Řízení oxidační fosforylace
Rychlost využití ATP v buňkách řídí jeho syntézu a zase díky vazbě oxidační fosforylace s elektronovým transportním řetězcem také obecně reguluje rychlost elektronového transportu..
Oxidační fosforylace má přísnou kontrolu, která zajišťuje, že ATP není generován rychleji, než je spotřebován. V procesu přenosu elektronů a vázané fosforylace existují určité kroky, které regulují rychlost výroby energie..
Koordinovaná kontrola produkce ATP
Hlavní cesty produkce energie (buněčný ATP) jsou glykolýza, cyklus kyseliny citronové a oxidativní fosforylace. Koordinované řízení těchto tří procesů reguluje syntézu ATP.
Řízení fosforylace poměrem hmotnostní akce ATP závisí na přesném příspěvku elektronů v transportním řetězci. To zase závisí na [NADH] / [NAD+], který je udržován zvýšený působením glykolýzy a cyklu kyseliny citronové.
Tato koordinovaná kontrola se provádí regulací kontrolních bodů glykolýzy (PFK inhibovaná citrátem) a cyklu kyseliny citronové (pyruvát dehydrogenáza, citrát tapease, isocitrát dehydrogenáza a a-ketoglutarát dehydrogenáza)..
Ovládání akceptorem
Komplex IV (cytochrom c oxidáza) je enzym regulovaný jedním ze svých substrátů, to znamená, že jeho aktivita je řízena sníženým cytochromem c (cdva+), který je zase v rovnováze s koncentračním poměrem mezi [NADH] / [NAD+] a poměr hmotnostní akce [ATP] / [ADP] + [Pi].
Čím vyšší je poměr [NADH] / [NAD+] a snižte [ATP] / [ADP] + [Pi], tím vyšší je koncentrace cytochromu [cdva+] a čím větší je aktivita komplexu IV. To se interpretuje například tím, že porovnáme organismy s různými aktivitami odpočinku a vysoké aktivity.
U jedince s vysokou fyzickou aktivitou spotřeba ATP a tedy jeho hydrolýza na ADP + Pi bude velmi vysoká, což vytvoří rozdíl v poměru masové akce, který způsobí zvýšení [cdva+] a tedy zvýšení syntézy ATP. U klidového jedince nastává obrácená situace.
Nakonec se rychlost oxidační fosforylace zvyšuje s koncentrací ADP v mitochondriích. Tato koncentrace závisí na translokátorech ADP-ATP odpovědných za transport adeninových nukleotidů a P.i z cytosolu do mitochondriální matrice.
Odpojení agentů
Oxidační fosforylace je ovlivněna určitými chemickými látkami, které umožňují pokračovat v přenosu elektronů, aniž by došlo k fosforylaci ADP, což vede k odpojení výroby energie a jejímu zachování.
Tato činidla stimulují rychlost spotřeby kyslíku mitochondrií v nepřítomnosti ADP, což také způsobuje zvýšení hydrolýzy ATP. Působí tak, že vylučují prostředníka nebo narušují energetický stav elektronového transportního řetězce.
2,4-dinitrofenol, slabá kyselina, která prochází mitochondriálními membránami, je zodpovědná za rozptýlení protonového gradientu, protože se k nim váže na kyselé straně a uvolňuje je na bazické straně.
Tato sloučenina byla používána jako „pilulka na hubnutí“, protože bylo zjištěno, že způsobuje zvýšení dýchání, tedy zvýšení rychlosti metabolismu a souvisejícího úbytku hmotnosti. Ukázalo se však, že jeho negativní účinek může dokonce způsobit smrt.
Ztráta protonového gradientu produkuje teplo. Buňky v hnědé tukové tkáni používají k výrobě tepla hormonálně řízené odpojení. Hibernující savci a novorozenci, kterým chybí srst, se skládají z této tkáně, která slouží jako druh tepelné přikrývky..
Inhibitory
Sloučeniny nebo inhibiční látky zabraňují konzumaci Odva (transport elektronů), jako je asociovaná oxidační fosforylace. Tato činidla zabraňují tvorbě ATP pomocí energie vyrobené v elektronickém přenosu. Proto se dopravní řetězec zastaví, protože uvedená spotřeba energie není k dispozici..
Antibiotikum oligomycin funguje jako inhibitor fosforylace u mnoha bakterií a brání stimulaci ADP k syntéze ATP.
Existují také ionoforová činidla, která tvoří komplexy rozpustné v tucích s kationty, jako je K.+ a Na+, a procházejí mitochondriální membránou s těmito kationty. Mitochondrie pak používají energii produkovanou při transportu elektronů k čerpání kationtů namísto syntézy ATP..
Reference
- Alberts, B., Bray, D., Hopkin, K., Johnson, A., Lewis, J., Raff, M., Roberts, K. & Walter, P. (2004). Základní buněčná biologie. New York: Garland Science.
- Cooper, G. M., Hausman, R. E. & Wright, N. (2010). Buňka. (str. 397-402). Marban.
- Devlin, T. M. (1992). Učebnice biochemie: s klinickými korelacemi. John Wiley & Sons, Inc..
- Garrett, R. H. a Grisham, C. M. (2008). Biochemie. Thomson Brooks / Cole.
- Lodish, H., Darnell, J. E., Berk, A., Kaiser, C. A., Krieger, M., Scott, M. P., & Matsudaira, P. (2008). Molekulární buněčná biologie. Macmillana.
- Nelson, D. L. a Cox, M. M. (2006). Lehningerovy principy biochemie 4. vydání. Ed Omega. Barcelona.
- Voet, D. a Voet, J. G. (2006). Biochemie. Panamerican Medical Ed..



Zatím žádné komentáře