
Hemokateréza, co to je, proces a funkce

The hemokateritida jedná se o sérii událostí, které se odehrávají za účelem „zbavení se cirkulace“ starých červených krvinek, což se děje 120 dní po propuštění do krve. Lze říci, že hemokateréza je opakem hematopoézy, protože druhá je postup, při kterém se tvoří červené krvinky.
Hemokateréza je méně známý proces než hematopoéza, ale není o nic méně důležitá, protože normální fyziologie tvorby a destrukce červených krvinek do značné míry závisí na vzájemné interakci. Hemokateréza je rozdělena do dvou hlavních procesů: destrukce červených krvinek a „recyklace hemoglobinu“.
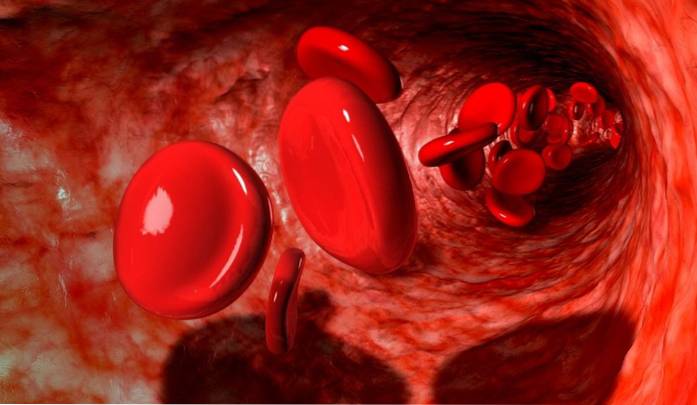
K tomu je nutné, aby řada biologických procesů vzájemně interagovala, takže červené krvinky mohou být degradovány, jakmile dosáhnou své přirozené životnosti..
Rejstřík článků
- 1 Proces
- 1.1 Apoptóza
- 1.2 Síť sinusových kapilár
- 1.3 Recyklace hemoglobinu
- 2 Funkce hemokaterézy
- 3 Rozdíly mezi hemokaterézou a krvetvorbou
- 4 Odkazy
Proces
Buňky, jako jsou buňky kůže nebo sliznice trávicího traktu, rostou v jakémsi „nosném pásu“ podél epitelu, dokud se nakonec neoddělí (nevylučují) a neuvolní se. Místo toho jsou červené krvinky uvolňovány do oběhu, kde zůstávají volné, přičemž svou funkci vykonávají přibližně 120 dní..
Během tohoto procesu řada vysoce specializovaných mechanismů zabraňuje „úniku“ červených krvinek z cév, jejich filtrování do moči nebo odklonění z krevního řečiště..
Pokud by tedy procesy spojené s hemokaterézou neexistovaly, mohly by červené krvinky zůstat v oběhu neomezeně dlouho..
To se však neděje; naopak, jakmile dosáhnou své životnosti, jsou červené krvinky vylučovány z krevního oběhu díky spojení řady velmi složitých procesů, které začínají apoptózou.
Apoptóza
Apoptóza nebo „programovaná buněčná smrt“ je proces, kterým je buňka předurčena k tomu, aby zemřela v určité době nebo jakmile vykonala určitou funkci..
V případě červených krvinek, postrádajících buněčná jádra a organely, nemá buňka schopnost napravit poškození buněčné membrány, produkt rozkladu fosfolipidů a stres způsobený cirkulací kilometry cév.
Postupem času se tedy buněčná membrána červených krvinek stává stále tenčí a křehčí až do té míry, že již není možné udržet její integritu. Buňka tedy doslova exploduje.
Nikde však nevybuchne. Ve skutečnosti by to byl problém, protože by to mohlo vést k zablokování cév. Z tohoto důvodu existuje vysoce specializovaná vaskulární síť, jejíž funkcí je téměř výhradně ničit staré červené krvinky, které procházejí..
Sínusová kapilární síť
Je to síť kapilár ve slezině a v menší míře v játrech. V těchto bohato vaskularizovaných orgánech je komplikovaná síť stále tenčích a klikatých kapilár, které nutí červené krvinky kroutit se a kroutit se, když procházejí..
Tímto způsobem budou moci projít pouze ty buňky s dostatečně pružnou buněčnou membránou, zatímco červené krvinky s křehkými membránami se rozloží a uvolní své složky - zejména skupinu hemu - směrem k okolní tkáni, kde bude proces recyklace místo..
Recyklace hemoglobinu
Jakmile jsou rozbity, zbytky červených krvinek jsou fagocytovány (konzumovány) makrofágy (specializované buňky hojné v játrech a slezině), které štěpí různé složky, dokud nejsou redukovány na své základní prvky.
V tomto smyslu je globinová část (protein) rozložena na aminokyseliny, které ji tvoří, které budou později použity k syntéze nových proteinů..
Hemová skupina se rozkládá až do získání železa, jehož část se stane součástí žluči jako bilirubin, zatímco další část je navázána na proteiny (transferin, feritin), kde může být skladována, dokud není potřeba při syntéze nových molekuly skupiny hemu.
Jakmile jsou dokončeny všechny fáze hemokaterézy, je životní cyklus červených krvinek uzavřen, což vytváří prostor pro nové buňky a recykluje životně důležité složky červených krvinek, aby byly znovu použity.
Funkce hemokaterézy
Nejviditelnější funkcí hemokaterézy je odstranění červených krvinek, které již dosáhly své životnosti z oběhu. To však má důsledky, které jdou dále, například:
- Umožňuje rovnováhu mezi tvorbou a vylučováním červených krvinek.
- Pomáhá udržovat hustotu krve a zabraňuje příliš velkému množství červených krvinek.
- Umožňuje, aby krev byla vždy udržována na maximální přepravní kapacitě kyslíku, čímž eliminuje buňky, které již nemohou optimálně vykonávat svou funkci.
- Pomáhá udržovat zásoby železa v těle stabilní.
- Zajišťuje, že cirkulující červené krvinky mají schopnost dostat se do všech koutů těla kapilární sítí.
- Zabraňuje vstupu deformovaných nebo abnormálních červených krvinek do oběhu, jako je tomu v případě sférocytózy, srpkovité anémie a eliptocytózy, kromě jiných stavů spojených s tvorbou změněných červených krvinek.
Rozdíly mezi hemokaterézou a krvetvorbou
První rozdíl spočívá v tom, že krvetvorba „generuje“ nové červené krvinky, zatímco hemokateréza „ničí“ staré nebo špatné červené krvinky. Mezi těmito dvěma procesy je však třeba vzít v úvahu další rozdíly..
- Hematopoéza probíhá v kostní dřeni, zatímco hemokateréza se vyskytuje ve slezině a játrech.
- Hematopoéza je modulována hormony (erytropoetin), zatímco hemokateréza je předurčena od okamžiku, kdy erytrocyt vstupuje do oběhu.
- Hematopoéza vyžaduje konzumaci „surovin“, jako jsou aminokyseliny a železo, k produkci nových buněk, zatímco hemokateréza uvolňuje tyto sloučeniny k pozdějšímu skladování nebo použití..
- Hematopoéza je buněčný proces, který zahrnuje složité chemické reakce v kostní dřeni, zatímco hemokateréza je relativně jednoduchý mechanický proces.
- Hematopoéza spotřebovává energii; hemokateréza ne.
Reference
-
- Tizianello, A., Pannacciulli, I., Salvidio, E., & Ajmar, F. (1961). Kvantitativní hodnocení podílu sleziny a jater na normální hemokateréze. Journal of Internal Medicine, 169(3), 303-311.
- Pannacciulli, I., & Tizianello, A. (1960). Játra jako místo hemokaterézy po splenektomii. Lékařská minerva, 51, 2785.
- TIZIANELLO, A., PANNACCIULLI, I., & SALVIDIO, E. (1960). Slezina jako místo normální hemokaterézy. Experimentální studie. Il Progresso medico, 16, 527.
- Sánchez-Fayos, J., & Outeiriño, J. (1973). Úvod do dynamické fyziopatologie buněčného systému hemopoéza-hemokateréza. Španělský klinický deník, 131(6), 431-438.
- Balduini, C., Brovelli, A., Balduini, C. L., & Ascari, E. (1979). Strukturální modifikace membránových glykoproteinů během životnosti erytrocytů. Ricerca na klinice a v laboratoři, 9(1), 13.
- Maker, V. K., & Guzman-Arrieta, E. D. (2015). Slezina. v Kognitivní perly v obecné chirurgii (str. 385-398). Springer, New York, NY.
- Pizzi, M., Fuligni, F., Santoro, L., Sabattini, E., Ichino, M., De Vito, R.,… & Alaggio, R. (2017). Histologie sleziny u dětí se srpkovitou anémií a dědičnou sférocytózou: náznaky patofyziologie onemocnění. Lidská patologie, 60, 95-103.

Zatím žádné komentáře