
Kyselý déšť, jak se tvoří, složení, reakce a účinky

The kyselý déšť Jedná se o mokré nebo suché srážení látek, které generují pH nižší než 5,6. Tyto srážky mohou být mokré (zředěné dešťovou vodou) nebo suché (depozice částic nebo aerosolů).
Termín „kyselý déšť“ poprvé navrhl anglický badatel Robert Angus Smith v roce 1850, uprostřed průmyslové revoluce. Nejpočetnější kyseliny, které se tvoří v atmosféře, jsou dusičná a sírová oxidací přírodních nebo umělých znečišťujících látek..
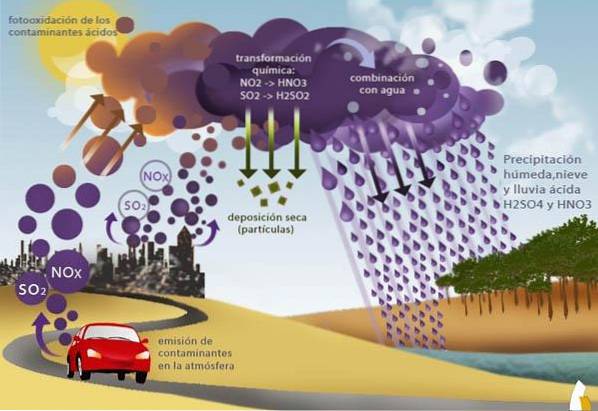
Nejvýznamnějšími znečišťujícími látkami jsou oxidy: NO2, NO3, SO2, jejichž přirozeným zdrojem jsou sopečné erupce, lesní požáry a degradace bakterií. Umělými zdroji jsou emise plynů ze spalování fosilních paliv (průmyslová činnost a automobilová doprava).
Kyselý déšť má negativní dopady na životní prostředí, jako je okyselování půd a vod, které ovlivňují živé bytosti, včetně lidí. Podobně jsou půdy a voda kontaminovány těžkými kovy a ve vodních útvarech dochází k eutrofizaci..
Na vegetační úrovni dochází k přímému poškození listů a je ovlivněn růst rostlin. Okyselení půdy navíc znehybňuje živiny a ovlivňuje mykorhizy (půdní houby). Podobně budovy, stroje, památky a umělecká díla vystavená těmto prvkům jsou vážně oxidována nebo erodována účinkem vysrážených kyselin..
K nápravě účinků kyselých dešťů lze přijmout některá zásadní opatření, jako je ochrana památek a úprava okyselování půd a vod. Základním řešením pro kyselé deště je však snížení emise chemických látek, které jsou předchůdci tvorby kyselin, do atmosféry..
Rejstřík článků
- 1 Jak vzniká kyselý déšť?
- 1.1 Chemické prekurzory
- 1.2 Troposférický proces a vyrobené kyseliny
- 1.3 Srážky
- 2 Složení
- 3 Chemické reakce kyselých dešťů
- 3.1 Tvorba kyseliny sírové (H2SO4)
- 3.2 Tvorba kyseliny dusičné (HNO3)
- 4 Dopady na životní prostředí
- 4.1 Okyselování půdy a jeho vliv na vegetaci
- 4.2 Dopad na kolektory a lidské zdraví
- 4.3 Zhoršení budov, památek a materiálů
- 5 Flóra a fauna
- 5.1 Rostliny a zvířata ve vodních útvarech lentic
- 5.2 Vegetace a dostupnost živin
- 5.3 Přímé poškození rostlin a zvířat
- 6 řešení
- 6.1 Snižte emise
- 6.2 Použijte opatření pro korekci kyselosti
- 6.3 Ochrana povrchu
- 7 Reference
Jak se tvoří kyselý déšť?

Chemické prekurzorové látky
Fenomén kyselých dešťů začíná emisemi chemických sloučenin do atmosféry, které jsou předchůdci tvorby kyselin. Tyto sloučeniny mohou být emitovány z přírodních nebo umělých zdrojů.
Přírodní zdroje zahrnují sopečné erupce, vegetační požáry a emise oceánů. Jako umělé zdroje působí průmyslové emise, emise ze spalovacích motorových vozidel nebo spalování odpadu.
Tyto zdroje emitují různé sloučeniny, které mohou generovat kyseliny v atmosféře. Nejdůležitější jsou však oxidy dusíku a oxidy síry.
Oxidy dusíku jsou známé jako NOx a zahrnují oxid dusičitý (NO2) a oxid dusný (NO). Oxid siřičitý je SO2 nebo oxid siřičitý.
Troposférický proces a vyrobené kyseliny
Fenomén kyselých dešťů se vyskytuje v troposféře (atmosférická zóna, která vede od zemského povrchu do výšky 16 km).
V troposféře mohou vzdušné proudy přenášet tyto sloučeniny na jakoukoli část planety, což z ní dělá globální problém. V tomto procesu dusík a oxidy síry interagují s jinými sloučeninami za vzniku kyseliny dusičné a kyseliny sírové..
Podpora reakce
Chemické reakce mohou být prováděny buď na pevných částicích v suspenzi nebo v kapkách vody v suspenzi..
Kyselina dusičná se tvoří hlavně v plynné fázi kvůli své nízké rozpustnosti ve vodě. Kyselina sírová je rozpustnější ve vodě a je hlavní složkou kyselého deště.
Kyselina dusičná
Při tvorbě kyseliny dusičné (HNO3) reagují oxidy dusíku s vodou, s radikály, jako je OH (v menší míře s HO2 a CH3O2), nebo s troposférickým ozonem (O3).
Kyselina sírová
V případě výroby kyseliny sírové (H2SO4) se podílejí také radikály OH, HO2, CH3O2, voda a ozon. Dále může být vytvořen reakcí s peroxidem vodíku (H2O2) a různými oxidy kovů..
Kyselina uhličitá
H2CO3 vzniká díky fotochemické reakci oxidu uhličitého s atmosférickou vodou.
Kyselina chlorovodíková
HCl představuje pouze 2% kyselého deště a jeho prekurzorem je methylchlorid (ClCH3). Tato sloučenina pochází z oceánů a je oxidována OH radikály za vzniku kyseliny chlorovodíkové..
Srážky
Jakmile se vytvoří kyselé sloučeniny (kyselina dusičná nebo kyselina sírová a v menší míře kyselina chlorovodíková), budou se vysrážet.
Srážení může být depozicí suspendovaných částic, ve kterých proběhla okyselovací reakce v plynné fázi. Dalším způsobem je, že v dešti se sráží kondenzovaná voda, kde se tvoří kyseliny.
Složení
Přirozená kyselost deště se blíží hodnotě pH 5,6, i když v některých nekontaminovaných oblastech jsou hodnoty 5. Tyto nízké hodnoty pH byly spojeny s přítomností kyselin přírodního původu..
Předpokládá se, že v závislosti na úrovni pH lze déšť rozdělit na:
a) Mírně kyselé (pH mezi 4,7 a 5,6)
b) Střední kyselina (pH mezi 4,3 a 4,7)
c) Silně kyselé (pH menší nebo rovné 4,3).
Pokud má déšť koncentraci> 1,3 mg / l dusičnanů a> 3 mg / l v případě síranů, považuje se kontaminace za vysokou.
Kyselý déšť je tvořen ve více než dvou třetinách případů přítomností kyseliny sírové, následované v hojném množství kyselinou dusičnou. Dalšími složkami, které mohou přispívat ke kyselosti deště, jsou kyselina chlorovodíková a kyselina uhličitá..
Chemické reakce kyselého deště
Tvorba kyseliny sírové (H2SO4)
Produkce kyseliny sírové může probíhat v plynné fázi nebo v kapalné fázi.
Plynná fáze
Pouze 3–4% SO2 se v plynné fázi oxiduje za vzniku kyseliny sírové. Existuje mnoho cest pro tvorbu kyseliny sírové z plynných prekurzorů, zde je ukázána reakce SO2 s troposférickým ozonem.
Reakce probíhá ve dvou fázích:
1. - Oxid siřičitý reaguje s troposférickým ozonem za vzniku oxidu siřičitého a uvolňování kyslíku.
SO2 + O3 = SO3 + O2
2.- Potom se oxid sírový oxiduje vodními parami a vytváří kyselinu sírovou.
SO3 + H2O = H2SO4
Kapalná fáze
V kapkách vody, které vytvoří déšť, může být kyselina sírová produkována několika způsoby:
1. - SO2 se rozpouští ve vodě za vzniku kyseliny sírové a ta je oxidována peroxidem vodíku:
SO2 + H2O = H2SO2
H2SO2 + H2O2 = H2SO4 + H2O
2. - Fotokatalytický mechanismus: V tomto případě se částice oxidu kovu (železo, zinek, titan) aktivují působením slunečního záření (fotochemická aktivace) a oxidují SO2 za vzniku kyseliny sírové.
Tvorba kyseliny dusičné (HNO3)
Troposférický ozon O3 produkuje transformaci NO2 na HNO3 ve třístupňovém procesu:
1. - NO2 + O3 = NO3 + O2
2. - NO3 + NO2 = N2O5
3. - N2O5 + H20 = 2HNO3
Dopady na životní prostředí

Okyselování půdy a její účinky na vegetaci
Účinek kyselého deště na půdu se liší v závislosti na jeho složení. Například půdy vápnitého, čedičového a magmatického původu mají větší schopnost neutralizovat kyselost..
Půdy bohaté na křemen jako inertní materiál nejsou schopné regulovat obsah kyselin. V půdách, kde kyselý déšť zvyšuje kyselost, se tak uvolňují a odnášejí kovové ionty, které jsou toxické pro rostliny a zvířata..
Relevantním případem je rozpuštění aluminosilikátů, které uvolňují ionty hliníku, které jsou velmi škodlivé pro vegetaci..
Kyselost půdy obecně snižuje dostupnost živin pro rostliny. Kromě toho podporuje uvolňování a promývání vápníku, což způsobuje nedostatek rostlin.
Dopad na kolektory a lidské zdraví
Ve většině případů kyselý déšť nevypadá ani nechutná jinak než normální déšť, ani nevyvolává pocity na pokožce. Jeho účinky na lidské zdraví jsou nepřímé a jen zřídka způsobují poškození kůže kvůli extrémní kyselosti..
Jedním z problémů kyselých dešťů je, že snížením hodnot pH pod 5 se uvolňují a odnášejí těžké kovy. Tyto znečišťující látky, jako je hliník a kadmium, se mohou dostat do podzemních vodonosných vrstev.
Pokud voda z těchto kontaminovaných vodonosných vrstev přejde do studní používaných k lidské spotřebě, může to způsobit vážné poškození zdraví.
Zhoršení budov, památek a materiálů

Kameny vápenatého typu
Stavby, pomníky a sochy vyrobené z vápence nebo mramoru jsou silně ovlivněny kyselými dešti. To je docela vážné, protože mnoho historických budov a uměleckých děl je postaveno z těchto materiálů..
V případě vápence způsobují kyselé deště rozpuštění vápence a způsobují rekrystalizaci kalcitu. Tato rekrystalizace produkuje na povrchu bělavé tóny..
Ve specifickém případě deště s kyselinou sírovou dochází k jevu sulfatace. Tímto procesem se povrch horniny přemění na sádru a uvolní se CO2..
Mramor, i když je odolnější, je také ovlivněn kyselými dešti. V tomto případě dochází k odlupování kamene, a proto jsou jeho povrchové vrstvy odděleny.
Jiné nekorozivní materiály
U některých budov je strukturální zhoršení malé, ale také s negativními dopady. Například suché kyselé usazeniny špiní stěny, což zvyšuje náklady na údržbu.
Kovy
Kyselý déšť způsobuje korozi kovů v důsledku jevu oxidace. To způsobuje obrovské ekonomické ztráty, protože jsou vážně zasaženy konstrukce, vybavení, stroje a vozidla s kovovými částmi..
Flóra a fauna

Kyselý déšť mění přirozenou rovnováhu vodních a suchozemských ekosystémů.
Rostliny a zvířata ve vodních útvarech lentic
Lentické vodní útvary jsou náchylnější k okyselování, protože jsou uzavřenými ekosystémy. Akumulace kyselin ve vodě má navíc negativní dopady na život, ve kterém se nachází..
Dalším důsledkem okyselování je srážení dusičnanů deštěm, které způsobuje eutrofizaci vodních útvarů. Přebytek živin snižuje dostupný kyslík a negativně ovlivňuje přežití vodních živočichů.
Dalším nepřímým negativním účinkem je unášení iontů těžkých kovů z pozemského prostředí do vodních útvarů. Tyto ionty se uvolňují do půdy působením hydroniových iontů, když se zvyšuje kyselost..
Vegetace a dostupnost živin
Nejzávažnějšími problémy způsobenými okyselováním půdy jsou nehybnost základních živin a nárůst toxických kovů..
Například hliník a hořčík se uvolňují z půdních částic nahrazením vodíkem. Hliník ovlivňuje strukturu a funkci kořenů a snižuje vstřebávání vápníku nezbytného pro rostliny.
Na druhé straně okyselování půdy poškozuje mykorhizy (houby spojené s kořeny), které jsou zásadní v dynamice lesa..
Přímé poškození rostlin a zvířat
Kyselina sírová způsobuje přímé poškození listů degradací chlorofylu a produkcí chlorózy (zežloutnutí listu). U některých druhů klesá růst a produkce životaschopných semen.
Obojživelníci (žáby a ropuchy) jsou obzvláště citliví na účinky kyselosti ve vodě. Některá poškození jsou přímá zranění a snížená obrana proti patogenům (zejména kožním houbám).
Řešení
Snižte emise
Závěrem pro kyselé deště je snížení úniků chemických prekurzorů kyselin do životního prostředí. Nejdůležitější z nich jsou oxidy síry a dusíku.
To však má určité obtíže, protože to má dopad na ekonomické a rozvojové zájmy společností a zemí. Jedním z hlavních zdrojů oxidu siřičitého je například spalování uhlí, které v Číně představuje více než 70% energie..
Existuje několik technologických alternativ, které mohou pomoci snížit emise. Například v průmyslu takzvaná „fluidní lože“ obsahují absorbenty (vápenec nebo dolomit), které zadržují SO2. V případě motorových vozidel a spalovacích motorů obecně přispívají ke snížení emisí SO2 také katalyzátory.
Na druhé straně některé země prováděly konkrétní programy snižování kyselých dešťů. Spojené státy například vyvinuly Národní program hodnocení srážení kyselin (NAPAP). Mezi některá z opatření uvažovaných NAPAP patří implementace používání paliv s nízkým obsahem síry.
Dalším možným opatřením je nahrazení vozového parku elektromobily, aby se snížil jak kyselý déšť, tak globální oteplování. Přestože k dosažení tohoto cíle existuje technologie, tlak v automobilovém a ropném průmyslu oddálil rozhodnutí v tomto ohledu. Dalšími faktory, které ovlivňují, jsou kulturní prvky související s rychlostí, které se vozidlo snaží dosáhnout..
Použijte opatření pro korekci kyselosti
V některých případech lze pH půdy a vody zvýšit přidáním alkálií, například přidáním velkého množství vápna. Tento postup však není proveditelný na velmi velkých pozemcích..
Ochrana povrchu
Kámen
Existují různé způsoby, jak chránit nebo alespoň omezit poškození kamene působením kyselého deště. Jednou z těchto metod je mytí parou nebo horkou vodou..
Mohou být také použita chemická činidla, jako je kyselina fluorovodíková nebo bifluorid amonný. Po umytí může být kámen utěsněn použitím speciálních produktů, které ucpávají póry, jako je hydroxid barnatý.
Kov
Zkorodované kovové povrchy lze chránit potahem nekorozivním kovem, jako je zinek..
K tomu lze použít elektrolytické nanášení nebo lze chráněnou kovovou konstrukci ponořit do ochranného kovu v kapalném stavu..
Reference
- Espada L a A. Sánchez (1995). Vliv kyselých dešťů na korozi kovů. str. 145-171. In: Sastre de Vicente M. (Coord.) Elektrochemie a životní prostředí na prahu XXI. Století. University of La Coruña. Publikační služba. La Coruña, Španělsko.
- García-Ruiz G (2018). Ochrana stavebních konstrukcí v korozivním prostředí. Projekt ukončení inženýrství v průmyslových technologiích. Polytechnická univerzita v Cartageně. Vyšší průmyslová škola průmyslového inženýrství. Cartagena, Španělsko. 75 s.
- Granados-Sánchez D, GF López-Ríos a MA Hernández-García (2010). Kyselé deště a lesní ekosystémy ... Časopis Chapingo Magazine Forestry and Environmental Sciences Series 16: 187-206.
- Likens GE, CT Driscoll a DC Buso (1996). Dlouhodobé účinky kyselých dešťů: reakce a obnova lesního ekosystému. Science, 272; 244-246.
Likens GE a FH Bormann (1974). Acid Rain: Vážný regionální ekologický problém. Science, 184: 1176-1179. - Schindler DW (1988). Účinky kyselých dešťů na sladkovodní ekosystémy. Science, 239: 149-157.
- Vélez-Upegui JJ, MC Valencia-Giraldo, A Londoño-Carvajal, CM González-Duque, JP Mariscal-Moreno (2010). Znečištění ovzduší a kyselé deště. Diagnóza jevu ve městě Manizales. Fakulta inženýrství a architektury. Kolumbijská národní univerzita. Sídlo společnosti Manizales. Redakční Blanecolor Ltda. První vydání. Manizales, Kolumbie. 150 s.



Zatím žádné komentáře