
K čemu je periodická tabulka? 7 důležitých použití

The periodická tabulka Slouží k zobrazení vztahů mezi různými prvky; Lze jej také použít k předpovědi vlastností nových, dosud objevených nebo dosud nesyntetizovaných prvků..
Poskytuje informace a údaje o skupinách, prvcích, atomové hmotnosti, ionizační energii, elektronické konfiguraci, atomovém čísle, elektronegativitě a oxidačních stavech. Periodická tabulka také poskytuje užitečný rámec pro analýzu chemického chování; Je široce používán v oblasti chemie a v mnoha dalších vědách.
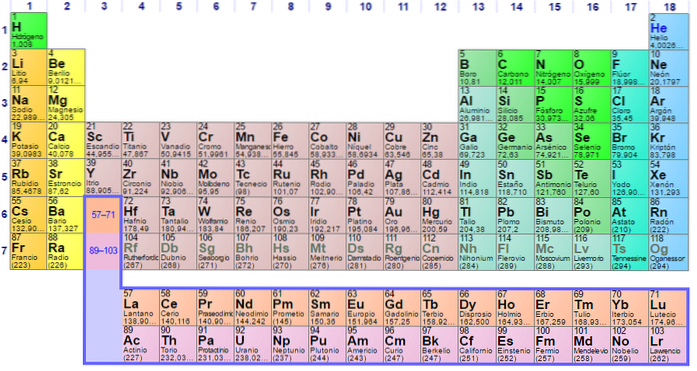
Byl postaven v roce 1869 ruským vědcem Dmitrijem Ivanovičem Mendělejevem k vizualizaci různých vztahů mezi různými chemickými prvky.
Periodická tabulka je řazena podle atomového čísla, elektronových konfigurací a opakujících se chemických vlastností. Je také uspořádáno tak, aby položky s podobným chováním byly ve stejném sloupci.
Tabulka má čtyři obdélníkové bloky s podobnými chemickými vlastnostmi. Obecně platí, že prvky umístěné na levé straně řady jsou kovy a nekovy jsou umístěny vpravo.
Prvky jsou umístěny v periodické tabulce na základě jejich atomové struktury. Každý řádek a každý sloupec mají zvláštní vlastnosti.
Všechny řádky v tabulce jsou čteny zleva doprava a každý řádek je označován jako tečka. Každý sloupec v tabulce se nazývá skupina. Každá skupina v tabulce má stejný počet elektronů.
Je snadné najít počet elektronů ve vnějším obalu každého prvku v tabulce. Skupina jedna má jeden elektron, skupina dvě má dva atd.
Dobrá periodická tabulka je skvělý nástroj pro řešení problémů v chemii. Periodické tabulky najdete na webu nebo je lze vytisknout.
Použití periodické tabulky k čemu slouží?
Znát symbol chemického prvku
Symboly jsou zkratkou pro název položky. V mnoha případech pochází zkratka z původního latinského názvu.
Každý symbol má jedno nebo dvě písmena jako zkratku. Symbol je obvykle zkratkou názvu prvku, ale některé symboly odkazují na staré názvy prvků.
Příkladem tohoto případu je stříbro; jeho symbol je Ag, který odkazuje na jeho staré jméno, které bylo argentum.
Znát atomové číslo prvku
Toto je počet protonů, které atom tohoto prvku obsahuje. Počet protonů je rozhodujícím faktorem, pokud jde o rozlišení jednoho prvku od druhého. Rozdíly v počtu elektronů nebo neutronů nemění typ prvku.
Měnící se počet elektronů produkuje ionty, zatímco změny v počtu neutronů produkují izotopy. Moderní periodická tabulka je uspořádána vzestupně podle atomového čísla.
Určete, co znamenají období a skupiny periodické tabulky
Vodorovné řádky se nazývají tečky. Každé období označuje nejvyšší úroveň energie, kterou každý z elektronů tohoto prvku zabírá ve svém základním stavu..
Svislé sloupce se nazývají skupiny. Každý prvek ve skupině má stejné valenční číslo elektronu a obvykle se chovají podobným způsobem, když souvisí s jinými prvky..
Poslední dva řádky, lanthanoidy a aktinidy, patří do skupiny 3B a jsou uvedeny samostatně..
Znát název prvku
Mnoho periodických tabulek obsahuje také celý název položky. To je užitečné, pokud jde o poznání prvku, protože si nemůžete vždy pamatovat symboly všech prvků.
Seznamte se s atomovou hmotou prvku v jednotkách atomové hmotnosti
Toto číslo se vztahuje k průměrné těžké hmotnosti izotopů chemického prvku. Mendělejevova původní periodická tabulka byla uspořádána tak, aby se prvky zobrazovaly ve vzestupném pořadí podle atomové hmotnosti nebo hmotnosti..
Určete typy prvků
Mnoho periodických tabulek identifikuje různé typy prvků pomocí různých barev pro různé typy prvků.
Mezi tyto typy patří alkalické kovy, obecné kovy, přechodné kovy, nekovy, vzácné plyny, alogeny, kovy alkalických zemin, polokovy, aktinidy a lanthanoidy..
Zobrazit různé trendy (periodicita)
Periodická tabulka je uspořádána tak, aby zobrazovala různé typy trendů (periodicitu). Mezi nimi:
- Atomový poloměr, což je polovina vzdálenosti mezi středy dvou atomů, které se sotva dotýkají:
- Zvyšuje se při přechodu z horní do dolní části periodické tabulky.
- Klesá, jak se pohybuje periodickou tabulkou zleva doprava.
- Ionizační energie, což je energie potřebná k odstranění elektronu z atomu.
- Klesá, jak se pohybuje nahoru a dolů v periodické tabulce.
- Zvyšuje se při pohybu zleva doprava v periodické tabulce.
- Elektronegativita, která měří schopnost vytvářet chemickou vazbu.
- Sestupuje při pohybu nahoru a dolů.
- Zvyšuje se při pohybu zleva doprava.
- Elektronová afinita, která se týká schopnosti prvku přijímat elektron.
Elektronovou afinitu lze předpovědět na základě skupin prvků. Ušlechtilé plyny, jako je argon a neon, mají téměř nulovou elektronovou afinitu a nemají tendenci přijímat elektrony..
Halogeny, jako je chlor a jód, mají vysokou elektronovou afinitu. Většina ostatních skupin prvků má elektronovou afinitu nižší než u alogenů, ale mnohem vyšší než u vzácných plynů..
Reference
- Jaký je účel periodické tabulky? Obnoveno z reference.com
- Jak používat periodickou tabulku (2017) Obnoveno z thoughtco.com
- Jak jsou uspořádány prvky periodické tabulky? Obnoveno z reference.com
- Periodická tabulka. Obnoveno z wikipeda.org
- Proč je periodická tabulka užitečná. Obnoveno z reference.com



Zatím žádné komentáře