
Odůvodnění, postup a použití testu na oxidázu
The oxidázový test Jedná se o diagnostickou metodu, která ukazuje přítomnost komplexu enzymů zvaného cytochromoxidáza c. Tento systém indukuje transformaci cytochromu redukovaného na oxidovaný, protože zachycuje kyslík a ten zase působí jako poslední akceptor elektronů (H+) v dýchacím řetězci.
Termín oxidáza je zkratkovým způsobem, který označuje enzym cytochromoxidáza, známý také jako indofenoloxidáza. V dávných dobách se věřilo, že enzymy cytochromoxidáza a indofenoloxidáza jsou dva různé enzymy, ale dnes je známo, že jsou stejné.
Cytochromy jsou hemoproteiny, které obsahují železo a doplňují systém cytochromoxidázy. Cytochromy se mohou u jednotlivých druhů lišit.
Existují různé odrůdy cytochromů (cytochromy a1, a2, a3 a 0). Některé bakterie mohou produkovat pouze jednu, ale jiné až dvě nebo tři najednou. V tomto smyslu je přítomnost cytochromu a a a3 známá jako cytochromoxidáza c. Toto je typ cytochromu, který detekuje oxidázový test..
Rod Neisseria a Pseudomonas obsahuje cytochromoxidázu c. Tyto rody poskytují pozitivní test na oxidázu a pomáhají je odlišit od rodů Acinetobacter a Stenotrophomonas..
Existují také další rody, které jsou oxidázově pozitivní.
Rejstřík článků
- 1 Odůvodnění
- 1.1 Charakteristiky systému cytochromoxidázy c
- 1.2 Princip zkoušky
- 2 Postup
- 2.1 Činidla
- 2.2 Protokoly
- 3 Použijte
- 4 Kontrola kvality
- 5 Omezení
- 6 doporučení
- 7 Reference
Základ
Vlastnosti systému cytochromoxidázy c
Systém cytochromoxidázy c funguje následovně: mikroorganismy pozitivní na oxidázu používají kyslík k výrobě energie prostřednictvím aerobního dýchání. Tento systém funguje díky transportu elektronů z donorových látek, jako je NADH+ vůči receptorovým látkám, v tomto případě kyslíku.
To má za následek produkci energie (ATP) a vody nebo peroxidu vodíku v závislosti na systému cytochromoxidázy, který mikroorganismus vlastní..
Proto je většina bakterií pozitivních na oxidázu také pozitivní na katalázu, což je nezbytná podmínka pro eliminaci produkovaného peroxidu vodíku, protože tato látka je toxická pro bakterie..
Systém cytochromoxidázy c je přítomen v některých aerobních bakteriích, některých fakultativních anaerobech, několika mikroaerofilních a bez přísných anaerobů. To je pochopitelné, protože přísné anaeroby nemohou žít v přítomnosti kyslíku, proto jim chybí systém cytochromoxidázy..
Princip testu
V tomto testu používá látky, které působí jako umělé akceptory elektronů a nahrazují přirozené v řetězci transportu elektronů..
Používají se hlavně barviva, jako je parafenylendiamin a indofenol, která působí jako receptorové substráty a umělé donory elektronů.
Parafenylendiamin je oxidován systémem cytochromoxidázy c. Barvivo v redukované formě je bezbarvé, ale v oxidované formě je zbarveno.
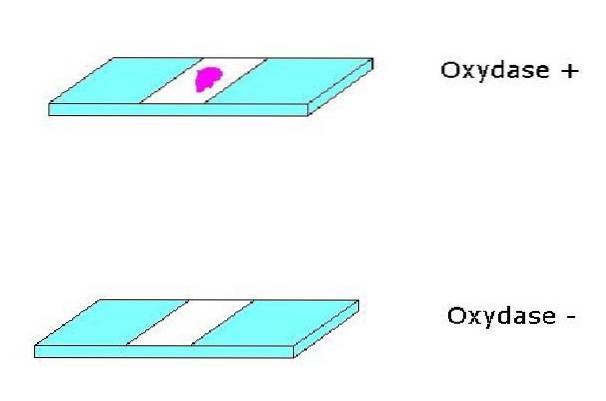
Takto se dokazuje přítomnost systému cytochromoxidázy c; protože pozitivní reakce vygeneruje levandulovou nebo modrofialovou barvu v závislosti na použitém reagenci.
Na druhou stranu, pokud se poslední látka přijímající elektrony v dýchacím řetězci liší od kyslíku, bude test oxidázy negativní (nedochází k žádné produkci barvy); to je případ anaerobních mikroorganismů.
Podobně, pokud se cytochrom používaný mikroorganismem liší od cytochromoxidázy c, provede také negativní test..
Proces
Pro oxidázový test existují různá činidla a protokoly, všechny pro stejný účel..
Činidla
Kovacsovo činidlo, Gordonovo a McLeodovo činidlo, Nadiho činidlo, Carpenter, Suhrlandovo a Morrisonovo činidlo a použití oxidázových disků.
-Kovacs oxidázové činidlo
Skládá se z 1% tetramethyl-p-fenylendiamin dihydrochloridu.
Kovacsovo činidlo se připraví rozpuštěním 1 g výše uvedené látky v 50 ml destilované vody. Jemně se zahřívá, dokud se úplně nerozpustí. Přeneste do jantarové lahve dostatečné kapacity a doplňte objem na 100 ml destilovanou vodou. Před použitím vyčkejte alespoň 15 minut. Uchovávejte v chladničce chráněné před světlem.
Je označen jako kovacs oxidázové činidlo, aby se odlišilo od kovacsova činidla použitého k odhalení indolového testu. Toto činidlo je nejcitlivější, méně toxické, ale dražší než ostatní činidla.
Pozitivní reakce bude prokázána u tohoto činidla se změnou barvy kolonií na levanduli, která rychle zčervená až téměř zčerná. Negativní reakce je evidentní, protože v kolonii nedochází k žádné barevné změně nebo má mírné narůžovělé zabarvení. Médium může také ztmavnout, ale to neznamená pozitivní reakci.
U tohoto činidla je rozhodující doba reakce, změna barvy, ke které dojde mezi 5 až 15 sekundami, je považována za pozitivní reakci..
-Gordonovo a McLeodovo činidlo
Je složen z dimethyl-p-fenylendiamin dihydrochloridu, také známého jako N-dimethyl-p-fenylenediamin nebo monohydrochlorid p-aminodimethylanilinu. Je připraven, jak je popsáno pro kovacs oxidázové činidlo, nahrazením použité látky..
Toto činidlo je o něco stabilnější než činidlo Kovacs oxidázy, i když všechna činidla obsahující p-fenylendiamin jsou nestabilní..
Tato reakce je později, je interpretována jako pozitivní s výskytem modrofialové barvy během 10 až 30 minut..
-Činidlo Nadi
Je složen z 1% α-naftolu v ethylalkoholu (95% ethanolu) a 1% aminodimethylanilinu. Směs se připravuje ve stejných dílech za použití absolutního ethylalkoholu jako ředidla, dokud se nedosáhne dostatečného množství pro 100 ml.
-Činidlo Carpenter, Suhrland a Morrison
Je složen z 1% p-aminodimethylalanin oxalátu. Připravte stejným způsobem, jak je popsáno pro kovacs oxidázové činidlo, výměnou za odpovídající látku.
Když je roztok připraven, připravte testovací proužky následujícím způsobem: Proužky filtračního papíru 6-8 cm Whatman č. 1 jsou impregnovány 1% dimethyl-p-fenylendiamin oxalátovým činidlem.
Nechají se sušit bez kontaktu s kovem, skladují se v nádobách se šroubovacím uzávěrem s vysoušedlem a skladují se v chladničce. Tyto proužky jsou stabilní až 6 měsíců.
Jedná se o nejstabilnější činidlo ze všech zmíněných a v roztoku může trvat až 6 měsíců. Dalším plusovým bodem je, že nezbarví médium kolem kolonie, pokud je použito přímo na talíři.
Vzhled červené barvy je interpretován jako pozitivní test.
-Oxidázové disky
Jsou to komerční disky, které jsou impregnovány reagentem pro oxidázový test. Na trhu existuje několik komerčních značek.
Jeho použití je docela praktické, protože není nutné připravovat nová činidla, což usnadňuje práci. Získané výsledky jsou spolehlivé, pokud jsou disky řádně uchovány.
Protokoly
Metoda přímé desky, nepřímá metoda na papíře a použití disků impregnovaných oxidázovými činidly.
-Metoda přímé desky
2 nebo 3 kapky kteréhokoli z výše uvedených činidel se za tímto účelem přidají přímo na kolonii (kolonie) obsažené v misce kultivačního média, které neobsahuje glukózu..
Interpretuje se změna barvy kolonií, nikoli média. Platná doba reakce závisí na použitém činidle.
-Nepřímá metoda na papíře
Odřízněte kousek filtračního papíru (Whatman č. 1) na velikost 6 cmdva a umístil do prázdné Petriho misky.
Přidejte 2 nebo 3 kapky činidla Kovacs oxidázy na papír, vezměte část kolonie, která má být studována, platinovou rukojetí nebo dřevěným párátkem a rovnoměrně ji rozložte na papír impregnovaný reagentem. Proveďte během 5-10 sekund.
S proužky připravenými s činidly Carpenter, Suhrland a Morrison se na suchý proužek nanese kolonie. Jeden proužek se používá k testování několika kmenů. Tlumočit do 10 s.
-Disky (mpřímá metoda)
Obchodní disky jemně navlhčete sterilní destilovanou vodou a položte je na studovanou kolonii. Doporučuje se používat destičky při 35 ° C, pokud jsou použity destičky při pokojové teplotě nebo chlazené destičky, reakce je o něco pomalejší. Interpretujte změnu barvy mezi 10 až 20 s.
Lze použít kolonie obsažené v krvi nebo čokoládovém agaru.
-Disky (nepřímá metoda)
Navlhčete disk, jak bylo popsáno výše. Umístěte jej do prázdné Petriho misky. Vezměte dostatečné množství kolonie ke studiu s platinovou rukojetí nebo dřevěným párátkem a umístěte na disk. Interpretujte změnu barvy mezi 10 až 20 s.
Použití
Rod Neisseria a Acinetobacter jsou někdy morfologicky velmi podobné, protože i když je rod Acinetobacter gramnegativní tyč, může někdy mít kokokidovou formu a být distribuován v párech, simulujících rod Neisseria..
V tomto případě je oxidázový test opravdu užitečný. Rod Neisseria je pozitivní a Acinetobacter negativní.
Rod Moraxella je však velmi podobný rodu Neisseria a oba dávají pozitivní reakci; proto musí být pro konečnou identifikaci vždy provedeny testy fermentace sacharidů.
Na druhé straně je oxidázový test užitečný k odlišení bakterie patřící do čeledi Enterobacteriaceae (všechny oxidázově negativní) od jiných fermentorů, jako jsou rody Pasteurella, Aeromonas, Plesiomonas (oxidáza pozitivní).
Rod Vibrio a Helicobacter jsou také pozitivní na oxidázu.
QA
Použijte známé kmeny Escherichia coli jako negativní kontrola a kmeny Pseudomonas aeruginosa jako pozitivní kontrola.
Omezení
-Činidla musí být použita čerstvě připravená, jejich skladovatelnost v roztoku při pokojové teplotě je krátká, protože jsou velmi nestabilní. V chladu mohou trvat 5 dní až 2 týdny.
-Činidla jsou bezbarvá, pokud změní barvu, musí být zlikvidována. Poškozené disky jsou evidentní, protože časem ztmavnou.
-Pozitivní reakce s oxidačním činidlem Kovacs mezi 15-60 s je považována za opožděnou reakci a po 60 sekundách by měla být považována za negativní.
-The Haemophylus influenzae poskytuje negativní oxidázovou reakci, pokud se použije jakékoli činidlo s dimethyl-p-fenylendiaminem, ale pozitivní, pokud se použije kovacsovo oxidasové činidlo (tetramethyl-p-fenylendiamin).
-Média obsahující glukózu interferují s testem a dávají falešné negativy.
-Kmeny Bordetella pertussis může dát falešně pozitivní reakci, pokud pocházejí z vysoce koncentrovaných krevních agarových destiček.
-Použití kovových (železných) rukojetí dává falešně pozitivní reakci.
doporučení
-Jelikož jsou reagencie velmi nestabilní a mají tendenci se samooxidovat, doporučuje se zmrazit alikvotní podíly 1 až 2 ml a podle potřeby je odstranit..
-Dalším způsobem, jak oddálit autooxidaci činidla, je přidání 0,1% kyseliny askorbové při přípravě činidel..
-Jelikož jsou činidla nestabilní, doporučuje se týdenní kontrola kvality..
-Činidla, která neprošly testem kontroly kvality, by se neměla používat..
Reference
- Koneman E, Allen S, Janda W, Schreckenberger P, Winn W. (2004). Mikrobiologická diagnostika. 5. vyd. Redakční Panamericana S.A. Argentina.
- Forbes B, Sahm D, Weissfeld A. (2009). Bailey & Scott mikrobiologická diagnostika. 12 ed. Redakční Panamericana S.A. Argentina.
- „Test oxidázy.“ Wikipedia, The Free Encyclopedia. 15. ledna 2018, 10:32 UTC. 3. dubna 2019, 14:03
- Světová zdravotnická organizace. Laboratorní příručka pro identifikaci a testování antimikrobiální citlivosti bakteriálních patogenů důležitých pro veřejné zdraví v rozvojovém světě.2004. K dispozici na: who.int/drugresistance/infosharing
- Testovací proužky pro diagnostiku aktivity oxidázy v bakteriích. Rev Cubana Med Trop [internet]. 2000; 52 (2): 150-151.



Zatím žádné komentáře