
Struktura tetrodotoxinu, charakteristika, použití, účinky

The tetrodotoxin (TTX) je jedovatý aminoperhydrochinazolin, který se nachází v játrech a vaječnících ryb řádu tetraodontiformes; včetně nafoukaných ryb. Stejně tak je to u mloka, plochých červů (ploché červy), kraby, chobotnice s modrými kruhy a velké množství bakterií.
Mezi bakteriální druhy, ve kterých se nachází tetrodotoxin (zkráceně TTX), patří: Vibrio algynolyticus, Pseudoalteromonas tetraodonis, stejně jako v jiných bakteriích rodu Vibrio a Pseudomonas. Odtud lze pochopit, že jeho původ je bakteriální..

Přítomnost exokrinních žláz pro sekreci TTX u bahňáků, jakož i jejich skladování ve slinných žlázách chobotnice s modrým prstencem však ukázaly, že určitá zvířata mohou mít také schopnost syntetizovat ji.
TTX působí na tělo blokováním sodíkových kanálů neuronálních axonů a buněk kosterního a hladkého svalstva; s výjimkou buněk srdečního svalu, které mají „brány“ odolné vůči TTX.
Hlavní příčinou náhlé smrti u člověka zprostředkované TTX je jeho paralyzující účinek na bránici a mezižeberní svaly; svaly potřebné k dýchání. K úmrtí tedy dochází během několika hodin po požití TTX..
Střední letální orální dávka (LD50) tetrodotoxinu pro myši je 334 ug / kg tělesné hmotnosti. Mezitím je LD50 pro kyanid draselný 8,5 mg / kg. To znamená, že TTX je jed asi 25krát účinnější než kyanid draselný..
Rejstřík článků
- 1 Struktura tetrodotoxinu
- 1.1 Klec a vodíkové mosty
- 2 Funkce
- 3 Mechanismus účinku
- 3.1 Blok sodíkových kanálů
- 3.2 Ochrnutí
- 4 použití
- 5 Účinky na tělo
- 5.1 Parestézie
- 5.2 Příznaky
- 5.3 Smrt
- 5.4 Fugus: smrtící talíř
- 6 Reference
Struktura tetrodotoxinu
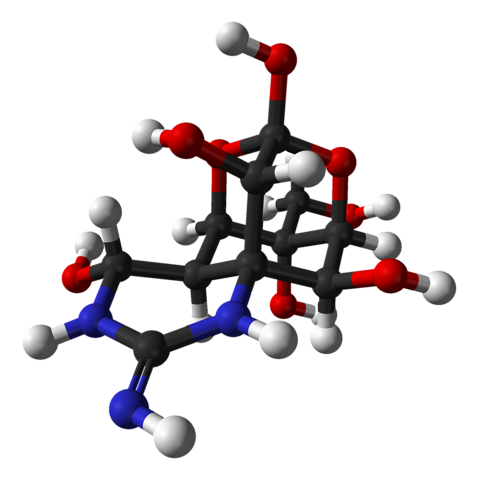
Horní obrázek ukazuje molekulární strukturu tetrodotoxinu s modelem koulí a tyčí. Červená koule odpovídají atomům kyslíku, modrá koule atomům dusíku a bílá koule vodíkům a uhlíkům..
Pokud se na chvíli zastavíte u atomů O, uvidíte, že šest z nich se nachází jako hydroxylové skupiny, OH; na periferii molekuly tedy existuje šest skupin OH. Mezitím jsou dva zbývající atomy jako okysličené můstky v kondenzovaných cyklických jednotkách..
Na druhou stranu existují sotva tři atomy dusíku, ale patří do jedinečné skupiny: guanidino. Tato skupina může nést kladný náboj, pokud C = NH získá vodíkový iont a transformuje se na C = NHdva+; byl by tedy umístěn ve spodní části molekuly. Zatímco nahoře může být -OH nahoře deprotonován a může být jako -O-.
Tetrodotoxin tedy může mít dva iontové náboje současně v různých oblastech své struktury; který, i když se to může zdát složitý, je zjednodušený tím, že jej považujeme za klec.
Klec a vodíkové mosty
Tetrodotoxin lze poté vizualizovat jako klec, protože jeho kondenzované cykly představují kompaktní strukturu. Výše bylo řečeno, že má na svém obvodu šest OH skupin (pokud nemá záporný náboj), kromě tří NH skupin patřících do skupiny guanidino (pokud nemá kladný náboj)..
Celkově je tedy molekula schopná darovat až devět vodíkových vazeb; a podobně může přijímat stejný počet můstků a další dva kvůli vnitřním atomům kyslíku v jeho cyklech. Uvedená klec je tedy docela aktivní, pokud jde o intermolekulární interakce; nemůže se „procházet“, aniž by si toho někdo všiml.
To znamená, že stačí, aby tetrodotoxin kvůli silným interakcím zakotvil dusíkový nebo okysličený povrch. To je ve skutečnosti důvod, proč blokuje sodíkové kanály a chová se jako korková klec, která brání průchodu iontů Na.+ uvnitř buněk.
Vlastnosti
Některé vlastnosti nebo vlastnosti tetrodotoxinu jsou uvedeny níže:
-Jeho molekulární vzorec CjedenáctH17N3NEBO8 a molekulová hmotnost 319,27 g / mol.
-TTX lze připravit z vaječníků nafoukaných ryb. Po homogenizaci se proteiny vysráží a supernatant se podrobí chromatografii na aktivním uhlí; získání 8–9 g čistého TTX na 1 000 g jikry ryb.
-Dehydratovaný TTX je bílý prášek, rozpustný ve vodě a zředěné kyselině octové; ale prakticky nerozpustný v organických rozpouštědlech.
-Je tepelně stabilní, s výjimkou alkalického média. Je také nestabilní, když se zahřeje na 100 ° C v kyselém prostředí.
-Při zahřátí na 220 ° C ztmavne, aniž by se rozložil.
-TTX je zničen silnými kyselinami a zásadami.
-Má disociační konstantu, pKa = 8,76 ve vodě a pKa = 9,4 v 50% alkoholu.
-Je to monoacidická báze, stabilní mezi pH 3 - 8,5.
-Toxicita TTX je eliminována působením 2% hydroxidu sodného po dobu 90 minut..
-Byla odhadnuta hustota TTX 1,3768 g / cm3. Rovněž byla odhadnuta teplota varu 458,31 ° C..
Mechanismus účinku
Blok sodíkového kanálu
TTX blokuje Na kanály+, zabránění šíření akčních potenciálů nebo nervových impulsů v excitovatelných buňkách.
Zabráněním šíření akčních potenciálů vede TTX k paralýze svalových buněk vedoucí ke smrti zvířat v krátké době.
Na kanály+, stejně jako ostatní iontové kanály jsou to proteiny, které procházejí plazmatickou membránou. Ty jsou závislé na napětí; to znamená, že jsou schopné reagovat na adekvátní variaci membránového potenciálu svým otevřením.
TTX je molekula o průměru přibližně 8 Å, která je umístěna na vnější straně Na kanálu+; přesně v ústech, které umožňují přístup do kanálu a brání vstupu Na+ skrz to. Má se za to, že k blokování Na kanálu stačí jedna molekula TTX+.
Ochrnutí
TTX blokováním vstupu Na+ zabraňuje tvorbě akčního potenciálu v neuronové buňce a jeho šíření podél axonu. Stejným způsobem je zabráněno tvorbě akčních potenciálů ve svalových buňkách, což je požadavek na jejich kontrakci..
Jelikož se svalové buňky nestahují, dochází k jejich paralýze. V případě bráničkového svalu a mezižeberních svalů jejich paralýza blokuje dýchání a během několika hodin způsobí smrt.
Aplikace
Nízká dávka TTX má analgetický účinek u pacientů se silnou bolestí, u nichž nedochází k úlevě od konvenční léčby. Bylo léčeno 24 pacientů trpících terminálním karcinomem, kteří byli podrobeni 31 léčebným cyklům s dávkami TTX mezi 15 a 90 µg / den.
Výsledkem bylo klinicky významné snížení intenzity bolesti v 17 z 31 cyklů. Úleva od bolesti přetrvávala dva nebo více týdnů. TTX účinně zmírňoval silnou a refrakterní bolest u většiny pacientů s rakovinou.
Společnost Wex Pharmaceuticals dále studuje použití tetrodotoxinu k léčbě bolesti u pacientů s pokročilým nádorovým onemocněním. A také u uživatelů opia, aby se snížila spotřebovaná dávka drogy.
Účinky na tělo
Parestézie
Nízká dávka TTX produkuje parestézii, což je brnění a necitlivost kolem úst a prstů na rukou a nohou. Tyto příznaky jsou také součástí obecných příznaků otravy TTX..
Příznaky
Existují kontrakce kosterního svalu jako celku, projevující se obtížemi artikulovat slova a polykat. Žáci otrávených lidí jsou zafixováni a rozšířeni. Nejdramatičtější věcí je, že lidé jsou úplně paralyzovaní, ale vědomi si.
Kardiovaskulární příznaky jsou charakterizovány bolestí na hrudi, hypotenzí a srdeční arytmií. Dýchací potíže se projevují dušností a cyanózou; to je namodralá barva kůže a ústní dutiny.
Nevolnost, zvracení a průjem jsou v gastrointestinálním systému běžné..
Smrt
Míra úmrtí lidí, kteří požili TTX a nebyli léčeni, je vyšší než 50%. Smrt nastává do 4 až 6 hodin po otravě.
V některých případech může smrt nastat už za 20 minut. TTX může zabít člověka v dávce od 1 do 4 mg..
Fugus: smrtící jídlo
V minulosti byla většina otrav TTX způsobena požitím fugu. Fugus je jídlo, které je považováno za pochoutku japonského jídla a je připraveno z nafoukaných ryb; který má nejvyšší koncentraci TTX v játrech a pohlavních žlázách.
V současné době byly zavedeny kontroly ke snížení rizika otravy z této příčiny. Lidé, kteří zpracovávají ryby typu Puffer a kteří připravují fugus, vyžadují několikaleté školení, aby získali obratnost, která jim umožňuje připravit pokrm.
Reference
- Lago, J., Rodríguez, L. P., Blanco, L., Vieites, J. M., & Cabado, A. G. (2015). Tetrodotoxin, extrémně silný mořský neurotoxin: distribuce, toxicita, původ a terapeutická použití. Marine drog, 13 (10), 6384-6406. doi: 10,3390 / md13106384
- Národní centrum pro biotechnologické informace. (2019). Tetrodotoxin. Databáze PubChem. CID = 11174599. Obnoveno z: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2019). Tetrodotoxin. Obnoveno z: en.wikipedia.org
- Chemická kniha. (2017). Tetrodotoxin. Obnoveno z: chemicalbook.com
- Drogová banka. (2019). Tetrodotoxin. Obnoveno z: drugbank.ca



Zatím žádné komentáře