
Struktura oxidu ceričitého, vlastnosti, použití

The oxid ceričitý u oxid ceričitý je bílá nebo světle žlutá anorganická pevná látka, která se vyrábí oxidací ceru (Ce) kyslíkem na jeho 4+ valenci. Chemický vzorec oxidu ceričitého je CeOdva a je nejstabilnějším oxidem ceru.
Cer (Ce) je prvek ze série lanthanoidů, které jsou zahrnuty do skupiny vzácných zemin. Přirozeným zdrojem tohoto oxidu je minerál bastnasit. V komerčním koncentrátu tohoto minerálu je CeOdva lze nalézt v přibližném podílu až 30% hmotnostních.

Generální řediteldva lze snadno získat zahřátím hydroxidu ceričitého, Ce (OH) na vzduchu nebo v kyslíku3, nebo jakákoli sůl ceru (III), jako je oxalát, uhličitan nebo dusičnan.
Generální řediteldva Stechiometrické lze získat vysokoteplotní reakcí oxidu ceričitého s elementárním kyslíkem. Kyslík musí být v přebytku a musí být ponechán dostatek času na dokončení přeměny různých nestechiometrických fází, které se tvoří..
Tyto fáze zahrnují vícebarevné produkty se vzorcem CeOX (kde x se pohybuje mezi 1,5 a 2,0). Také se jim říká CeO2-x, kde x může mít hodnotu až 0,3. Generální řediteldva Je to nejpoužívanější forma Ce v průmyslu. Má nízkou klasifikaci toxicity, zejména kvůli své špatné rozpustnosti ve vodě..

Rejstřík článků
- 1 Struktura
- 2 Názvosloví
- 3 Vlastnosti
- 3.1 Fyzický stav
- 3.2 Mohsova tvrdost
- 3.3 Molekulová hmotnost
- 3.4 Bod tání
- 3.5 Hustota
- 3.6 Rozpustnost
- 3.7 Index lomu
- 3.8 Další vlastnosti
- 4 použití
- 4.1 - V hutním průmyslu
- 4.2 - Ve sklářském průmyslu
- 4.3 - Ve smaltech
- 4,4 - V keramice ze zirkonu
- 4.5 - V katalyzátorech pro regulaci emisí vozidla
- 4.6 - Při katalýze chemických reakcí
- 4.7 - V biologických a biomedicínských aplikacích
- 4.8 - Jiná použití
- 5 Reference
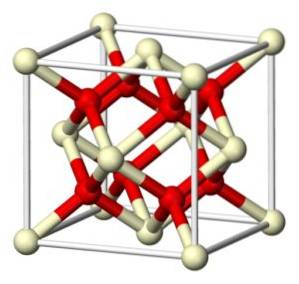
Struktura
Stechiometrický oxid ceričitý krystalizuje v fluoritové krychlové mřížce (CaFdva), s 8 ionty Odva- v kubické struktuře koordinované se 4 ionty Ce4+.
Nomenklatura
- Oxid ceričitý.
- Oxid ceričitý.
- Oxid ceričitý.
- Ceria.
- Stechiometrický oxid ceričitý: materiál vyrobený výhradně z CeOdva.
- Nestechiometrický oxid ceričitý: materiál tvořený směsnými oxidy z CeOdva až po generálního ředitele1.5
Vlastnosti
Fyzický stav
Světle žlutá pevná látka. Barva je citlivá na stechiometrii a přítomnost dalších lanthanoidů. Nestechiometrické oxidy jsou často modré.
Mohsova tvrdost
Přibližně 6-6,1.
Molekulární váha
172,12 g / mol.
Bod tání
Přibližně 2 600 ° C.
Hustota
7,132 g / cm3
Rozpustnost
Nerozpustný v teplé a studené vodě. Rozpustný v koncentrované kyselině sírové a koncentrované kyselině dusičné. Nerozpustný ve zředěných kyselinách.
Index lomu
2.2.
Další vlastnosti
Generální řediteldva Je to inertní látka, není napadena silnými kyselinami nebo zásadami. Může však být rozpuštěn kyselinami v přítomnosti redukčních činidel, jako je peroxid vodíku (HdvaNEBOdva) nebo cín (II), mimo jiné, generující roztoky ceru (III).
Má vysokou tepelnou stabilitu. Během obvyklých intervalů ohřevu nepodléhá krystalografickým změnám.
Jeho hydratovaný derivát (CeOdva.nHdvaO) je žlutá a želatinová sraženina, která se získá zpracováním roztoků ceru (IV) bázemi.
Generální řediteldva špatně se vstřebává z gastrointestinálního traktu, takže nemá žádné toxické účinky.
Aplikace
- V metalurgickém průmyslu
Generální řediteldva používané na elektrodách určitých svařovacích technologií, jako je svařování wolframovým obloukem pomocí inertního plynu.
Oxid je jemně rozptýlen v celé wolframové matrici. Při nízkém napětí tyto částice CeOdva poskytují větší spolehlivost než samotný wolfram.
- Ve sklářském průmyslu
Leštění skla
Oxid ceru je nejúčinnějším lešticím prostředkem pro většinu komerčních skleněných kompozic. Generální řediteldva téměř úplně nahradil jiné leštící oxidy, jako je FedvaNEBO3, oxid křemičitý a ZrOdva, díky své vyšší rychlosti leštění a čištění, které se zvyšují se zvyšujícím se stupněm čistoty oxidu.
Komerční leštidla na sklo na bázi prášků oxidu ceričitého mají definované velikosti částic a kontrolovanou dispergovatelnost ve vodných systémech..
Proces leštění skla vyžaduje vodu a to, co je odstraněno nebo reformováno, je měkčí hydratovaná povrchová vrstva. Leštidlo by mělo mít tvrdost podle Mohse přibližně 6,5, blízkou tvrdosti většiny skla.
Oxid ceričitý ve vodě obsahuje pár Ce (IV) / Ce (III), který svými oxidačně-redukčními reakcemi může poskytnout chemickou pomoc při rozpadu sítě silikátu skla.
Generální řediteldva s vysokým stupněm čistoty se používá k ošetření zrcadel, televizorů, očních čoček a přesného optického materiálu.
Odbarvení skla
Generální řediteldva může odbarvit sodnovápenaté sklo na lahve, džbány a podobně. Ce (IV) oxiduje nečistoty Fe (II), které poskytují modrozelenou barvu, na Fe (III), které dává 10krát slabší žlutou barvu.
Sklo odolné proti záření
Přidání 1% CeOdva Al sklo potlačuje změnu barvy nebo ztmavnutí skla způsobené bombardováním vysokoenergetických elektronů v TV brýlích. Totéž platí pro sklo používané v oknech v horkých komorách v jaderném průmyslu, protože potlačuje zbarvení vyvolané gama paprsky..
Předpokládá se, že mechanismus potlačení závisí na přítomnosti iontů Ce4+ a Ce3+ ve skleněné síti.
Fotocitlivé brýle
Některé skleněné formulace mohou vytvářet latentní obrazy, které lze poté převést na trvalou strukturu nebo barvu..
Tento typ skla obsahuje CeOdva který absorbuje UV záření a uvolňuje elektrony ve skleněné matrici.
Po ošetření se generuje růst krystalů jiných sloučenin ve skle a vytváří se podrobné vzory pro elektronické nebo dekorativní použití..
- V emailech
Díky vysokému indexu lomu CeOdva je zakalující činidlo ve smaltovaných kompozicích používaných jako ochranné povlaky na kovech.
Díky vysoké tepelné stabilitě a jedinečnému krystalografickému tvaru v celém rozsahu teplot dosažených během procesu zasklení je vhodný pro použití v porcelánových emailech..
V této aplikaci CeOdva Poskytuje požadovaný bílý povlak během vyhoření skloviny. Je to složka, která poskytuje neprůhlednost.
- V zirkoniové keramice
Zirkoniová keramika je tepelný izolátor a používá se při vysokých teplotách. Vyžaduje přísadu, která má vysokou pevnost a houževnatost. Přidávání CeOdva Oxid zirkoničitý vyrábí materiál s výjimečnou houževnatostí a dobrou odolností.
CeO-dopovaný oxid zirkoničitýdva používá se v nátěrech jako tepelná bariéra na kovových površích.
Například v částech leteckých motorů tyto povlaky chrání před vysokými teplotami, kterým by byly vystaveny kovy..
- V katalyzátorech pro regulaci emisí vozidla
Generální řediteldva Je aktivní složkou při odstraňování znečišťujících látek z emisí vozidel. To je do značné míry způsobeno jeho schopností ukládat nebo uvolňovat kyslík v závislosti na okolních podmínkách..
Katalyzátor v motorových vozidlech je umístěn mezi motorem a výstupem výfukových plynů. Má katalyzátor, který musí oxidovat nespálené uhlovodíky, převádět CO na COdva, a snížit oxidy dusíku, NOX, do Ndva mědva.

Kromě platiny a dalších katalytických kovů je hlavní aktivní složkou těchto multifunkčních systémů CeOdva.
Každý katalyzátor obsahuje 50-100 g CeOdva jemně rozdělené, které slouží několika funkcím. Nejdůležitější jsou:
Působí jako stabilizátor pro oxid hlinitý o vysoké ploše
Oxid hlinitý o vysoké ploše má tendenci slinovat a během provozu za vysokých teplot ztrácí svůj velký povrch. To je zpožděno přítomností CeOdva.
Chová se jako uvolňovač kyslíkového pufru
Díky své schopnosti tvořit nestechiometrické oxidy CeO2-x, oxid ceričitý poskytuje během období cyklu bohatého na kyslík / palivo elementární kyslík své vlastní struktury.
Oxidace nespálených uhlovodíků pocházejících z motoru a přeměna CO na CO tedy může pokračovat.dva, i když je plynný kyslík nedostatečný.
Poté v období cyklu bohatého na kyslík pohltí kyslík a znovu oxiduje a získá stechiometrickou formu CeOdva.
Ostatní
Funguje jako zesilovač katalytické kapacity rhodia při snižování oxidů dusíku NOX na dusík a kyslík.
- Při katalýze chemických reakcí
V procesech katalytického krakování rafinérií CeOdva působí jako katalytické oxidační činidlo, které napomáhá přeměně SOdva na SO3 a podporuje tvorbu síranů ve specifických pasti procesu.
Generální řediteldva zlepšuje aktivitu katalyzátoru na bázi oxidu železa použitého k získání styrenu vycházejícího z ethylbenzenu. To je pravděpodobně způsobeno pozitivní interakcí mezi páry redukce oxidů Fe (II) - Fe (III) a Ce (III) - Ce (IV).
- V biologických a biomedicínských aplikacích
Byly nalezeny nanočástice CeOdva práce zachycením volných radikálů, jako je superoxid, peroxid vodíku, hydroxylové skupiny a radikály oxidu dusnatého.
Mohou chránit biologické tkáně před poškozením vyvolaným zářením, laserem indukovaným poškozením sítnice, prodloužit životnost fotoreceptorových buněk, snížit poškození páteře, snížit chronický zánět a podpořit angiogenezi nebo tvorbu krevních cév..
Dále některá nanovlákna obsahující nanočástice CeOdva Bylo prokázáno, že jsou toxické proti bakteriálním kmenům a jsou slibnými kandidáty na baktericidní aplikace.
- Jiná použití
Generální řediteldva Jedná se o elektroizolační materiál díky své vynikající chemické stabilitě, vysoké relativní permitivitě (má vysokou tendenci polarizovat při použití elektrického pole) a krystalické mřížce podobné křemíku..
Našel uplatnění v kondenzátorech a tlumících vrstvách supravodivých materiálů.
Používá se také v plynových čidlech, materiálech elektrod palivových článků na tuhé oxidy, kyslíkových pumpách a kyslíkových monitorech..
Reference
- Cotton, F. Albert a Wilkinson, Geoffrey. (1980). Pokročilá anorganická chemie. Čtvrté vydání. John Wiley & Sons.
- Bailar, J. C.; Emeléus, HJ; Sir Ronald Nyholm a Trotman-Dickenson, A.F. (1973). Komplexní anorganická chemie. Svazek 4. Pergamon Press.
- Kirk-Othmer (1994). Encyclopedia of Chemical Technology. Svazek 5. Čtvrté vydání. John Wiley & Sons.
- Ullmann's Encyclopedia of Industrial Chemistry. (1990). Páté vydání. Svazek A6. VCH Verlagsgesellschaft mbH.
- Casals, Eudald a kol. (2012). Analýza a riziko nanomateriálů ve vzorcích prostředí a potravin. In Comprehensive Analytical Chemistry. Obnoveno ze sciencedirect.com.
- Mailadil T. Sebastian. (2008). Alumina, Titania, Ceria, Silicate, Tungstate and other materials. V dielektrických materiálech pro bezdrátovou komunikaci. Obnoveno ze sciencedirect.com.
- Afeesh Rajan Unnithan a kol. (2015). Lešení s antibakteriálními vlastnostmi. In Nanotechnology Applications for Tissue Engineering. Obnoveno ze sciencedirect.com.
- Gottardi V. a kol. (1979). Leštění povrchu skla zkoumané jadernou technikou. Bulletin of the Spanish Society of Ceramics and Glass, Vol.18, No. 3. Obnoveno z boletines.secv.es.



Zatím žádné komentáře