
Struktura octanu draselného, vlastnosti, použití, výroba
The octan draselný je organická sloučenina tvořená iontem draslíku K.+ a acetátový ion CH3VRKAT-. Jeho chemický vzorec je CH3COOK nebo KCH3COO nebo také C.dvaH3KOdva. Je to bezbarvá nebo bílá krystalická pevná látka, velmi dobře rozpustná ve vodě..
Používá se k regulaci kyselosti určitých průmyslově zpracovaných potravin. Díky své vysoké afinitě k vodě se používá v laboratořích nebo při určitých procesech k absorpci vody z jiných sloučenin, například k dehydrataci alkoholu..

Octan draselný se podílí na některých chemických reakcích jako jejich urychlovač a na syntéze organických sloučenin. Umožňuje také zvýšit tvorbu protilátek (přírodních látek, které bojují proti infekcím) v průmyslových metodách jejich výroby..
Díky svým velmi nízkým teplotám je dobrým kandidátem pro použití ve směsích pro tání ledu na betonových silnicích ve velmi chladném podnebí. Podle konzultovaných zdrojů se používá také v hasičských zařízeních a v sestavách k pozorování buněk v mikroskopech..
Rejstřík článků
- 1 Struktura
- 2 Názvosloví
- 3 Vlastnosti
- 3.1 Fyzický stav
- 3,2 Molekulová hmotnost
- 3.3 Teplota tání
- 3.4 Hustota
- 3.5 Rozpustnost
- 3,6 pH
- 3.7 Další vlastnosti
- 3.8 Chování při zahřívání
- 4 Získání
- 5 použití
- 5.1 V různých aplikacích
- 5.2 V polymerním průmyslu
- 5.3 Ve vědeckých a lékařských výzkumných laboratořích
- 5.4 V průmyslové výrobě protilátek
- 5.5 V nemrznoucích směsích
- 5.6 Jak to funguje jako nemrznoucí směs
- 6 Reference
Struktura
Octan draselný je tvořen kationtem draslíku K.+ a acetátový anion CH3VRKAT-. Posledně jmenovaná je konjugovaná báze kyseliny octové CH3COOH. Acetátový ion CH3VRKAT- sestává z methyl-CH3 navázaný na karboxylát -COO-.
Spojení mezi oběma ionty je elektrostatické nebo iontové, to znamená spojení mezi kladným a záporným iontem.
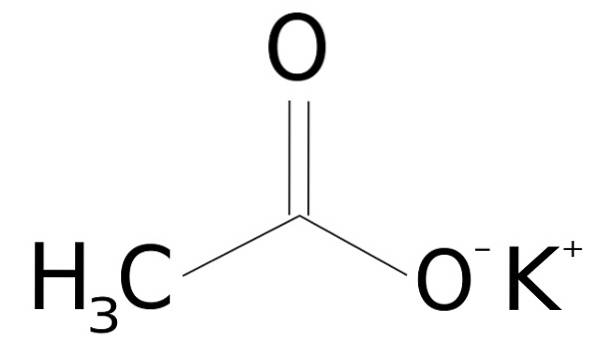
Nomenklatura
- Octan draselný
- Ethanoát draselný
- Draselná sůl kyseliny octové
- AcOK
- KOAc
Vlastnosti
Fyzický stav
Bezbarvá nebo bílá krystalická pevná látka.
Molekulární váha
98,14 g / mol
Bod tání
292 ° C
Hustota
1,6 g / cm3
Rozpustnost
Velmi dobře rozpustný ve vodě: 256 g / 100 ml při 20 ° C.
pH
5% vodný roztok octanu draselného má pH 7,5-9,0.
Další vlastnosti
Někdy má slabou octovou vůni. V 10% roztoku nenapadá hliník při pokojové teplotě, ale při 60-70 ° C kov ztmavne a trpí důlkovou korozí.
Při koncentraci 20% nebo více dochází k napadení povrchu hliníkem při jakékoli teplotě.
Acetát draselný (AcOK) je vysoce rozpustný ve vodě. Má hydrát: KCH3COO.1,5HdvaNebo, což je pevná látka, která se získá krystalizací z vodných roztoků AcOK.
Chování při zahřátí
Pokud je hydratovaný octan draselný (AcOK) (KCH3COO.1,5HdvaO) když dosáhne 40 ° C, začne ztrácet hydratační vodu.
KCH3COO.1,5HdvaO → KCH3COO + 1,5 hodinydvaNebo ↑
Pokud se zahřívá bezvodý octan draselný (bez vody: KCH3COO), po dosažení 340 ° C se začne rozkládat za vzniku uhličitanu draselného K.dvaCO3 podle následující reakce:
2 KCH3COO + 40dva → K.dvaCO3 + 3 HdvaO + 3 COdva↑
Získávání
Může být připraven působením hydroxidu draselného KOH na různé sloučeniny, jako je kyselina octová CH3COOH, anhydrid kyseliny octové (CH3CO)dvaO a octan amonný CH3COONH4.
KOH + CH3COOH → CH3COOK + HdvaNEBO
Lze jej také získat reakcí uhličitanu draselného K.dvaCO3 nebo hydrogenuhličitan draselný KHCO3 s kyselinou octovou CH3COOH.
KHCO3 + CH3COOH → CH3COOK + HdvaO + COdva↑
Octan draselný může být krystalizován z vodného roztoku, aby se získala vysoká čistota.
Aplikace
V různých aplikacích
Octan draselný se používá ve zpracovaném potravinářském průmyslu jako regulátor kyselosti. Používá se jako vysoušedlo v chemických metodách k měření propustnosti vodní páry u některých tkanin..
Slouží jako dehydratační činidlo pro ethanol při výrobě tohoto alkoholu, a to z lignocelulózy, materiálu získaného ze dřeva..
Používá se k výrobě antibiotik a je široce používán v hasičských zařízeních.
V polymerním průmyslu
Používá se k recyklaci polyurethanů, protože slouží ke katalyzování nebo urychlení hydrolýzy a glykolýzy uvedených polymerů tak, aby se z nich staly alkoholy a aminy..
Používá se také při výrobě organických silikonových pryskyřic.
Ve vědeckých a lékařských výzkumných laboratořích
Vysoce čistý octan draselný se používá v laboratořích jako činidlo v analytické chemii. Také provádět lékařsko-vědecký výzkum.
V histopatologických laboratořích se používá k zajištění média s neutrálním pH v nastavení mikroskopu..

Používá se pro syntézu heterocyklických organických sloučenin, což jsou sloučeniny s různými cykly velikosti..
Některé mikroelektrody používané ke studiu elektrických vlastností buněk jsou naplněny koncentrovaným roztokem octanu draselného..
V průmyslové výrobě protilátek
Acetát draselný se používá k velkovýrobě monoklonálních protilátek (které pocházejí ze stejné kmenové buňky) v buněčných kulturách. Umožňuje stimulovat syntézu nebo tvorbu protilátek.
Protilátky jsou látky produkované některými buňkami v krvi k boji proti infekcím způsobeným viry nebo bakteriemi..

V nemrznoucích směsích
Octan draselný se používá v nemrznoucích směsích. proti námraze) za účelem jejich použití k roztavení ledu na silnicích a cementových chodnících a umožnění jejich bezpečného používání.

Výběr octanu draselného (AcOK) pro tuto aplikaci je způsoben skutečností, že 50% hmotn. Vodný roztok AcOK je eutektický a má teplotu tání -62 ° C. To znamená, že i při teplotách až -62 ° C zůstává roztok roztavený..
Eutektikum je homogenní směs složek, která má nejnižší teplotu tání ze všech možných směsí těchto látek, včetně směsi čistých složek..
Jak to funguje jako nemrznoucí směs
Acetát draselný (AcOK) má velmi dobrou schopnost tavit led.
Při teplotě -5 ° C je schopen roztavit 11,5 kg ledu na každý kg AcOK. Tato vlastnost klesá se snižováním teploty, ale i při -50 ° C má schopnost roztavit 1,3 kg ledu na každou kg AcOH..
Při -5 ° C je tato kapacita srovnatelná s kapacitou chloridu sodného nebo kuchyňské soli (NaCl), zatímco od -30 ° C ji výrazně překračuje.

Avšak při zkouškách prováděných s AcOK spolu s dalšími sloučeninami byl pozorován určitý stupeň koroze povrchů cementu, proto se uvažovalo o přidání antikorozních látek do nemrznoucích směsí..
Na druhou stranu směs octanu draselného (CH3COOK) s mravenčanem draselným (HCOOK) je vynikající nemrznoucí směs a nevyžaduje antikorozní účinek.
Reference
- Baker, F.J. et al. (1976). Postupy barvení. Vodné koně. In Introduction to Medical Laboratory Technology (Páté vydání). Obnoveno ze sciencedirect.com.
- Hassan, A.A. et al. (2018). Indazoly: Syntéza a heterocyklizace vytvářející vazby. In Advances in Heterocyclic Chemistry. Obnoveno ze sciencedirect.com.
- NÁS. Národní lékařská knihovna. (2019). Octan draselný. Obnoveno z pubchem.ncbi.nlm.nih.gov.
- Das, A. a Alagirusamy, R. (2010). Přenos vlhkosti. Vysoušecí metoda v obráceném kelímku. Ve vědě v pohodlí oblečení. Obnoveno ze sciencedirect.com.
- Vargel, C. (2004). Karboxylové kyseliny a jejich deriváty. Octany. Koroze hliníku. Obnoveno ze sciencedirect.com.
- Cuevas, J. (2014). Techniky elektrofyziologického záznamu. Techniky intracelulárního záznamu. In Reference Module in Biomedical Sciences. Obnoveno ze sciencedirect.com.
- Fink, J.K. (2018). Poly (urethan) s. Recyklace. Solvolýza. In Reactive Polymers: Fundamentals and Applications (Third Edition). Obnoveno ze sciencedirect.com.
- Fong, W. a kol. (1997). Optimalizace produkce monoklonálních protilátek: kombinované účinky octanu draselného a perfúze v míchaném bioreaktoru nádrže. Cytotechnology 24: 47-54. Obnoveno z odkazu.springer.com.
- Danilov, V.P. et al. (2012). Nízkoteplotní činidla proti polevě ve vodných solných systémech obsahujících octany a mravenčany. Theoretical Foundations of Chemical Engineering, 2012, Vol 46, No. 5, pp. 528-535. Obnoveno z odkazu.springer.com.
- Fakeev, A.A. a kol. (2012). Výzkum a vývoj metody pro vysokou čistotu octanu draselného. Journal of Applied Chemistry, 2012, sv. 85, č. 12, str. 1807-1813. Obnoveno z odkazu.springer.com.



Zatím žádné komentáře