
Struktura terciárního alkoholu, vlastnosti, příklady
A terciární alkohol je skupina, ve které je hydroxylová skupina, OH, připojena k terciárnímu uhlíku. Jeho vzorec je i nadále ROH, stejně jako jiné alkoholy; ale je to snadno rozpoznatelné, protože OH je v molekulární struktuře blízko X. Podobně je jeho uhlíkový řetězec obvykle kratší a jeho molekulová hmotnost je vyšší..
Terciární alkohol má tedy tendenci být těžší, je více rozvětvený a je také nejméně reaktivní, pokud jde o oxidaci všech; to znamená, že jej nelze přeměnit na keton nebo karboxylovou kyselinu, jak je tomu u sekundárních a primárních alkoholů..
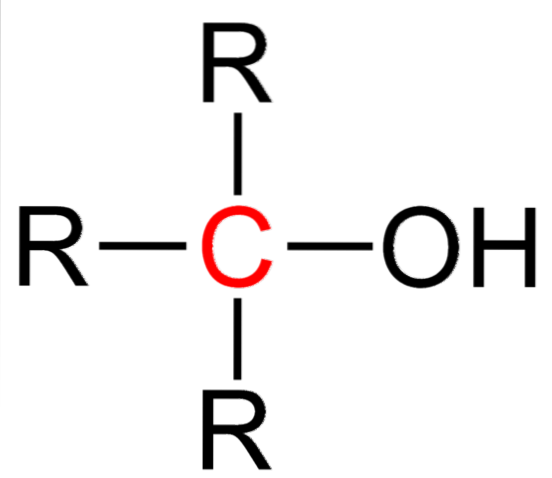
Obrázek výše ukazuje obecný strukturní vzorec pro terciární alkohol. Podle něj by mohl být napsán nový vzorec typu R.3COH, kde R může být alkylová nebo arylová skupina; methylová skupina, CH3, nebo krátký nebo dlouhý uhlíkový řetězec.
Pokud jsou tři skupiny R různé, centrální uhlík terciárního alkoholu bude chirální; to znamená, že alkohol bude vykazovat optickou aktivitu. Kvůli této skutečnosti jsou chirální terciární alkoholy zajímavé ve farmaceutickém průmyslu, protože tyto alkoholy se složitějšími strukturami jsou syntetizovány z ketonů s biologickou aktivitou..
Rejstřík článků
- 1 Struktura terciárního alkoholu
- 1.1 Sterická překážka
- 2 Vlastnosti
- 2.1 Fyzické
- 2.2 Kyselost
- 2.3 Reaktivita
- 3 Názvosloví
- 4 příklady
- 5 Reference
Struktura terciárního alkoholu
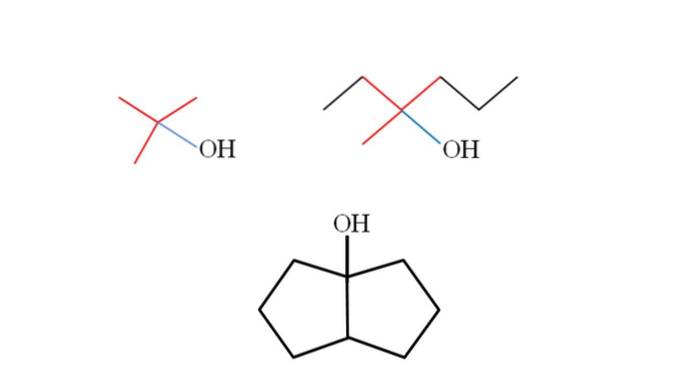
Zvažte struktury vyšších terciárních alkoholů a naučte se je rozpoznávat bez ohledu na to, o jakou sloučeninu jde. Uhlík vázaný na OH musí být také vázán na tři další uhlíky. Pokud se podíváte pozorně, všechny tři alkoholy toho dosáhnou..
První alkohol (vlevo) se skládá ze tří skupin CH3 navázaný na centrální uhlík, jehož vzorec by byl (CH3)3COH. Alkylová skupina (CH3)3C- je známý jako terc-butyl, je přítomen v mnoha terciárních alkoholech a lze jej snadno rozpoznat podle jeho tvaru T (červené T na obrázku).
Druhý alkohol (vpravo) má skupiny CH připojené k centrálnímu uhlíku3, CH3CHdva a CHdvaCHdvaCH3. Vzhledem k tomu, že tyto tři skupiny jsou různé, je alkohol chirální, a proto vykazuje optickou aktivitu. Zde není pozorováno T, ale X blízko OH (červená a modrá).
A ve třetím alkoholu (ten níže a bez barev) je OH spojen s jedním ze dvou uhlíků, které spojují dva cyklopentan. Tento alkohol nemá žádnou optickou aktivitu, protože dvě ze skupin připojených k centrálnímu uhlíku jsou identické. Stejně jako druhý alkohol, pokud se podíváte pozorně, najdete také X (spíše čtyřstěn).
Sterická překážka
Tři vyšší alkoholy mají něco společného více než X: centrální uhlík je stéricky bráněn; to znamená, že jej ve vesmíru obklopuje mnoho atomů. Okamžitým důsledkem toho je, že nukleofilům, kteří touží po kladných nábojích, je těžké se k tomuto uhlíku přiblížit..
Na druhou stranu, protože k centrálnímu uhlíku jsou vázány tři uhlíky, darují část hustoty elektronů, kterou od ní odečte elektronegativní atom kyslíku, a dále ji stabilizují proti těmto nukleofilním útokům. Terciární alkohol však může být substituován tvorbou karbokationtu.
Vlastnosti
Fyzický
Třetí alkoholy mají obecně vysoce rozvětvené struktury. Prvním důsledkem toho je, že je bráněno skupině OH, a proto má její dipólový moment menší účinek na sousední molekuly..
To má za následek slabší molekulární interakce ve srovnání s primárními a sekundárními alkoholy..
Zvažte například strukturní izomery butanolu:
CH3CHdvaCHdvaACH (n-butanol, Peb = 117 ° C)
(CH3)dvaCHdvaOH (isobutylalkohol, bp = 107 ° C)
CH3CHdvaCH (OH) CH3 (sek.butylalkohol, bp = 98 ° C)
(CH3)3COH (terc-butylalkohol, bp = 82 ° C)
Všimněte si, jak klesají body varu, když se izomer rozvětvuje.
Na začátku bylo zmíněno, že ve strukturách 3. alkoholů je pozorováno X, což samo o sobě naznačuje vysoké rozvětvení. Proto mají tyto alkoholy sklon k nižším bodům tání a / nebo bodu varu..
Trochu podobný je případ jeho mísitelnosti s vodou. Čím více bude bráněno OH, tím méně mísitelný bude 3. alkohol s vodou. Uvedená mísitelnost však klesá, čím delší je uhlíkový řetězec; V tomto případě je terciární butylalkohol rozpustnější a mísitelný s vodou než n-butanol.
Kyselost
Terciární alkoholy bývají ze všech nejméně kyselé. Důvody jsou četné a spolu souvisí. Stručně řečeno, záporný náboj odvozeného alkoxidu, RO-, pocítí silný odpor pro tři alkylové skupiny připojené k centrálnímu uhlíku, což oslabí anion.
Čím je anion nestabilnější, tím nižší je kyselost alkoholu.
Reaktivita
Třetí alkoholy nemohou podléhat oxidaci na ketony (R.dvaC = O) nebo aldehydy (RCHO) nebo karboxylové kyseliny (RCOOH). Za prvé, museli byste ztratit jeden nebo dva uhlíky (ve formě COdva) oxidovat, což snižuje jeho reaktivitu proti oxidaci; a na druhé straně postrádá vodík, který může ztratit, aby vytvořil další vazbu s kyslíkem.
Mohou však podléhat substituci a eliminaci (tvorba dvojné vazby, alkenu nebo olefinu).
Nomenklatura
Nomenklatura těchto alkoholů se neliší od ostatních. Existují běžná nebo tradiční jména a systematická jména, která se řídí IUPAC.
Pokud hlavní řetězec a jeho větve sestávají z uznané alkylové skupiny, používá se pro jeho tradiční název; není-li to možné, použije se nomenklatura IUPAC.
Zvažte například následující terciární alkohol:
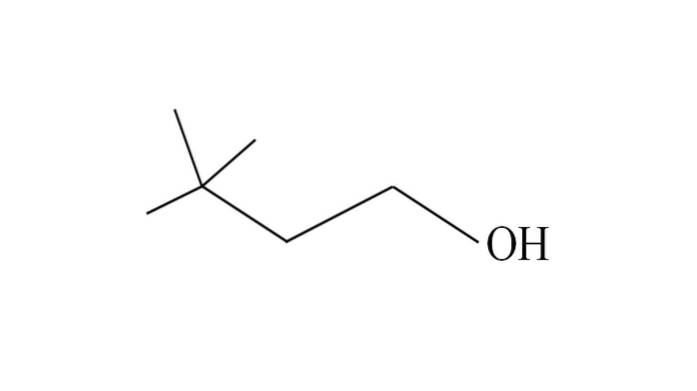
Uhlíky začínají být očíslovány zprava doleva. V C-3 existují dvě skupiny CH3 substituentů, a proto se tento alkohol jmenuje 3,3-dimethyl-1-butanol (hlavní řetězec má čtyři uhlíky).
Podobně celý řetězec a jeho větve sestávají z neohexylové skupiny; proto může být jeho tradičním názvem neohexylalkohol nebo neohexanol.
Příklady
Nakonec jsou zmíněny některé příklady terciárních alkoholů:
-2-methyl-2-propanol
-3-methyl-3-hexanol
-Bicyklo [3.3.0] oktan-1-ol
-2-methyl-2-butanol: CH3CHdvaCOH (CH3)dva
Na prvním obrázku jsou uvedeny vzorce prvních tří alkoholů.
Reference
- Carey F. (2008). Organická chemie. (Šesté vydání). Mc Graw Hill.
- Morrison, R. T. a Boyd, R, N. (1987). Organická chemie. (5. vydání). Redakční Addison-Wesley Interamericana.
- Graham Solomons T.W., Craig B.Fryhle. (2011). Organická chemie. Miny. (10. vydání.). Wiley plus.
- Gunawardena Gamini. (2016, 31. ledna). Terciární alkohol. Chemistry LibreTexts. Obnoveno z: chem.libretexts.org
- Ashenhurst James. (16. června 2010). Alkoholy (1) - nomenklatura a vlastnosti. Obnoveno z: masterorganicchemistry.com
- Clark J. (2015). Představujeme alkoholy. Obnoveno z: chemguide.co.uk
- Organická chemie. (s.f.). Jednotka 3. Alkoholy. [PDF]. Obnoveno z: sinorg.uji.es
- Nilanjana Majumdar. (3. března 2019). Syntéza chirálního terciárního alkoholu: významný vývoj. Obnoveno z: 2.chemistry.msu.edu


Zatím žádné komentáře