
Kalorimetrie, jaké studie a aplikace
The kalorimetrie je technika, která určuje změny kalorického obsahu systému spojené s chemickým nebo fyzikálním procesem. Je založen na měření teplotních změn, když systém absorbuje nebo vydává teplo. Kalorimetr je zařízení používané při reakcích, při nichž dochází k výměně tepla.
To, co je známé jako „šálek kávy“, je nejjednodušší forma tohoto typu zařízení. Prostřednictvím jeho použití se měří množství tepla zapojeného do reakcí prováděných za stálého tlaku ve vodném roztoku. Kalorimetr šálku na kávu se skládá z polystyrénové nádoby, která je umístěna v kádince..

Voda je umístěna do polystyrenové nádoby vybavené víkem ze stejného materiálu, které jí poskytuje určitý stupeň tepelné izolace. Nádoba má navíc teploměr a mechanické míchadlo..
Tento kalorimetr měří množství tepla, které je absorbováno nebo emitováno, v závislosti na tom, zda je reakce endotermická nebo exotermická, když reakce probíhá ve vodném roztoku. Systém, který má být studován, je tvořen reaktanty a produkty.
Rejstřík článků
- 1 Co studuje kalorimetrie?
- 2 Tepelná kapacita kalorimetru
- 2.1 Příklad použití kalorimetru k výpočtu měrného tepla
- 3 Kalorimetrické čerpadlo
- 4 typy kalorimetru
- 4.1 Izotermický titrační kalorimetr (CTI)
- 4.2 Diferenční skenovací kalorimetr
- 5 Aplikace
- 5.1 Použití izotermické titrační kalorimetrie
- 5.2 Použití diferenciální skenovací kalorimetrie
- 6 Reference
Co studuje kalorimetrie?
Kalorimetrie studuje vztah mezi tepelnou energií spojenou s chemickou reakcí a tím, jak se používá k určení jejích proměnných. Jejich aplikace v oblastech výzkumu ospravedlňují rozsah těchto metod.
Kalorická kapacita kalorimetru
Tato kapacita se vypočítá vydělením množství tepla absorbovaného kalorimetrem změnou teploty. Tato variace je produktem tepla, které je emitováno v exotermické reakci, které se rovná:
Množství tepla absorbovaného kalorimetrem + množství tepla absorbovaného roztokem
Změnu lze určit přidáním známého množství tepla měřením změny teploty. Pro toto stanovení kalorické kapacity se obvykle používá kyselina benzoová, protože je známo její spalné teplo (3 227 kJ / mol).
Kalorickou kapacitu lze také určit přidáním tepla pomocí elektrického proudu.
Příklad použití kalorimetru k výpočtu měrného tepla
95 g tyčinka kovu se zahřeje na 400 ° C a ihned se vezme do kalorimetru s 500 g vody, zpočátku na 20 ° C. Konečná teplota systému je 24 ° C. Vypočítejte měrné teplo kovu.
Δq = m x ce x Δt
V tomto výrazu:
Δq = změna zatížení.
m = hmotnost.
ce = měrné teplo.
Δt = kolísání teploty.
Teplo získané vodou se rovná teplu vydávanému z kovové tyče.
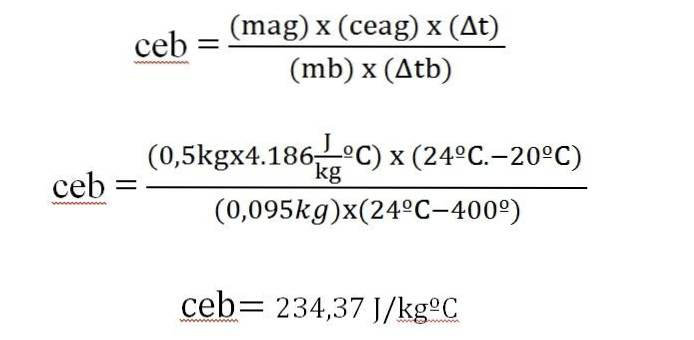
Tato hodnota je podobná té, která je uvedena v tabulce měrného tepla pro stříbro (234 J / kg ºC).
Jednou z aplikací kalorimetrie je tedy spolupráce při identifikaci materiálů.
Kalorimetrické čerpadlo
Skládá se z ocelové nádoby, známé jako čerpadlo, odolné vůči vysokým tlakům, které mohou vznikat během reakcí, ke kterým v této nádobě dochází; tento zásobník je připojen k zapalovacímu obvodu, aby se zahájily reakce.
Čerpadlo je ponořeno do velké nádoby s vodou, jejíž funkcí je absorbovat teplo, které je v čerpadle generováno během reakcí, čímž je malá teplotní odchylka. Nádoba na vodu je vybavena teploměrem a mechanickým míchadlem.
Změny energie se měří při téměř konstantním objemu a teplotě, takže se neprovádí žádná práce s reakcemi, které se vyskytují v čerpadle.
ΔE = q
ΔE je změna vnitřní energie v reakci a q teplo generované v této reakci.
Typy kalorimetru
Izotermický titrační kalorimetr (CTI)
Kalorimetr má dvě buňky: v jednom je umístěn vzorek a v druhém je referenční, obvykle voda.
Teplotní rozdíl, který je generován mezi buňkami - v důsledku reakce, která se vyskytuje ve vzorkovací buňce - je zrušen zpětnovazebním systémem, který vstřikuje teplo pro vyrovnání teplot buněk..
Tento typ kalorimetru umožňuje sledovat interakci mezi makromolekulami a jejich ligandy..
Diferenciální skenovací kalorimetr
Tento kalorimetr má dva články, jako je CTI, ale má zařízení, které umožňuje určovat teplotu a tepelné toky spojené se změnami materiálu jako funkci času.
Tato technika poskytuje informace o skládání proteinů a nukleových kyselin a jejich stabilizaci..
Aplikace

-Kalorimetrie umožňuje určit výměnu tepla, ke které dochází při chemické reakci, což umožňuje jasnější pochopení mechanismu tohoto.
-Stanovením měrného tepla materiálu poskytuje kalorimetrie data, která ho pomáhají identifikovat.
-Jelikož existuje přímá úměrnost mezi tepelnou změnou reakce a koncentrací reaktantů spolu se skutečností, že kalorimetrie nevyžaduje čiré vzorky, lze tuto techniku použít ke stanovení koncentrace látek přítomných ve složitých matricích..
-V oblasti chemického inženýrství se kalorimetrie používá v bezpečnostním procesu i v různých oblastech optimalizačního procesu, chemické reakce a v provozní jednotce..
Použití izotermické titrační kalorimetrie
-Spolupracuje při vytváření mechanismu působení enzymů i při jeho kinetice. Tato technika může měřit reakce mezi molekulami, určovat vazebnou afinitu, stechiometrii, entalpii a entropii v roztoku bez potřeby markerů..
-Posuzuje interakci nanočástic s proteiny a ve spojení s dalšími analytickými metodami je důležitým nástrojem pro zaznamenávání konformačních změn v proteinech.
-Má uplatnění při konzervování potravin a plodin.
-Pokud jde o konzervaci potravin, můžete určit jejich zhoršení a trvanlivost (mikrobiologická aktivita). Může porovnávat účinnost různých metod konzervace potravin a je schopen určit optimální dávku konzervačních látek i degradaci při kontrole balení.
-Pokud jde o zeleninové plodiny, můžete studovat klíčivost semen. Ve vodě a v přítomnosti kyslíku uvolňují teplo, které lze měřit izotermickým kalorimetrem. Prozkoumejte stáří a nesprávné skladování semen a studujte jejich rychlost růstu tváří v tvář kolísání teploty, pH nebo různých chemikálií.
-Nakonec můžete změřit biologickou aktivitu půd. Kromě toho dokáže detekovat nemoci.
Využití diferenciální skenovací kalorimetrie
-Spolu s izotermickou kalorimetrií bylo možné studovat interakci proteinů s jejich ligandy, alosterickou interakci, skládání proteinů a mechanismus jejich stabilizace..
-Teplo, které se uvolňuje nebo absorbuje během události molekulární vazby, lze přímo měřit.
-Diferenciální skenovací kalorimetrie je termodynamický nástroj pro přímé stanovení absorpce tepelné energie, ke které dochází ve vzorku. To umožňuje analyzovat faktory podílející se na stabilitě molekuly proteinu..
-Studuje také termodynamiku přechodu skládání nukleových kyselin. Tato technika umožňuje stanovení oxidační stability kyseliny linolové izolované a navázané na jiné lipidy.
-Tato technika se používá při kvantifikaci nanosolidů pro farmaceutické použití a při tepelné charakterizaci nanostrukturovaných lipidových transportérů..
Reference
- Whitten, K., Davis, R., Peck, M. a Stanley, G.. Chemie. (2008). 8. vydání. Cengage Learning Upravit.
- Rehak, N. N. a Young, D. S. (1978). Perspektivní aplikace kalorimetrie v klinické laboratoři. Clin. Chem. 24 (8): 1414-1419.
- Stossel, F. (1997). Aplikace reakční kalorimetrie v chemickém inženýrství. J. Therm. Anální. 49 (3): 1677-1688.
- Weber, P. C. a Salemme, F. R. (2003). Aplikace kalorimetrických metod při objevování léčiv a studiu proteinových interakcí. Curr. Opin. Struct. Biol. 13 (1): 115-121.
- Gill, P., Moghadem, T. a Ranjbar, B. (2010). Diferenční skenovací kalorimetrické techniky: aplikace v biologii a nanovědách. J. Biol. Tech. 21 (4): 167-193.
- Omanovic-Miklicanin, E., Manfield, I. a Wilkins, T. (2017). Aplikace izotermické titrační kalorimetrie při hodnocení interakcí protein-nanočástice. J. Therm. Anální. 127: 605-613.
- Konsorcium Community College pro pověření pro biologické vědy. (7. července 2014). Kalorimetr šálku kávy. [Postava]. Citováno dne 7. června 2018 z: commons.wikimedia.org


Zatím žádné komentáře