
Struktura kyanidinu, kde se nachází, přináší výhody
The kyanidin Je to chemická sloučenina patřící do skupiny antokyanů. Tyto bioaktivní sloučeniny mají schopnost snižovat oxidační poškození, stejně jako protizánětlivé a antimutagenní vlastnosti, a proto jsou zajímavé v různých farmakologických studiích..
Kromě toho mají antokyany vlastnosti přírodních ve vodě rozpustných barviv. Jsou odpovědné za červenou, modrou a fialovou pigmentaci rostlinných produktů, jako jsou ovoce, květiny, stonky, listy atd..
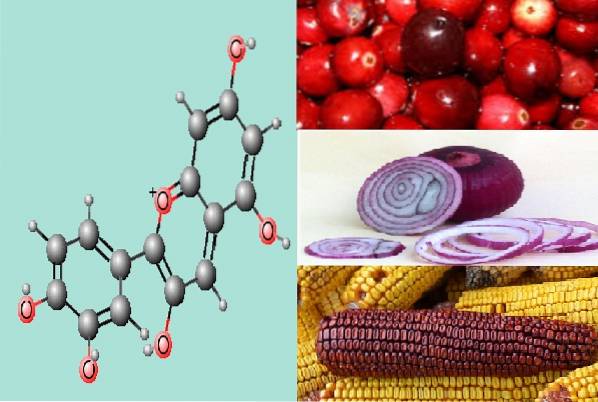
Kyanidin konkrétně vyvolává zbarvení plodů rostlin, jako je mexická purpurová kukuřice, fialové pigmentované červené zelí a nativní peruánské brambory, jejichž pigmenty jsou červené a fialové..
V současné době jsou antokyany v potravinářském průmyslu široce hodnoceny ve prospěch možné náhrady syntetických barviv v potravinách z důvodu jejich neškodnosti. To znamená, že nezpůsobují nepříznivé nebo škodlivé účinky na tělo.
V tomto smyslu je v některých zemích povoleno přidávání antiokyaninů jako potravinářských barviv, pokud jsou splněny specifické podmínky pro jejich použití..
Například v USA je povoleno pouze použití části, kterou lze z rostliny konzumovat, zatímco v Mexiku je její použití založeno na konkrétních potravinách, jako jsou klobásy, doplňky a některé nealkoholické nápoje..
Rejstřík článků
- 1 Chemická struktura
- 2 Kde se nachází?
- 3 Jak funguje cyanidin ke stanovení pH?
- 4 Další faktory, které mění vlastnosti kyanidinu
- 5 Výhody pro zdraví
- 6 Reference
Chemická struktura
Kyanidin je také známý pod názvem kyanidol a jeho molekulární vzorec je: C.patnáctHjedenáctNEBO6.
Jeho chemická struktura, stejně jako ostatní antokyany (pelargonidin, malvidin, petunidin, peonidin, delphinidin, mimo jiné), se skládá z flavonového jádra, které někteří autoři definují jako kruh C a dva aromatické kruhy (A a B).
Přítomnost těchto tří prstenů s dvojnými vazbami je to, co dává antokyanům jejich pigmentaci. Podobně je definice typu antokyaninu způsobena řadou substituentů v poloze uhlíku 3, 4 a 5 kruhu B.
Ve struktuře kyanidinu jsou konkrétně uhlíky v kruhu A a C číslovány od 2 do 8, zatímco uhlíky v kruhu B jdou od 2 do 6. Proto, když je hydroxylový radikál umístěn v kruhu B, uhlík 3 a na uhlíku 5 a vodík, tato změna odlišuje kyanidin od zbytku antokyanů.
Kde se to nachází?
Kyanidin je v přírodě převládající. Některé potraviny, jako je ovoce, zelenina a zelenina, mají vysoký obsah této sloučeniny.
To potvrzují některé studie, ve kterých nalezly různé deriváty kyanidinu, včetně kyanidin-3-glukosidu, jako nejběžnější derivát, většinou obsažený v třešní a malinách..
Vzhledem k tomu, že kyanidin-3-soforosid, kyanidin 3-glukorutinosid, kyanidin 3-rutinosid, kyanidin-3-arabinosid, kyanidin-3-malonyl-glukosid a kyanidin-3-malonylarabinosid jsou méně časté; ačkoli deriváty malonilu jsou přítomny ve větším množství v červené cibuli.
Podobně byl vysoký obsah kyanidinu hlášen u jahod, borůvek, hroznů, ostružin, ostružin, švestek, jablek a pitahaya (dračí ovoce). Je třeba poznamenat, že nejvyšší koncentrace kyanidinu se nachází v ovocných slupkách.
Kromě toho byla jeho přítomnost ověřena v mexické purpurové obilné zrně, rajčatovém stromě, v plodech kolumbijského koroza (kyanidin-3-glukosid a kyanidin 3-rutinosid) a v barvených původních bramborách: krev býka (cyanidin - 3-glukosid) a wenq'os, oba původem z Peru.
Jak funguje cyanidin pro stanovení pH?
Vzhledem ke svým vlastnostem jako barvivo a jeho citlivosti na kolísání pH se kyanidin používá jako indikátor při acidobazických titracích. Obvykle se získává z červeného zelí nebo se také nazývá fialové zelí (Brasica oleracea varianta capitata f. rubra).

Za kyselých podmínek pH, tj. S poklesem pH (≤ 3), změní zelné listy barvu a zčervená. To je způsobeno převahou flavilliového kationtu ve struktuře kyanidinu..
Zatímco při neutrálním pH (7) si zelné listy udržují svůj modrofialový pigment, protože ve struktuře kyanidinu dochází k deprotonaci a tvoří se modrá chinoidní báze..
Naopak, pokud jsou podmínky pH zásadité, to znamená, že se pH zvýší z 8 na 14, barva zelných listů se ionizací kyanidinu změní na zelené, žluté až bezbarvé tóny a vytvoří molekulu zvanou chalkon.
Tato molekula je považována za konečný produkt degradace kyanidinu, proto se nemůže znovu regenerovat na kyanidin..
Nedávné studie naznačují jeho použití v chemických laboratorních postupech jako náhradu za konvenční indikátory pH. Účelem by bylo snížit znečišťující odpad pro životní prostředí.
Další faktory, které mění vlastnosti kyanidinu
Je třeba poznamenat, že kyanidin ztrácí svou barevnou vlastnost zahříváním roztoku, čímž se stává bezbarvý. Je to proto, že tato sloučenina je při vysokých teplotách nestabilní..
Kromě toho jsou dalšími faktory, jako jsou: světlo, kyslík, aktivita vody, mimo jiné hlavní nevýhody jejich účinného začlenění do potravin..
Z tohoto důvodu je třeba vzít v úvahu, že postupy vaření v některých potravinách upřednostňují ztrátu jejich antioxidační kapacity, jako je tomu v případě nativních peruánských brambor wenq'os, které při smažení snižují obsah kyanidinu..
Studie, jako jsou Ballesteros a Díaz 2017, jsou však v tomto ohledu povzbudivé, protože ukázaly, že konzervace v hydrogensiřičitanu sodném při 1% w / v při teplotě 4 ° C může zlepšit stabilitu a trvanlivost tohoto indikátoru a prodloužit tímto způsobem jeho životnost.
Rovněž bylo testováno jeho zabudování do mléčných výrobků při pH < 3 y almacenados a bajas temperaturas por corto tiempo, con el fin de conservar la estabilidad de la molécula y por ende sus propiedades.
Výhody zdraví
Ve skupině antokyanů je nejdůležitější kyanidin, a to díky své široké distribuci v nejrůznějších druzích ovoce, kromě toho, že se ukázalo, že jeho spotřeba je bezpečná a účinná při inhibici reaktivních forem kyslíku a prevenci oxidačního poškození v různé buňky.
Kyanidin proto vyniká svým mimořádným antioxidačním potenciálem, díky němuž je možným biofarmakem v preventivní terapii množení rakovinných buněk (rakovina tlustého střeva a leukémie), mutací a nádorů..
Kromě toho se mu připisují protizánětlivé vlastnosti. Nakonec může snížit kardiovaskulární onemocnění, obezitu a cukrovku.
Reference
- Salinas Y, García C, Coutiño B, Vidal V. Variabilita obsahu a typů antokyanů v modro / fialových zrnech populací mexické kukuřice. fytotec. mex. 2013; 36 (Suppl): 285-294. K dispozici na: scielo.org.
- Castañeda-Sánchez A, Guerrero-Beltrán J. Pigmenty v červeném ovoci a zelenině: antokyany. Vybraná témata potravinářského inženýrství 2015; 9: 25–33. Dostupné na: web.udlap.mx.
- Aguilera-Otíz M, Reza-Vargas M, Chew-Madinaveita R, Meza-Velázquez J. Funkční vlastnosti antokyanů. 2011; 13 (2), 16-22. Dostupné na: biotecnia.unison
- Torres A. Fyzikální, chemická a bioaktivní charakterizace buničiny rajčat zralého stromu (Cyphomandra betacea) (Cav.) Sendt. ALAN. 2012; 62 (4): 381-388. K dispozici na: scielo.org/
- Rojano B, Cristina I, Cortes B. Stabilita hodnot antokyanů a absorpční kapacity kyslíkových radikálů (ORAC) vodných extraktů koroza (Bactris guineensis). Rev Cubana Plant Med. 2012; 17 (3): 244-255. Dostupné na: sld.cu/scielo
- Barragan M, Aro J. Stanovení účinku varných procesů u nativních pigmentovaných brambor (Solanum tuberosum spp. andigena) na jejich bioaktivní sloučeniny. vyšetřován. Altoandin. 2017; 19 (1): 47-52. K dispozici na: scielo.org.
- Heredia-Avalos S. Překvapivé chemické zkušenosti s domácími indikátory pH. Časopis Eureka o výuce přírodních věd a šíření. 2006; 3 (1): 89-103. Dostupné na: redalyc.org/
- Soto A, Castaño T. Studie enkapsulace antokyanů technikou sol-gel pro její použití jako potravinářského barviva [diplomová práce] Autonomní univerzita v Querétaro, Querétaro; 2018. Dostupné na: ri-ng.uaq.mx
- Ballesteros F, Díaz B, Herrera H, Moreno R. Anthocyanin jako náhrada syntetických indikátorů pH: krok k zeleným produktům [Environmental Engineering Thesis], Universidad de la Costa CUC, Barranquilla, Kolumbie; 2017.



Zatím žádné komentáře