
Struktura, funkce a nemoci kyseliny sialové
The kyseliny sialové jsou to monosacharidy devíti atomů uhlíku. Patří do rodiny derivátů neuraminových kyselin (kyselina 5-amino-3,5-dideoxy-D-glycero-D-galakto-nonulosonová) a jsou v přírodě široce distribuovány, zejména v živočišné říši.
Obvykle se nevyskytují jako volné molekuly, ale jsou spojeny α-glukosidovými vazbami s molekulami uhlohydrátů nebo jinými molekulami kyseliny sialové a poté mohou zaujímat koncové nebo vnitřní polohy v lineárním uhlovodíkovém řetězci.
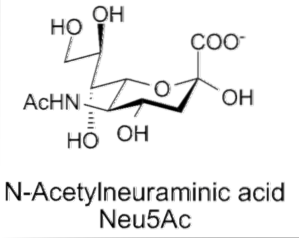
Termín „kyselina sialová“ poprvé vytvořil Gunnar Blix v roce 1957, i když předchozí zprávy jiných vědců naznačují, že jeho objev se datuje o deset nebo dva roky dříve, kdy byly popsány jako součást sialo mucinových glykoproteinů a sialo sialo sialo singolipidů (gangliosidy) ).
Kyseliny sialové jsou přítomny ve většině přírodních království. Byly detekovány u některých virů, patogenních bakterií, prvoků, korýšů, plochých červů, hmyzu a obratlovců, jako jsou ryby, obojživelníci, ptáci a savci. Naopak nebyly nalezeny v houbách, řasách ani rostlinách..
Rejstřík článků
- 1 Struktura
- 2 funkce
- 2.1 Úloha v procesech adheze buněk
- 2.2 Role v životnosti složek krevních buněk
- 2.3 Role v imunitním systému
- 2.4 Další funkce
- 3 Nemoci
- 4 Odkazy
Struktura
Kyseliny sialové se vyskytují hlavně v terminální části povrchových glykoproteinů a glykolipidů, což těmto glykokonjugátům poskytuje velkou rozmanitost. Diferenciální "sialylační" vzorce jsou produkty exprese tkáňově specifických glykosyltransferáz (sialyltransferáz).
Strukturálně patří sialové kyseliny do rodiny asi 40 přírodních derivátů kyseliny neuraminové, které jsou N-acylované, což vede ke dvěma „mateřským“ strukturám: kyselina N-acetylneuraminová (Neu5Ac) nebo kyselina N-glykolyluraminová (Neu5Gc).
Mezi jeho strukturní vlastnosti patří přítomnost aminoskupiny (kterou lze modifikovat) v poloze 5 a karboxylové skupiny v poloze 1, kterou lze ionizovat při fyziologickém pH. Deoxygenovaný uhlík C-3 a molekula glycerolu v poloze C-6.
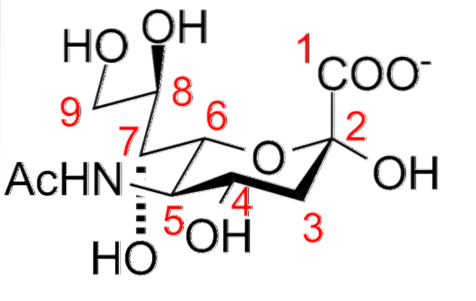
Mnoho derivátů vzniká substitucí hydroxylových skupin v polohách C-4, C-7, C-8 a C-9 acetylovými, glykolovými, laktylovými, methylovými, sulfátovými a fosfátovými částmi; stejně jako zavedení dvojných vazeb mezi C-2 a C-3.
V lineární koncové poloze připojení části kyseliny sialové k oligosacharidovému řetězci zahrnuje a-glukosidovou vazbu mezi hydroxylovou skupinou C-2 anomerního uhlíku kyseliny sialové a hydroxylovými skupinami uhlíků C-3, C 4 nebo C-6 monosacharidové části.
Tyto vazby mohou být mezi zbytky galaktózy, N-acetylglukosaminem, N-acetylgalaktosaminem a v některých jedinečných gangliosidech glukózou. Mohou se vyskytovat prostřednictvím N-glykosidových nebo O-glykosidových vazeb.
Funkce
Předpokládá se, že kyselina sialová pomáhá parazitickým organismům přežít v hostitelském organismu; příklady jsou savčí patogeny, které produkují enzymy metabolismu kyseliny sialové (sialidázy nebo N-acetylneuraminové lyázy).
Neexistuje žádný druh savce, u kterého by nebyla přítomna kyselina sialová jako součást glykoproteinů obecně, sérových glykoproteinů, sliznice, jako součást struktur buněčného povrchu nebo jako součást komplexních sacharidů..
Byly nalezeny v kyselých oligosacharidech v mléce a mlezivu lidí, skotu, ovcí, psů a prasat a také jako součást moči potkanů a lidí..
Role v procesech adheze buněk
Glykokonjugáty s částmi kyseliny sialové hrají důležitou roli v procesech výměny informací mezi sousedními buňkami a mezi buňkami a jejich prostředím..
Přítomnost kyseliny sialové v buněčných membránách přispívá k vytvoření negativního náboje na povrchu, což má pozitivní důsledky v některých událostech elektrostatického odpuzování mezi buňkami a některými molekulami..
Kromě toho záporný náboj dává sialovým kyselinám v membráně funkci při transportu kladně nabitých iontů..
Bylo popsáno, že navázání endotelu a epitelu na glomerulární bazální membránu usnadňuje kyselina sialová, což také ovlivňuje kontakt mezi těmito buňkami..
Role v životnosti složek krevních buněk
Kyselina sialová má důležité funkce jako součást glykoforinu A v plazmatické membráně erytrocytů. Některé studie ukázaly, že obsah kyseliny sialové je nepřímo úměrný stáří těchto buněk.
Erytrocyty ošetřené neuraminidázovými enzymy, které jsou zodpovědné za degradaci kyseliny sialové, drasticky snižují svůj poločas v krevním řečišti ze 120 dnů na několik hodin. Stejný případ byl pozorován u destiček.
Trombocyty ztrácejí svou adhezní a agregační kapacitu v nepřítomnosti kyseliny sialové v jejich povrchových proteinech. V lymfocytech hraje kyselina sialová také důležitou roli v procesech adheze a rozpoznávání buněk, jakož i v interakci s povrchovými receptory..
Funkce imunitního systému
Imunitní systém je schopen rozlišit mezi svými vlastními nebo napadajícími strukturami na základě rozpoznání vzorců kyseliny sialové přítomných v membránách.
Kyselina sialová, stejně jako enzymy neuraminidáza a sialyltransferáza, mají důležité regulační vlastnosti. Koncové části kyseliny sialové v glykokonjugátech s plazmatickou membránou mají maskování nebo jsou membránovými receptory..
Navíc různí autoři upozornili na možnost, že kyselina sialová má antigenní funkce, ale zatím to není s jistotou známo. Maskovací funkce zbytků kyseliny sialové jsou však při regulaci buněk velmi důležité..
Maskování může mít přímou nebo nepřímou ochrannou roli, v závislosti na tom, zda část kyseliny sialové přímo pokrývá zbytek antigenního uhlohydrátu, nebo zda je to kyselina sialová v sousedním glykokonjugátu, který maskuje část antigenu..
Některé protilátky obsahují zbytky Neu5Ac, které vykazují vlastnosti neutralizující viry, protože tyto imunoglobuliny jsou schopné zabránit adhezi virů pouze na konjugované (glykokonjugáty s částmi kyseliny sialové) na buněčné membráně.
Další funkce
Ve střevním traktu hrají kyseliny sialové stejně důležitou roli, protože jsou součástí mucinů, které mají lubrikační a ochranné vlastnosti, nezbytné pro celý organismus..
Kyseliny sialové jsou dále přítomny také v membránách bronchiálních, žaludečních a střevních epiteliálních buněk, kde se účastní transportu, sekrece a dalších metabolických procesů..
Nemoci
Je známo, že četné nemoci zahrnují abnormality v metabolismu kyseliny sialové a ty jsou známé jako sialidóza. Mezi nejvýznamnější patří sialurie a Sallova choroba, které se vyznačují vylučováním močí s velkým množstvím volných kyselin sialových..
Další nemoci imunologického řádu mají co do činění se změnami anabolických a katabolických enzymů souvisejících s metabolismem kyseliny sialové, které způsobují aberantní akumulaci glykokonjugátů s částmi kyseliny sialové..
Jsou také známa některá onemocnění související s krevními faktory, jako je trombocytopenie, která spočívá ve snížení hladiny trombocytů v krvi, pravděpodobně způsobené nedostatkem kyseliny sialové v membráně..
Von Willebrandova choroba odpovídá defektu schopnosti trombocytů adherovat na subendoteliální membránové glykokonjugáty stěny cév, způsobené nedostatkem nebo nedostatkem glykosylace nebo sialylace.
Glanzmannova trombastenie je další vrozená porucha agregace trombocytů, jejíž kořenem je přítomnost defektních glykoproteinů v membráně trombocytů. Ukázalo se, že vady těchto glykoproteinů jsou spojeny se sníženým obsahem Neu5Ac.
Reference
- Clayden, J., Greeves, N., Warren, S., & Wothers, P. (2001). Organická chemie (1. vyd.). New York: Oxford University Press.
- Demchenko, A. V. (2008). Příručka chemické glykosylace: Pokroky ve stereoselektivitě a terapeutické relevanci. Wiley-VCH.
- Rosenberg, A. (1995). Biologie sialových kyselin. New York: Springer Science + Business Media, LLC.
- Schauer, R. (1982). Kyseliny sialové: chemie, metabolismus a funkce. Springer-Verlag Wien New York.
- Traving, C., & Schauer, R. (1998). Struktura, funkce a metabolismus sialových kyselin. CMLS buněčné a molekulární biologické vědy, 54, 1330-1349.


Zatím žádné komentáře