
Kondenzovaný vzorec, co to je a příklady (metan, etan, glukóza ...)
The kondenzovaný vzorec jedná se o čistě textovou reprezentaci molekuly, ve které jsou odkazy vynechány. Jeho účelem je umožnit vědět, jaké je uspořádání atomů. Lineární nebo rozvětvené molekuly mají obecně kondenzované vzorce, s výjimkou cyklických nebo vysoce rozvětvených..
V organické chemii často panuje zmatek, jaký je rozdíl mezi tímto vzorcem a molekulárním. Ve skutečnosti je běžné je najít jako synonyma. Mezitím se v anorganické chemii více používají molekulární vzorce, protože ve většině případů přesně popisují kovalentní sloučeniny; jako voda, HdvaNEBO.
Rejstřík článků
- 1 Co je to kondenzovaný vzorec?
- 2 Příklady
- 2,1 metan
- 2.2 Ethan
- 2.3 Glukóza a fruktóza
- 2.4 Butan
- 2.5 Ethanol
- 2.6 Pentan
- 2,7 oktanu
- 2.8 Cyklohexan
- 2,9 aceton
- 2.10 Kyselina octová
- 3 Obecný komentář
- 4 Odkazy
Co je to kondenzovaný vzorec?
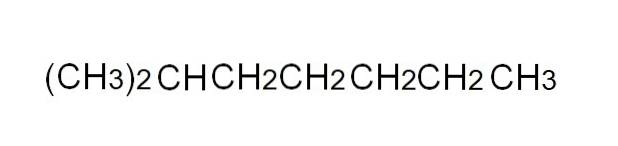
Abychom to pohodlněji definovali, je kondenzovaný vzorec zjednodušeným vyjádřením částečně roztaženého vzorce. Není nutné psát jednotlivé odkazy, ani nemusí obsahovat více než jeden řádek v textu. Například 2-methylheptan, rozvětvený alkan, může být zastoupen ve stejném řádku jako na obrázku výše.
Kondenzované vzorce jsou užitečné pro reprezentaci některých molekul, aniž byste je museli kreslit. To je vynikající při psaní chemických rovnic, kde nejsou zahrnuty vysoce rozvětvené nebo cyklické molekuly. Bude zřejmé, že tyto vzorce používají závorky k dalšímu zjednodušení reprezentace molekuly.
Příklady
Metan
Metan je jediná chemická sloučenina, která má jediný vzorec: CH4. To odpovídá empirickému, molekulárnímu, kondenzovanému a částečně vyvinutému současně. Proto mnohokrát lidé, aby se vyhnuli záměně mezi všemi těmito pojmy, raději jednoduše a nepřesně odkazují na „chemický vzorec“ sloučeniny.
Etan
Ethan má molekulární vzorec C.dvaH6. Kondenzovaným vzorcem je místo toho CH3CH3. Všimněte si, že vazby C-C a C-H jsou vynechány. Hlavní myšlenkou je být schopen psát vzorec, jako by to bylo „slovo“, aniž byste museli kreslit čáry nebo kreslit struktury.
Podle definice je molekulární vzorec CdvaH6 a ne CH3CH3; U jednoduchých molekul se však k výměně používají oba vzorce, i když je to stále nesprávné. Jedná se o rozpor mezi různými zdroji, kde zjevně neexistují v tomto ohledu žádná konkrétní pravidla..
Glukóza a fruktóza
Zde je příklad, kdy je okamžitě pozorována chyba, když se chce vyměnit molekulární vzorec za kondenzovaný.
Sladký pár, glukóza a fruktóza, mají stejný molekulární vzorec: C6H12NEBO6, a proto to neslouží k jejich odlišení. Naproti tomu strukturní a polorozvinuté vzorce vizuálně stanoví, že se jedná o různé molekuly.
Ani glukóza, ani fruktóza však nemají kondenzovaný vzorec. Je to proto, že bez ohledu na to, jaké je jejich zobrazení nebo projekce, jejich struktury nelze zapsat na stejný řádek; nebo alespoň způsobem, který je v očích čtenáře příjemný a jednoduchý.
Butan
Butan má molekulární vzorec C.4H10. Má dva izomery: lineární, n-butan a rozvětvený 2-methylpropan. Oba mohou být reprezentovány jejich kondenzovanými vzorci. The n-butan je CH3CHdvaCHdvaCH3 nebo CH3(CHdva)dvaCH3, a 2-methylpropan je CH3CH (CH3)dva nebo (CH3)3CH.
Ve 2-methylpropanu máme skupinu CH obklopenou třemi CH3. Jeho dva vzorce jsou platné a pro zvýraznění větví se používají závorky, dolní index je indikátorem toho, kolik skupin tvoří uvedenou větev.
Ethanol
Ethanol má kondenzovaný vzorec CH3CHdvaACH. Všimněte si, jak blízko se podobá svému částečně vyvinutému vzorci: CH3-CHdva-ACH. Totéž se děje s propanolem, CH3CHdvaCHdvaOh n-butanol, CH3CHdvaCHdvaCHdvaOH a se všemi ostatními alkoholy.
Pokud mají větev, bude to uvedeno v závorkách napravo od atomu, ke kterému je připojena. Například 2-methylbutanol lze psát jako: CH3CHdvaCH (CH3) CHdvaACH. Všimněte si, že pro mnoho molekul je stále pohodlnější uchýlit se ke strukturnímu nebo částečně vyvinutému vzorci.
Pentan
Lineární izomer pentanu, n-pentan, lze snadno vyjádřit jeho kondenzovaným vzorcem: CH3CHdvaCHdvaCHdvaCH3. Tento vzorec lze také zjednodušit pomocí závorek: CH3(CHdva)3CH3, což naznačuje, že mezi dvěma CH3 jsou tři CHdva.
Další dva izomery pentanu jsou však o něco složitější: CH3CHdvaCH (CH3)dva, pro 2-methylbutan a C (CH3)4 pro 2,2-dimethylpropan nebo neopentan. Všimněte si, že atom uhlíku nalevo od závorky je ten, který tvoří vazby se substituenty nebo větvemi..
Oktan
Lineární izomer oktanu, n-oktan, vzhledem ke své délce je nyní vhodné představovat jeho kondenzovaný vzorec jako CH3(CHdva)6CH3. Právě v tomto bodě by mělo být něco jasného o kondenzovaných vzorcích: snaží se ušetřit čas při reprezentaci molekul nebo sloučenin, aniž by museli tolik psát na papír.
Cyklohexan
Případ cyklohexanu je podobný případu glukózy a fruktózy: formálně mu chybí kondenzovaný vzorec, protože se jedná o cyklickou sloučeninu. Jedním ze způsobů, jak to zkusit reprezentovat, by bylo: (CHdva)6, což naznačuje, že šest CH skupindva musí být spojeny, což je možné, pouze pokud jsou uzavřeny v šestihranném kruhu. Je však lepší prsten nakreslit.
Aceton
Aceton má tu zvláštnost, že má karbonylovou skupinu, C = O. Proto, abychom napsali jeho zhuštěný vzorec, máme tři možnosti: (CH3)dvaCO, CH3C (O) CH3 nebo CH3(C = O) CH3.
Ve skutečnosti je ve větších molekulách karbonylová skupina obvykle reprezentována jako (O), s přihlédnutím k tomu, že atom uhlíku nalevo je ten, který tvoří dvojnou vazbu s kyslíkem, C = O.
Octová kyselina
Kondenzovaným vzorcem kyseliny octové je CH3COOH nebo CH3COdvaH. Objevuje se zde důležitý bod: funkční skupiny napsané na stejném řádku jsou součástí kondenzovaného vzorce. To byl případ ethanolu a acetonu a platí to také pro thioly (-SH), aldehydy (-CHO), estery (-COdvaR nebo -COOR) a aminy (-NHdva).
Obecný komentář
Mezi molekulárními a kondenzovanými formulemi dochází k velké záměně. Možná je to proto, že tyto reprezentace samotné již poskytují hrubý obraz molekuly, a proto si myslíme, že se jedná o molekulární vzorec.
Stejně tak vzorce jako C.6H12NEBO6 jsou také považovány za kondenzované, protože v nich je to zjednodušené, molekula je „kondenzována“ na atomy a indexy. Proto je běžné vidět, jak jsou tyto dva vzorce uvedeny, jako by šlo o synonyma.
V mnoha zdrojích, včetně článků na Wikipedii, se výrazy „chemický vzorec“ používají k označení molekuly (typ C6H12NEBO6 a další) a „vzorec“ označuje kondenzovaný.
Reference
- Whitten, Davis, Peck a Stanley. (2008). Chemie. (8. vydání). Učení CENGAGE.
- Helmenstine, Anne Marie, Ph.D. (18. listopadu 2019). Zhuštěná definice vzorce v chemii. Obnoveno z: thoughtco.com
- James Ashenhurst. (11. prosince 2019). Kondenzované vzorce: dešifrování, co znamenají závorky. Mistr v organické chemii. Obnoveno z: masterorganicchemistry.com
- Společné inženýrství. (2. května 2016). Empirický, strukturální a kondenzovaný vzorec. Obnoveno z: quimiotecablog.wordpress.com
- Úvod do chemie: Obecná, organická a biologická. (s.f.). Zhuštěné strukturní a lineární vzorce. Obnoveno z: 2012books.lardbucket.org



Zatím žádné komentáře