
Subatomární částice a jejich vlastnosti

The subatomární částice Jsou menší než atom a nacházejí se v přírodě, téměř všechny tvoří jeho součást. Známe dobře ty hlavní a nejstabilnější, kterými jsou elektron, proton a neutron..
Celá hmota se skládá z těchto částic, i když existují i jiné, i když jejich existence byla dlouho ignorována. První atomové modely pocházející z několika století před Kristem předpokládaly, že atomy jsou nedělitelné, něco jako kuličky, které při určitém spojení vedly k vzniku různých prvků.
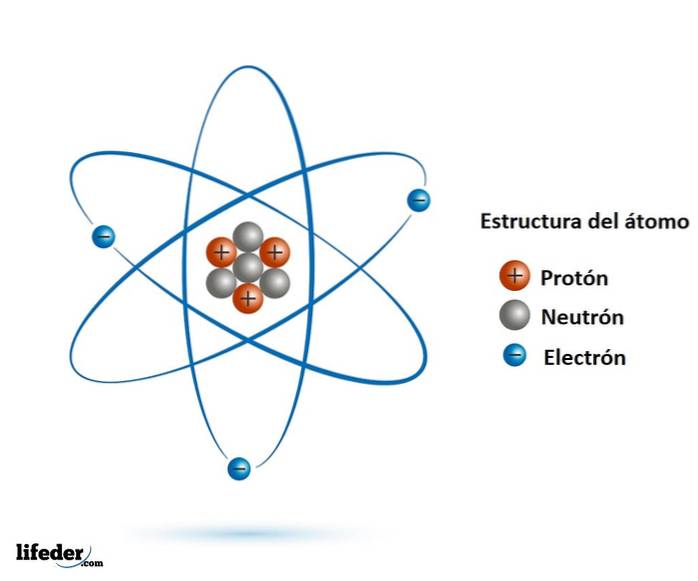
Když vyšlo najevo, že tomu tak není, díky objevům elektronu v 19. století a atomového jádra na počátku 20. století si vědci říkali, zda mají tyto částice vnitřní strukturu.
Ukázalo se, že ano, jak proton, tak neutron jsou částice složené z ještě menších, které nemají vnitřní strukturu: jsou to elementární částice.
Proto se subatomární částice dělí na:
- Složené částice.
- Elementární částice.
Elementární částice jsou kvarky, gluony a leptony. Kvarky a gluony tvoří protony a neutrony, zatímco elektron, elementární částice, je lepton.
Rejstřík článků
- 1 Objev subatomárních částic
- 1.1 Atomové jádro: protony a neutrony
- 2 Hlavní subatomární částice
- 2.1 Elektron
- 2.2 Proton
- 2.3 Neutron
- 2.4 Kvarky
- 3 Další částice
- 4 Odkazy
Objev subatomárních částic
Objevy subatomárních částic začaly v 19. století a jako první byl nalezen elektron.
V roce 1890 byli fyzici velmi zaneprázdněni studiem záření a přenosu elektromagnetických vln. J. J. Thomson byl jedním z nich a provedl řadu experimentů s trubicí, která měla odstraněný vzduch a připojenou dvojicí elektrod..

Když bylo aplikováno napětí, byly produkovány záhadné paprsky, nazývané katodové paprsky, jejichž povaha nebyla známa, dokud J. J. Thomson (1856-1940) nezjistil, že se skládají z proudu záporně nabitých částic.
Thomson získal podíl mezi nábojem a hmotou těchto částic: 1,76 x 108 C / g, kde C znamená coulomb, jednotka pro elektrický náboj v mezinárodním systému jednotek a g je gram.
A zjistil dvě velmi důležité věci, první, že hmotnost částic byla extrémně malá, a druhá, že tato hodnota byla pro všechny stejná, bez ohledu na to, z čeho jsou elektrody vyrobeny..
Hodnotu náboje zjistil krátce poté, počátkem 20. století, americký fyzik Robert Millikan (1868-1953) a jeho spolupracovníci, díky experimentu kapka oleje.
Atomové jádro: protony a neutrony
Na konci 19. století objevil Henri Becquerel (1852-1908) fenomén přirozené radioaktivity, který zaujal další fyziky jako Marie a Pierre Curie, stejně jako Novozélanďan Ernest Rutherford..
Ten našel tři různé typy záření ze vzorků uranu, známého radioaktivního prvku. Pojmenoval je prvními třemi písmeny řecké abecedy: α, β a γ.
Rutherfordovy rozptylové experimenty

Pomocí vysoce energetických, pozitivně nabitých částic α bombardoval Rutherford tenké zlaté fólie a zjistil, že podle očekávání většina částic alfa prošla fóliemi bez problémů.
Je ale zvědavé, že malý zlomek částic byl vychýlen a několik se dokonce odrazilo v opačném směru. Ten druhý byl nepředstavitelný, protože jak tvrdil Rutherford, bylo to jako střílet z pušky na tenký kapesník a sledovat, jak se kulky vracejí..
Důvodem, proč jsou částice α vychýleny, je to, že uvnitř listu je něco, co je odpuzuje, a proto musí být kladně nabité. Je to atomové jádro, malé velikosti, ale obsahující téměř veškerou hmotnost atomu.
Objev neutronu

Hledání neutronu trvalo o něco déle a jeho příčinou byl anglický fyzik James Chadwick (1891-1974), student Rutherfordu. Rutherford sám navrhl existenci nenabité částice v jádru, aby vysvětlil, proč se nerozpadá kvůli elektrostatickému odpuzování.
Chadwickovy experimenty odhalily v roce 1932 existenci částice hmoty velmi podobné té protonové, ale bez náboje. Proto jej nazývali neutronem a společně s protonem jsou základními složkami atomového jádra.
Hlavní subatomární částice
Obecně se subatomární částice vyznačují tím, že mají:
- Hmotnost.
- Elektrický náboj.
- Roztočit.
Spin je kvalita analogická rotaci kolem osy, ale svou povahou zcela kvantová. A na druhé straně existují částice s nábojem a hmotností 0, jako je foton.
Elektron
Elektron je stabilní subatomární částice, záporně nabitá a patřící do skupiny leptonů, která má nejnižší hmotnost. Je to podstatná součást atomu, může však existovat izolovaně od něj ve formě volné elektrony.
Ve skutečnosti se jedná o nejmenší elektrický náboj, který lze v přírodě nalézt, takže jakýkoli jiný náboj je násobkem elektronu podle principu kvantizace náboje..
Jeho hlavní vlastnosti jsou:
- Hmotnost: 9,1 x 10-31 kg
- Zatížení: e = -1,6 x 10-19 C
- Točení: ± ½
- Antičástice: pozitron.
Elektron je zodpovědný za tvorbu chemických vazeb, jakož i elektrického a tepelného vedení. A díky kvantové mechanice víme, že elektron má dvojí chování: vlnu a částice současně.
Proton
Je to elektricky nabitá částice, jejíž náboj je stejné velikosti jako náboj elektronu, ale s opačným znaménkem..
Proton není elementární částice jako elektron, ale skládá se ze tří kvarků spojených gluony a je mnohem hmotnější než elektron.
Na rozdíl od toho je proton omezen na atomové jádro a jeho množství určuje, o jaký prvek jde, a také o jeho vlastnostech..
- Hmotnost: 1672 x 10-27 kg
- Poplatek: e = +1,6 x 10-19 C
- Točení: ½
- Antičástice: antiproton.
Neutron
Neutron spolu s protonem tvoří atomové jádro a je také složen ze tří kvarků: dvou typu dolů a jeden svého druhu nahoru.
- Hmotnost: 1 675 x 10-27 kg
- Žádný čistý poplatek.
- Točení: ½.
Je to stabilní částice v atomovém jádře, ale jako volná částice se rozpadá s poločasem přibližně 10,3 minut. Jeho hmotnost je o něco větší než hmotnost protonu a jak jsme již řekli, nemá žádný čistý náboj..
Počet neutronů v atomu je důležitý, protože i když neurčuje povahu prvku, stejně jako proton, určuje třídu izotopů..
Izotopy prvku jsou jeho variantami a jejich chování se může od sebe zcela lišit. Existují stabilní a nestabilní, například vodík má jako izotopy deuterium a tritium.
Bombardováním atomů určitých sloučenin uranu a plutonia neutrony štěpí jádro a rozkládá se na částice. Nukleární řetězová reakce, která nastane, je schopna emitovat velké množství energie.
Kvarky
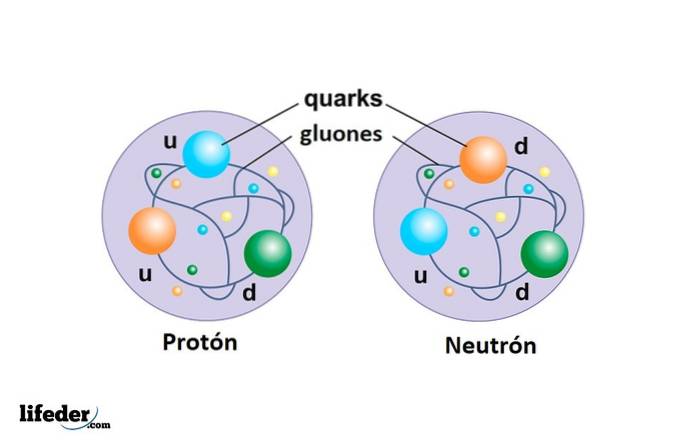
Jsou složkami protonů a neutronů. Dosud bylo nalezeno 6 typů kvarků, ale žádný jako volná částice, ale spíše spojený s tvorbou dalších složených částic.
Důkazy o jeho existenci byly získány experimenty prováděnými od 60. let 20. století pomocí Stanfordova lineárního urychlovače a později v CERNu.
- Poplatek: + 2 / 3e, -1 / 3e
- Točení: ½
- Antičástice: antikvark.
Jiné částice
Počínaje rokem 1930 následovaly objevy nových částic, mnoho předpovězených teorií. Standardní model částic uvažuje o existenci 17 typů základních částic, mezi kvarky, leptony, bosony a Higgsovým bosonem..
Mají také své příslušné antičástice, které při interakci ničí a generují nové částice. Tady jsou některé z nich:
-Pozitron, identický s elektronem, ale kladně nabitý.
-Neutrino, bez poplatku.
-mezon.
-Bosoni, kteří jsou nositeli základních interakcí, kromě gravitace.
-Higgsův boson, zodpovědný za mši.
-Graviton, je částice navržená k vysvětlení gravitace, ale stále neexistuje žádný důkaz, že existuje.
Reference
- Chang, R. 2013. Chemistry. 11. Edice. Mc Graw Hill Education.
- Cobian, J. Standardní model částic. Obnoveno z: sne.es.
- Fernández de Sala, P. Elementární částice, složené částice a virtuální částice. Obnoveno z: ific.uv.es.
- Giambattista, A. 2010. Fyzika. 2. místo Ed. McGraw Hill.
- Olmo, M. Protony a neutrony. Obnoveno z: hyperphysics.phy-astr.gsu.edu.



Zatím žádné komentáře