
Vlastnosti, použití a toxicita p-nitrofenolu
The p-nitrofenol nebo 4-nitrofenol je fenolová organická sloučenina, protože má benzenový kruh připojený k hydroxylové skupině. Písmeno „p“ znamená „pro“ a označuje, že jeho radikály jsou umístěny v poloze 1 a 4 benzenového kruhu.
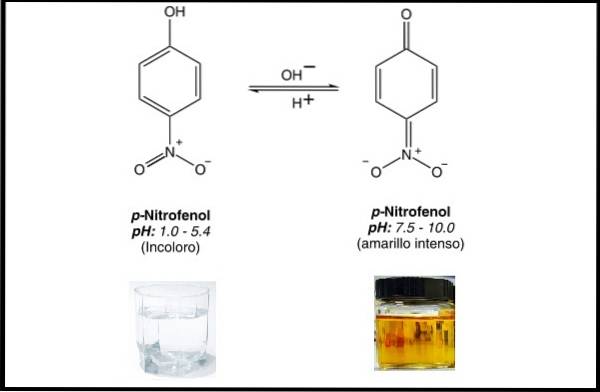
Skupiny přítomné jsou hydroxyl v poloze 1 a nitro skupina v poloze 4. Chemický vzorec p-nitrofenolu je C6H5NE3. P-Nitrofenol je indikátor pH, který je při pH pod 5,4 bezbarvý a nad 7,5 žlutý.
Na druhou stranu se tato sloučenina používá k syntéze různých látek důležitých pro zdraví, jako je paracetamol (známý také jako acetaminofen), což je uznávané analgetikum a antipyretikum..
Podobně slouží jako prekurzor pro syntézu fenethidinu, který je antikonvulzivem, a acetofenethidinu, který slouží jako analgetikum. Dalšími látkami, které lze odvodit z p-nitrofenolu, jsou různé suroviny nezbytné pro výrobu určitých fungicidů a pesticidů..
Kromě toho je to také surovina pro výrobu barviv používaných k tmavnutí kůže..
Navzdory svým výhodám je p-nitrofenol látkou, se kterou je třeba zacházet velmi opatrně, protože představuje vysoké riziko pro zdraví. Má mírnou hořlavost a střední reaktivitu, jak naznačuje NFPA (National Fire Protection Association).
Rejstřík článků
- 1 Funkce
- 2 použití
- 2.1 Indikátor pH
- 2.2 Prekurzor při syntéze sloučenin
- 2.3 Tvorba p-nitrofenolu působením určitých enzymů na specifické substráty
- 3 Toxicita
- 3.1 Účinky na zdraví
- 3.2 První pomoc
- 3.3 Opatření v oblasti biologické bezpečnosti
- 4 Odkazy
Vlastnosti
P-nitrofenol je syntetická chemická látka, což znamená, že se nevyrábí z přírodních zdrojů.
Vyznačuje se tím, že je nažloutlý nebo světle žlutý krystalický prášek. P-nitrofenol má molekulovou hmotnost 139,11 g / mol, bod varu 279 ° C, bod tání 110-115 ° C a teplotu samovznícení 268 ° C. Tato látka se při pokojové teplotě neodpařuje.
Rozpustnost ve vodě při teplotě místnosti je 16 g / l. Je rozpustný v ethanolu, chloroformu a v diethyletheru.
P-nitrofenol je složitá sloučenina, protože jeho pevný stav (krystaly) je tvořen směsí dvou molekulárních forem: jedné zvané alfa a druhé beta.
V alfa formě (4-nitrofenol) je bezbarvý, vykazuje nestabilitu při pokojové teplotě a nevykazuje změny tváře slunečního světla (stabilní).
Zatímco beta forma (4-nitrofenolát nebo fenoxid) se jeví jako žluté krystaly a chová se opačně; to znamená, že je stabilní při pokojové teplotě, ale tváří v tvář slunečnímu záření postupně zčervená..
Tato látka má svůj isosbestický bod při 348 nm pro alfa a beta formy.
Aplikace
Indikátor PH
Ačkoli tato sloučenina má funkci indikátoru pH, není pro tento účel široce používána. Ve vztahu k barevným změnám podle pH se velmi podobá jiným indikátorům pH, jako je thymophthalein a fenolftalein. Společné je, že při nízkém pH jsou bezbarvé.
Prekurzor při syntéze sloučenin
P-nitrofenol je sloučenina používaná ve farmaceutickém průmyslu k syntéze látek s příznivými účinky na zdraví..
Například acetaminofen nebo paracetamol mohou být syntetizovány z p-nitrofenolu, který je jedním z léků s analgetickým a antipyretickým účinkem, které komunita obecně obecně používá..
Z něj se také získává fenethidin, antikonvulzivum používané v případech poruch CNS. Stejně jako acetofenethidin s analgetickým účinkem.
Tvorba p-nitrofenolu působením určitých enzymů na specifické substráty
4-Nitrofenylfosfát je syntetický substrát používaný ke stanovení alkalické fosfatázy. Když enzym působí na tento substrát, tvoří p-nitrofenol (bezbarvá látka).
Později 4-nitrofenol ztrácí protony, aby se z něj stal 4-nitrofenolát, který má žlutou barvu. Reakce musí probíhat při alkalickém pH> 9,0, aby se podpořila konverze na beta formu (4-nitrofenolát).
Vytvořená barva se měří spektrofotometricky při 405 nm, a tak lze tento enzym kvantifikovat.
Totéž platí pro ostatní enzymy na jiných substrátech. Mezi nimi můžeme zmínit působení enzymu karboanhydrázy na 4-nitrofenylacetát a glykosidázy na 4-nitrofenyl-β-D-glukopyranosid.
Toxicita
Podle NFPA (National Fire Protection Association) je p-nitrofenol klasifikován jako látka se zdravotním rizikem stupně 3. To znamená, že poškození zdraví je vážné..
Na druhou stranu představuje riziko hořlavosti 1, což znamená, že riziko jeho vzniku je malé. Nakonec má riziko stupně reaktivity 2 (střední riziko). To znamená, že za určitých podmínek je tato látka schopna emitovat energii.
Zdravé efekty
Mezi nejvýznamnější účinky této látky na zdraví patří účinky, které uvedeme níže.
Na úrovni pokožky způsobuje podráždění, zánět a popáleniny. Kontakt s pokožkou navíc představuje cestu absorpce produktu. Přehnané vystavení p-nitrofenolu může ovlivnit centrální nervový systém (CNS).
Na oční sliznici může způsobit těžké popáleniny se závažným poškozením očí. Na úrovni dýchání zánět, kašel a udušení. V případě náhodného požití vyvolává zvracení se silnými bolestmi břicha, duševními zmatky, tachykardií, horečkou a slabostí..
Pokud je absorbován ve velkém množství, může způsobit onemocnění zvané methemoglobinemie, charakterizované zvýšením množství methemoglobinu v krvi..
Toto onemocnění významně ovlivňuje transport kyslíku, a proto vytváří příznaky charakterizované bolestmi hlavy, únavou, závratěmi, cyanózou a dýchacími potížemi. V závažných případech může také způsobit smrt.
Lidé vystavení malému množství projdou produkt močí. A konečně, navzdory všem popsaným škodlivým účinkům nebylo prokázáno, že má karcinogenní účinek.
První pomoc
Pokud jste přišli do styku s výrobkem, je nutné odstranit kontaminovaný oděv a postižené místo (kůži nebo sliznice) umýt velkým množstvím vody. V případě vdechnutí odneste postiženého na dobře větrané místo. V případě, že pacient nedýchá, použijte asistované dýchání.
Poté je nutné oběť co nejdříve převést do zdravotnického zařízení.
Opatření v oblasti biologické bezpečnosti
- Musíte pracovat pod digestoří nebo jinak nosit respirátory. Noste vhodné oblečení (plášť, rukavice, ochranné brýle, uzavřené boty a čepice).
- Okamžitě vyperte oděv kontaminovaný výrobkem.
- Kontaminované pracovní nářadí si nevezměte domů.
- Pracoviště by mělo být vybaveno výplachem očí a nouzovými sprchami.
- Při manipulaci s touto látkou nepoužívejte kontaktní čočky.
- Nekuřte, nejezte a nepijte uvnitř zařízení, kde se s touto látkou zachází.
- P-nitrofenol je nekompatibilní s určitými látkami, a proto musí být skladován odděleně od silných alkálií, jako je hydroxid sodný nebo hydroxid draselný. Je také nekompatibilní s peroxidy, chloristany, manganistany, chlorem, dusičnany, chlorečnany, bromem a fluorem, mezi jinými oxidanty..
- Pamatujte, že v případě požáru mohou nádoby obsahující tuto látku explodovat..
Reference
- Ministerstvo zdravotnictví a služeb pro seniory v New Jersey. Informační list o nebezpečných látkách. 4-nitrofenol. 2004. Dostupné na: nj.gov/health.
- „4-nitrofenol.“ Wikipedia, The Free Encyclopedia. 22. února 2019, 13:58 UTC. 29. května 2019, 03:59 wikipedia.org.
- Rojas H, Cubillos J, Guerrero D. Hydrogenace p-nitrofenolu pomocí Ir, Ni a Ir-Ni katalyzátorů nanesených na TiO2. Časopis Fakulty strojní, UPTC; 2012, 21 (3): 63-72
- Agentury pro toxické látky a registr nemocí. Souhrny veřejného zdraví. Nitrofenoly. Dostupné na: atsdr.cdc.gov
- Národní institut bezpečnosti a hygieny při práci. Mezinárodní karty chemické bezpečnosti. 4-nitrofenol. Španělsko. K dispozici na: insht.es/InshtWeb



Zatím žádné komentáře