
Co je to Molality? (s příklady)
The molalita, označený malým písmenem m, je to termín používaný k popisu koncentrace roztoku. Lze jej definovat jako počet molů rozpuštěné látky v 1 kilogramu rozpouštědla.
Rovná se molům rozpuštěné látky (látka, která se rozpouští) děleno kilogramy rozpouštědla (látka použitá k rozpuštění).
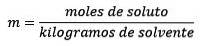
V případě, že moly rozpuštěné látky jsou dány rovnicí:
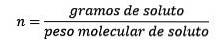
Nakonec tedy rovnice molality je

Rejstřík článků
- 1 Charakteristiky molality
- 2 Rozdíly a podobnosti mezi molalitou (m) a molaritou (M)
- 3 Příklady molality
- 3.1 Příklad 1:
- 3.2 Příklad 2:
- 3.3 Příklad 3:
- 4 Odkazy
Charakteristiky molality
Molalita je míra koncentrace rozpuštěné látky v roztoku. Používá se především tam, kde je problém s teplotou.

Molalita není tak běžná jako její protějšek, molarita (moly rozpuštěné látky na litr rozpouštědla), ale používá se ve velmi konkrétních výpočtech, zejména s ohledem na koligativní vlastnosti (zvýšení bodu varu, deprese bodu varu). Zmrazení).
Vzhledem k tomu, že objem podléhá změnám v důsledku teploty a tlaku, mění se také molarita v závislosti na teplotě a tlaku. V některých případech je použití závaží výhodou, protože hmotnost se nemění podle podmínek prostředí..
Je důležité použít hmotnost rozpouštědla, nikoli hmotnost roztoku. Roztoky označené koncentrací molal jsou označeny malým písmenem m. 1,0 m roztok obsahuje 1 mol rozpuštěné látky na kilogram rozpouštědla.
Příprava roztoku dané molality je snadná, protože vyžaduje pouze dobré měřítko. Obě rozpouštědla a rozpuštěné látky jsou namíchány namísto objemových.
Jednotka SI (mezinárodní systém) pro molalitu je mol / kg nebo molů rozpuštěných látek na kg rozpouštědla. Roztok s molalitou 1 mol / kg je často popisován jako „1 molal“ nebo „1 m“.
V návaznosti na systém jednotek SI však National Institute of Standards and Technology, což je orgán USA pro měření, považuje termín „molal“ a symbol jednotky „m“ za zastaralý a navrhuje použití mol / kg.
Rozdíly a podobnosti mezi molalitou (m) a molaritou (M)
Příprava roztoku dané molality zahrnuje zvážení jak rozpuštěné látky, tak rozpouštědla a získání jejich hmot..
Ale v případě molarity se měří objem roztoku, což ponechává prostor pro změny hustoty v důsledku podmínek prostředí teploty a tlaku..
To znamená, že je výhodné pracovat s molalitou, která se zabývá hmotou, protože v chemickém složení je hmotnost známé čisté látky důležitější než její objem, protože objemy lze měnit vlivem teploty a tlaku, zatímco hmota zůstává nezměněna.
Chemické reakce navíc probíhají v poměru k hmotnosti, nikoli objemu. Na základě hmotnosti lze molalitu snadno převést na hmotnostní poměr nebo hmotnostní zlomek.
U vodných roztoků (roztoků, ve kterých je rozpouštědlem voda) blízké teplotě místnosti je rozdíl mezi molárními a molárními roztoky zanedbatelný..
Je tomu tak proto, že kolem teploty místnosti má voda hustotu 1 kg / l. To znamená, že „na litr“ molarity se rovná „na kg“ molality..
Pro rozpouštědlo, jako je ethanol, kde hustota je 0,789 kg / l, by 1M roztok byl 0,789 m.
Důležitou součástí zapamatování rozdílu je:
Molarita - M → mol na litr roztoku.
Molalita - m → mol na kilogram rozpouštědla.
Příklady molality
Příklad 1:
Problém: Jaká je molalita roztoku obsahujícího 0,086 mol NaCl rozpuštěného ve 25,0 g vody?
Odpovědět: Tento příklad používá rovnici přímé molality:
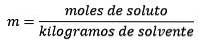
Mole rozpuštěné látky (NaCl) = 0,086 mol
Hmotnost (voda) = 25,0 g = 25,0 x 10-3 kg
Nahrazení máme:
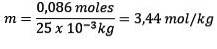
Příklad 2:
Problém: Jaká je molalita roztoku, pokud je 124,2 gramu NaOH rozpuštěno v 1,00 litru vody? (Hustota vody se rovná 1,00 g / ml).
Odpovědět: Voda je známá jako univerzální rozpouštědlo a hustota se obvykle udává jako 1,00 gramů na mililitr, což je 1 kilogram na litr. To usnadňuje převod z litrů na kilogramy..
V tomto problému bude muset být 124,2 gramů NaOH převedeno na moly (pro mol rozpuštěné látky) a jeden litr vody bude muset být převeden na kilogramy (na kilogram rozpouštědla) pomocí hustoty.
Nejprve najděte molární hmotnost NaOH:
ODPOLEDNENa= 22,99 g / mol
ODPOLEDNENEBO= 16 g / mol
ODPOLEDNEH= 1 g / mol
ODPOLEDNENaOH= 22,99 g / mol +16 g / mol +1 g / mol = 39,99 g / mol
Za druhé převádíte gramy NaOH na mol pomocí molární hmotnosti:
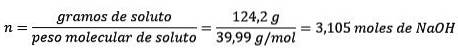
Za třetí, převeďte litr vody na kilogramy pomocí hustoty.
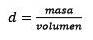
Řešení pro hmotu zůstává
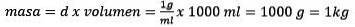
Nakonec je vyřešena rovnice molality:
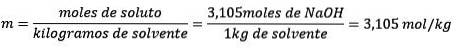
Příklad 3:
Problém: Jaká je hmotnost vody vodného roztoku obsahujícího 0,52 gramu chloridu barnatého (BaCldva, PM = 208,23 g / mol), jehož koncentrace je 0,005 mol / kg?
Odpovědět: v tomto případě se pro stanovení množství vody v roztoku použije koncentrace molalu.
Nejprve se získá počet molů BaCldva v řešení:
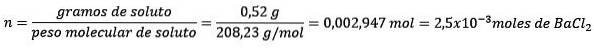
Za druhé, odstraňte kilogramy rozpouštědla z rovnice molality a vyřešte.
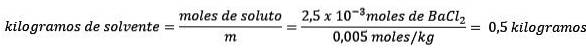
Reference
- Vědecké poznámky a projekty. (2015, 22. února). Příklad problému výpočtu molality. Obnoveno ze sciencenotes.org.
- Bhardwaj, M. (2014, 26. listopadu). Jaký je příklad molality? Obnoveno ze socratic.org.
- (S.F.). Molalita. Obnoveno z boundless.com.
- Helmenstine, T. (2017, 19. února). Jaký je rozdíl mezi molaritou a molalitou? Obnoveno z thoughtco.com.
- Molality vzorec. (S.F.). Obnoveno z softschools.com.
- Molalita. (S.F.). Obnoveno z chemteam.l
- Co je to Molality? (S.F.). Obnoveno z freechemistryonline.com.


Zatím žádné komentáře