
Jaké jsou Van der Waalsovy síly?
The Van der Waalsovy síly jsou to mezimolekulární síly elektrické povahy, které mohou být atraktivní nebo odpudivé. Existuje interakce mezi povrchy molekul nebo atomů, která se v podstatě liší od iontových, kovalentních a kovových vazeb, které se tvoří uvnitř molekul..
I když jsou tyto síly slabé, jsou schopné přilákat molekuly plynu; také u zkapalněných a ztuhlých plynů a u všech organických kapalin a pevných látek. Johannes Van der Waals (1873) byl ten, kdo vyvinul teorii vysvětlující chování skutečných plynů.

V takzvané Van der Waalsově rovnici pro skutečné plyny - (P + nandva/ Vdva) (V - čb)) = nRT - zavedou se dvě konstanty: konstanta b (tj. objem obsazený molekulami plynu) a „a“, což je empirická konstanta.
Konstanta „a“ opravuje odchylku od očekávaného chování ideálních plynů při nízkých teplotách, přesně tam, kde je vyjádřena přitažlivá síla mezi molekulami plynů. Schopnost atomu polarizovat se v periodické tabulce zvyšuje od horní části skupiny ke spodní části skupiny a zprava doleva po určité období..
Zvyšováním atomového čísla - a tím i počtu elektronů - se ty, které jsou umístěny ve vnějších skořápkách, snáze přesunou za vzniku polárních prvků.
Rejstřík článků
- 1 Intermolekulární elektrické interakce
- 1.1 Interakce mezi permanentními dipóly
- 1.2 Interakce mezi permanentním dipólem a indukovaným dipólem
- 2 Londýnské síly nebo rozptyl
- 3 rádia Van der Waals
- 4 Síly a energie elektrické interakce mezi atomy a mezi molekulami
- 5 Reference
Intermolekulární elektrické interakce
Interakce mezi permanentními dipóly
Existují elektricky neutrální molekuly, které jsou permanentními dipóly. To je způsobeno narušením elektronické distribuce, které vytváří prostorové oddělení kladných a záporných nábojů směrem ke koncům molekuly, což představuje dipól (jako by to byl magnet).
Voda je tvořena 2 atomy vodíku na jednom konci molekuly a atomem kyslíku na druhém konci. Kyslík má vyšší afinitu k elektronům než vodík a přitahuje je.
Toto produkuje posun elektronů směrem ke kyslíku a zanechává tento záporně nabitý a vodík s kladným nábojem..

Negativní náboj molekuly vody může elektrostaticky interagovat s kladným nábojem jiné molekuly vody a způsobit tak elektrickou přitažlivost. Tento typ elektrostatické interakce se tedy nazývá Keesomovy síly.
Interakce mezi permanentním dipólem a indukovaným dipólem
Trvalý dipól má tzv. Dipólový moment (µ). Velikost dipólového momentu je dána matematickým výrazem:
µ = q.x.
q = elektrický náboj.
x = prostorová vzdálenost mezi póly.
Dipólový moment je vektor, který je podle konvence znázorněn orientovaný od záporného pólu ke kladnému pólu. Velikost μ bolí vyjádřit v debye (3,34 × 10-30 Cm.
Permanentní dipól může interagovat s neutrální molekulou, což způsobí změnu v její elektronické distribuci, což má za následek indukovaný dipól v této molekule.
Permanentní dipól a indukovaný dipól mohou elektricky interagovat a vytvářet elektrickou sílu. Tento typ interakce se nazývá indukce a síly působící na něj se nazývají Debyeovy síly..
Londýnské síly nebo rozptyl
Povaha těchto atraktivních sil je vysvětlena kvantovou mechanikou. London předpokládal, že v elektricky neutrálních molekulách se střed negativních nábojů elektronů a střed kladných nábojů jader nemusí shodovat..
Kolísání hustoty elektronů tedy umožňuje molekulám chovat se jako dočasné dipóly.
Toto není samo o sobě vysvětlení atraktivních sil, ale dočasné dipóly mohou vyvolat správně zarovnanou polarizaci sousedních molekul, což má za následek generování atraktivní síly. Atraktivní síly generované elektronickými fluktuacemi se nazývají Londýnské síly nebo disperze..
Van der Waalsovy síly ukazují anizotropii, a proto jsou ovlivněny orientací molekul. Interakce typu disperze jsou však vždy převážně atraktivní..
Londýnské síly zesilují, jak se zvětšuje velikost molekul nebo atomů.
V halogenech jsou to molekuly F.dva a Cldva nízká atomová čísla jsou plyny. BRdva s nejvyšším atomovým číslem je kapalina a Idva, halogen s nejvyšším atomovým číslem je při teplotě místnosti pevná látka.
Zvýšení atomového čísla zvyšuje počet přítomných elektronů, což usnadňuje polarizaci atomů, a tím i interakce mezi nimi. To určuje fyzikální stav halogenů.
Van der Waalsovy rádia
Interakce mezi molekulami a mezi atomy mohou být atraktivní nebo odpudivé v závislosti na kritické vzdálenosti mezi jejich středy, která se nazývá rproti.
Na vzdálenosti mezi molekulami nebo atomy větší než rproti, přitažlivost mezi jádry jedné molekuly a elektrony druhé převažuje nad odpuzováním mezi jádry a elektrony dvou molekul.
V popsaném případě je interakce atraktivní, ale co se stane, když se molekuly přiblíží ve vzdálenosti mezi jejich středy, která je menší než rv? Pak odpudivá síla převažuje nad tou atraktivní, která se staví proti bližšímu přístupu mezi atomy..
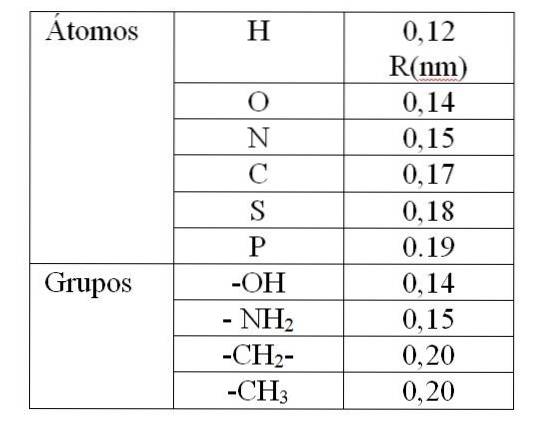
Hodnota rproti Je to dáno tzv. Van der Waalsovým poloměrem (R). Pro sférické a identické molekuly rproti se rovná 2R. Pro dvě různé molekuly poloměrů R.1 a R.dva: rproti rovná se R1 + Rdva. Hodnoty Van der Waalsových poloměrů jsou uvedeny v tabulce 1.
Hodnota uvedená v tabulce 1 označuje Van der Waalsův poloměr 0,12 nm (10-9 m) pro vodík. Pak hodnota rproti pro tento atom je to 0,24 nm. Pro hodnotu rproti méně než 0,24 nm způsobí odpor mezi atomy vodíku.
Síly a energie elektrické interakce mezi atomy a mezi molekulami
Síla mezi dvojicí nábojů q1 a codva, oddělené ve vakuu vzdáleností r, je dáno Coulombovým zákonem.
F = k. co1.codva/ rdva
V tomto výrazu k je konstanta, jejíž hodnota závisí na použitých jednotkách. Pokud je hodnota síly - daná použitím Coulombova zákona - záporná, znamená to přitažlivou sílu. Naopak, pokud je hodnota uvedená pro sílu kladná, znamená to odpudivou sílu.
Protože molekuly jsou obvykle ve vodném prostředí, které chrání elektrické síly, je nutné zavést pojem dielektrická konstanta (ε). Tato konstanta tedy koriguje hodnotu danou pro elektrické síly aplikací Coulombova zákona.
F = k.q1.codva/ε.rdva
Podobně je energie pro elektrickou interakci (U) dána výrazem:
U = k. co1.codva/ε.r
Reference
- Redaktoři Encyclopaedia Britannica. (2018). Van der Waalsovy síly. Citováno dne 27. května 2018 z webu: britannica.com
- Wikipedia. (2017). Van der Waalsovy síly. Citováno dne 27. května 2018 z: es.wikipedia.org
- Kathryn Rashe, Lisa Peterson, Seila Buth, Irene Ly. Van der Waalsovy síly. Citováno dne 27. května 2018 z: chem.libretexts.org
- Morris, J. G. (1974) Biologist's Physical Chemistry. 2 a vydání. Edward Arnold (Publishers) Limited.
- Mathews, C. K., Van Holde, K.E. a Ahern, K.G. (2002) Biochemistry. Třetí edice. Addison Wesley Longman, Inc..



Zatím žádné komentáře