
Redukce (chemie) z čeho se skládá a příklady

The snížení Je to celá ta chemická reakce, kdy atomy jednoho z reaktantů nakonec získají elektrony; Co lze také vidět takto: snižuje se vaše neobsazenost nebo elektronické „nepohodlí“. Atom získává elektrony, když je druh daruje; to znamená, že rez.
K tomuto typu reakce nemůže dojít samo: pokud jeden druh přijímá elektrony, musí se jich jiný nutně vzdát. Jinak by hmota byla vytvářena z ničeho, redukováním atomů po získání elektronů z vakua. Proto se jedná o redoxní poloviční reakci (redukce / oxidace).
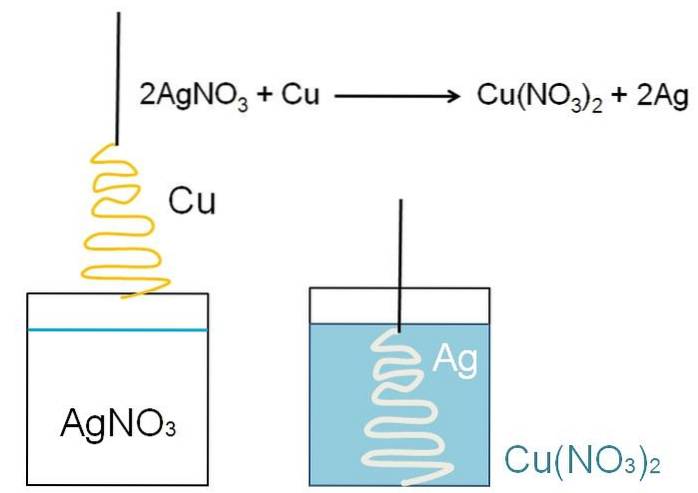
Názorným příkladem redukce, kterou lze ukázat ve třídách, je reakce mezi kovovým povrchem mědi a vodným roztokem dusičnanu stříbrného AgNO3.
V roztoku se stříbro nachází jako kationty Ag+, kladně nabitý. Ty interakcí s povrchem mědi ve tvaru vánočního stromku vytrhávají elektrony z atomů mědi. Když k tomu dojde, měď nahradí stříbro v dusičnanové soli; a ve výsledku dusičnan měďnatý, Cu (NO3)dva.
Cu kationtydva+ vedle NO3- otočte roztok do modra; a stříbro, bělí vánoční stromek, jako by ho zakryl sněhem.
Rejstřík článků
- 1 Jaká je redukce?
- 1.1 Počet kyslíku
- 1.2 Elektronegativní atom
- 2 Příklady
- 2.1 Snížení v organické chemii
- 2.2 Těžba kovů
- 3 Odkazy
Jaká je redukce?
Při redukci již bylo řečeno, že druh získává elektrony. Jak to lze ověřit chemickou rovnicí? Například v rovnici pro reakci mezi Cu a AgNO3, Jak zjistit, kdy ke snížení dojde? K jeho ověření je nutné určit počet nebo oxidační stav.
Prvky v jejich přirozených stavech mají ze své podstaty oxidační stav rovný nule, protože se předpokládá, že neztratily ani nezískaly elektrony. Pevné kovy tedy mají nulový oxidační stav. Stříbro tedy jde od +1 (Ag+) na 0 (Ag). Náboj kovového iontu se rovná jeho oxidačnímu stavu.
Na druhou stranu, elektrony pocházely z mědi: od 0 (Cu) do +2 (Cudva+). Dusičnanový anion, NO3- zůstává beze změny, zatímco oba kovy si vyměňují elektrony; proto lze rovnici psát jako:
2Ag+ + Cu => 2Ag + Cudva+
Všimněte si, že jak náboje, tak atomy jsou vyvážené..
To je to, z čeho se skládá chemická redukce: v zisku elektronů, díky nimž jsou oxidační stavy atomů méně pozitivní než u elektronů..
Číslo kyslíku
Kyslíky jsou velmi elektronegativní a oxidující atomy, takže když s nimi atom vytváří sloučeniny (jako oxidy), mají pozitivní oxidační stavy. Čím větší je počet kyslíků interagujících s atomem, tím pozitivnější bude jeho oxidační stav; nebo co je stejné, je rezavější.
Proto, když má sloučenina méně atomů kyslíku, říká se, že je méně oxidovaná; to znamená, že atom ztrácí méně elektronů.
Klasickým příkladem je oxid uhelnatý a oxid uhličitý. U CO má uhlík oxidační stav +2; zatímco pro COdva, jeho oxidační stav je +4.
Takže pokud v reakci COdva transformuje se na CO, říká se, že dochází ke snížení; protože uhlík nyní interaguje s jedním kyslíkem a ne se dvěma. Pro opačnou reakci se CO transformuje na COdva, hovoří se o oxidaci uhlíku.
To platí pro všechny atomy, zejména kovy v jejich oxidech kovů; například CrOdva (Cr4+) a CrO3 (Cr6+).
V chemických rovnicích, kde jeden druh ztrácí kyslík, zatímco druhý druh ho získává, se říká, že dochází k přenosu kyslíku.
Elektronegativní atom
Vždy můžete určit, zda došlo ke snížení, změnou oxidačního stavu na méně pozitivní hodnotu. Jak jsme právě vysvětlili, rychlým způsobem, jak si toho všimnout, aniž bychom matematiku zvládli, je pozorování, zda ve sloučenině dochází k poklesu atomů kyslíku..
Totéž se může stát s jakýmkoli jiným atomem, který je elektronegativnější než atom, který získává nebo ztrácí elektrony.
Například pokud CF4 reaguje takovým způsobem, že se z něj stane CH4, pak se říká, že došlo ke snížení; protože fluor je mnohem elektronegativnější než atom vodíku. Ve výsledku je uhlík v CH méně oxidován4 že v CF4, což se rovná tvrzení, že byla snížena.
Příklady
Snížení v organické chemii
Příklad CF4 a CH4 odráží to, co se děje v organických reakcích, kde je snížení parciálního náboje atomu považováno za elektronický zisk. To platí hodně, když uvažujeme o redukci okysličených funkčních skupin..
Zvažte například skupiny ROH, RCHO a COOH. První odpovídá alkoholům, kde se uhlík váže s kyslíkem (C-OH); druhá je aldehydová skupina, kde uhlík tvoří dvojnou vazbu s kyslíkem a je také vázán na vodík (C = O-H); a třetí je karboxylová skupina.
V karboxylové skupině tvoří uhlík dvojnou vazbu s jednou O a jednoduchou vazbu s druhou O (HO-C = O).
Proto dojde k redukci, pokud se karboxylová kyselina přemění na alkohol:
RCOOH => ROH
Těžba kovů
Chemická redukce je nesmírně důležitá v procesech těžby kovů z jejich minerálů. Některé z reakcí jsou:
HgS + Odva => Hg + SOdva
Sulfid rtuťnatý se redukuje na kovovou rtuť.
CudvaS + Odva => 2Cu + SOdva
Sulfid měďnatý se redukuje na kovovou měď.
2ZnS + 3Odva => 2ZnO + 2SOdva
ZnO + C => Zn + CO (všimněte si převodu O)
Sulfid zinečnatý se nejprve redukuje na jeho oxid uhelnatý a poté na jeho kovovou formu.
VíradvaNEBO3 + 3CO => 2Fe + 3COdva
Oxid železitý se redukuje na kovové železo.
WO3 + 3Hdva => W + 3HdvaNEBO
A oxid wolframový se redukuje na kovový wolfram.
Jako cvičení lze určit oxidační číslo kovu před jeho snížením.
Reference
- Whitten, Davis, Peck a Stanley. (2008). Chemie. (8. vydání). Učení CENGAGE.
- Chemistry LibreTexts. (9. prosince 2018). Oxidačně-redukční reakce. Obnoveno z: chem.libretexts.org
- Helmenstine, Anne Marie, Ph.D. (04. července 2018). Definice redukce v chemii. Obnoveno z: thoughtco.com
- Hultzman R. (2019). Reduction in Chemistry: Definition & Overview. Studie. Obnoveno z: study.com
- Clark J. (2013). Definice oxidace a redukce (redox). Obnoveno z: chemguide.co.uk
- Pohled lektora. (s.f.). Redukční reakce. Obnoveno z: chemistry.tutorvista.com



Zatím žádné komentáře