
Síran vápenatý (CaSO4) Chemická struktura, vlastnosti, použití

The síran vápenatý Je to ternární sůl vápníku, kovu alkalických zemin (pan Becambara), síry a kyslíku. Jeho chemický vzorec je CaSO4, což znamená, že pro každý kation Cadva+ existuje anion SO4dva- interakce s ním. Představuje sloučeninu se širokou distribucí v přírodě.
Jeho nejhojnější formou je CaSO42HdvaO (sádra) a bezvodá forma CaSO4 (anhydrit). Existuje také třetí forma: sádra z Paříže, vyráběná zahříváním sádry (hemidrát, CaSO41 / 2HdvaNEBO). Pevná část této ternární soli je zobrazena na dolním obrázku a má bělavý vzhled..

Rejstřík článků
- 1 Chemická struktura
- 2 Vlastnosti
- 2.1 Molekulární vzorec
- 2.2 Bezvodá molekulová hmotnost
- 2.3 Zápach
- 2.4 Vzhled
- 2.5 Hustota
- 2.6 Teplota tání
- 2.7 Rozpustnost
- 2.8 Stabilita
- 3 použití
- 3.1 Ve stavebnictví a umění
- 3.2 Terapeutika
- 3.3 Ve zpracování potravin
- 3.4 Jako hnojivo a kondicionér pro rostlinné půdy
- 3.5 Při výrobě dalších sloučenin
- 4 Odkazy
Chemická struktura
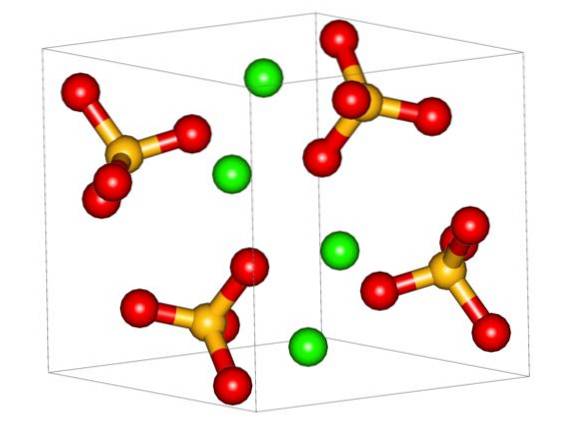
Horní obrázek ukazuje ortorombickou jednotkovou buňku pro CaSO4. Zde se předpokládá, že interakce jsou čistě elektrostatické; tj. kationty Cadva+ přilákat čtyřboké anionty SO4dva-.
Avšak Cadva+ je vysoce náchylný ke koordinaci a tvoří kolem ní mnohostěnné struktury. Co to je? K elektronické dostupnosti vápníku přijímat elektrony bazických nebo negativních druhů (jako jsou O atomy SO4dva-).
S ohledem na předchozí bod, nyní Ca iontydva+ Přijímají datové odkazy (poskytované OS) a jednotková buňka je transformována, jak je uvedeno na obrázku níže:
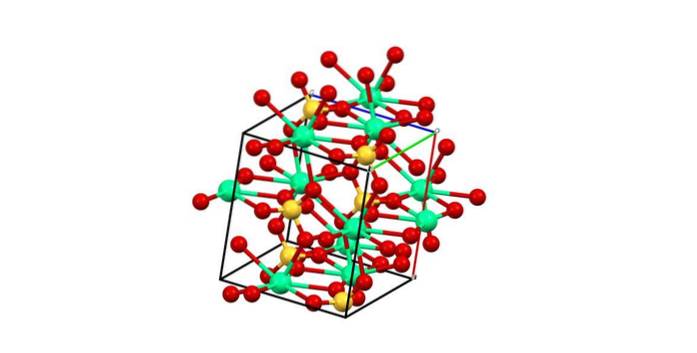
V důsledku toho se vytvoří mnohostěn CaO8 (zelená koule Cadva+ obklopen osmi červenými koulemi O z tetraedru SO4 poblíž). Vápenatý polyhedra a síranový čtyřstěn; toto je krystalická struktura CaSO4 bezvodý.
Navíc, když krystaly hydratují - tvoří se dihydrátovaná sůl nebo hemidrát (CaSO41/2 HdvaO) - struktura se rozšiřuje a začleňuje molekuly vody.
Tyto molekuly se mohou prokládat a koordinovat s vápníkem; to znamená, že nahrazují jednu nebo dvě sulfátové skupiny.
Na druhou stranu ne celá voda se stává součástí mnohostěnu CaO.8. Některé naopak tvoří vodíkové vazby se sírany. Ty slouží jako spojení dvou klikatých sekcí, produktů uspořádání iontů v krystalu.
Vlastnosti
Molekulární vzorec
CaSO4 nH2O.
Bezvodá molekulová hmotnost
136,134 g / mol.
Zápach
Je bez zápachu.
Vzhled
V případě anhydritu to vypadá jako bílý prášek nebo pevné ortorombické nebo monoklinické krystaly. Krystaly mají různou barvu: mohou být bílé nebo s namodralým, šedavým nebo načervenalým odstínem; může být také cihlově červená.
Hustota
2,96 g / cm3 (bezvodá forma). 2,32 g / cm3 (ve formě dihydrátu).
Bod tání
1450 ° C (2840 ° F). Charakteristické pro silné elektrostatické interakce mezi dvojmocnými ionty Cadva+ A tak4dva-.
Rozpustnost
0,2-0,3% ve vodě při 25 ° C Je špatně rozpustný ve vodě a nerozpustný v ethanolu.
Stabilita
Stabilní při pokojové teplotě.
Aplikace

Ve stavebnictví a v umění
Používá se při zpracování štuku ke zpevnění stěn domů a jiných staveb, které přispívají k jeho zkrášlení. Reliéfy se navíc vyrábějí pomocí forem ve stropech a okenních rámech. Omítka je také ve stropech.
Síran vápenatý se používá k řešení problému, který se vyskytuje při hydrataci betonu, a tím spolupracuje na stavbě silnic, cest atd..
Sádrové sochy jsou vyrobeny, zejména náboženské postavy, a na hřbitovech jsou použity na náhrobcích.
Terapeutika
veterinář
Experimentálně se ve veterinární medicíně používají sterilní kousky síranu vápenatého k opravě kostních defektů nebo dutin, jako jsou ty, které zůstaly po ranách nebo nádorech..
Sádra z Paříže může být použita k opravě kostních defektů kvůli své jedinečné schopnosti stimulovat osteogenezi. Rentgenové studie a technecium (Tc99m) medronát podporují použití sádry z Paříže jako aloplastu a jeho osteogenní kapacitu při implantaci do čelního sinu.
Regenerace kostí byla prokázána u šesti psů v období 4 až 6 měsíců. Síran vápenatý se v této oblasti začal používat v roce 1957 ve formě sádry z pařížských tablet, které byly schopny vyplnit vady v kostech psů..
Kostní substituce síranem vápenatým je srovnatelná s náhradou pozorovanou v autogenní kosti.
Ruhaimi (2001) aplikoval síran vápenatý na nedávno zničenou králičí čelistní kost, přičemž sledoval nárůst osteogeneze a kalcifikace kostí..
Lék
Síran vápenatý se v medicíně používá k imobilizaci vykloubených kloubů a zlomenin kostí a používá se jako pomocná látka při výrobě tablet..
odontologie
Ve stomatologii se používá jako základ pro výrobu zubních náhrad, při náhradách a otiscích zubů..
Při zpracování potravin
Používá se jako koagulant při výrobě tofu, potraviny vyrobené ze sóji a široce konzumované ve východních zemích jako náhrada masa. Kromě toho se používá jako zpevnění potravin a při zpracování mouky.
Jako hnojivo a kondicionér pro rostlinné půdy
Sádra (CaSO42HdvaO) se v Evropě používalo jako hnojivo od osmnáctého století, což má tu výhodu oproti použití vápna jako zdroje vápníku pro větší mobilitu.
Vápník musí být k dispozici kořenům rostlin pro jeho dostatečný přísun. Přidání vápníku tedy zlepšuje zahradnické a podzemnice olejné..
Hniloba kořenů arašídů způsobená biologickými patogeny, stejně jako hniloba konce melounu a rajčatového květu, je částečně potlačována aplikacemi v zemědělství..
Sádra pomáhá snižovat rozptyl jílu, který způsobuje tvorbu krust na zemi. Zmenšením krust vytvořených na zemi sádra usnadňuje výstup sazenic. Rovněž zvyšuje vstup vzduchu a vody do země.
Sádra pomáhá zlepšovat půdu zmírňováním kyselosti a toxicity hliníku, čímž přizpůsobuje plodinu sodným půdám.
Při výrobě dalších sloučenin
Síran vápenatý reaguje s hydrogenuhličitanem amonným za vzniku síranu amonného. Rovněž se používá při výrobě kyseliny sírové.
Bezvodý síran vápenatý se smísí s břidlicí nebo chudou látkou a při zahřívání směsi se uvolňuje oxid sírový v plynné formě. Oxid siřičitý je prekurzorem kyseliny sírové.
Reference
- Kouřová noha. (26. prosince 2015). Struktura CaSO4. [Postava]. Citováno dne 6. května 2018 z: commons.wikimedia.org
- Takanori Fukami a kol. (2015). Syntéza, krystalová struktura a tepelné vlastnosti CaSO42HdvaNebo jednotlivé krystaly. International Journal of Chemistry; Sv. 7, č. 2; ISSN 1916-9698 E-ISSN 1916-9701 Publikováno Kanadským střediskem pro vědu a vzdělávání.
- PubChem. (2018). Síran vápenatý. Citováno dne 6. května 2018 z: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2018). Síran vápenatý. Citováno dne 6. května 2018 z: en.wikipedia.org
- Elsevier. (2018). síran vápenatý. Citováno dne 6. května 2018 z: sciencedirect.com
- Kimberlitesoftwares. (2018). Síran vápenatý. Citováno dne 6. května 2018 z: worldofchemicals.com
- Intagri. (2017). Příručka pro použití zemědělské sádry jako zlepšení půdy. Citováno dne 6. května 2018 z: intagri.com



Zatím žádné komentáře