
Vzorec, vlastnosti a použití kyseliny chloristé

The kyselina chloristá Je to velmi silná minerální kyselina, která se obvykle vyskytuje jako bezbarvý vodný roztok bez zápachu, korozivní pro kovy a tkaniny. Je to horký silný oxidant, ale jeho vodné roztoky (až do asi 70% hmotnostních) při pokojové teplotě jsou obecně bezpečné a vykazují pouze silné kyselé vlastnosti a žádné oxidační vlastnosti..
Kyselina chloristá a její soli (zejména chloristan amonný [NH4ClO4, CAS: 7790-98-9], chloristan sodný [NaClO4, 7601-89-0] a chloristan draselný [KClO4, 7778-74- 7]), najít mnoho aplikací díky své silné oxidační síle.

Jeho výroba se zvýšila díky jeho použití jako výchozího materiálu pro výrobu čistého chloristanu amonného, základní přísady do výbušnin a pevných pohonných hmot pro rakety a střely..

Kyselina chloristá se také v omezeném měřítku používá jako činidlo pro analytické účely. Jeho uzavřené kontejnery mohou při dlouhodobém působení tepla prudce prasknout..
Vzorce: Kyselina chloristá: HClO4
CAS: 7601-90-3
2D struktura
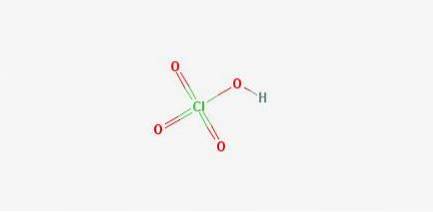
3D struktura
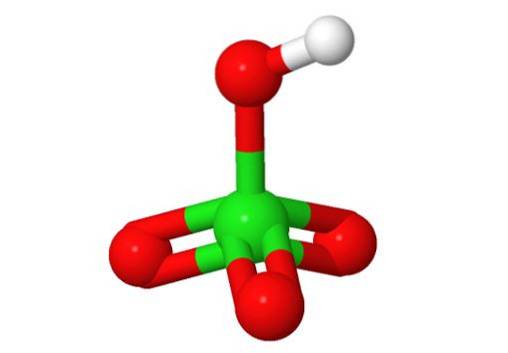
Vlastnosti kyseliny chloristé
Fyzikální a chemické vlastnosti
- Vzhled: bezbarvá kapalina
- Zápach: bez zápachu
- Molekulová hmotnost: 100,454 g / mol
- Bod varu: 19 ° C
- Teplota tání: -112 ° C
- Hustota: 1,768 g / cm3
- Rozpustnost ve vodě: Mísitelný
- Kyselost (pKa): -15,2 (± 2,0)
Kyselina chloristá patří do skupiny silně oxidujících kyselin.
Hořlavost
-Silné oxidační kyseliny nejsou obecně hořlavé, ale mohou urychlit spalování jiných materiálů poskytnutím kyslíku (působí jako oxidační činidla).
-Roztoky kyseliny chloristé mohou explodovat z tepla nebo kontaminace.
-Při zahřátí nad 160 ° C nebo při požáru se mohou explozivně rozložit.
-Mohou výbušně reagovat s uhlovodíky (palivy). Může vznítit paliva (dřevo, papír, olej, oblečení atd.).
-Nádoby mohou při zahřátí explodovat.
-Odtok může způsobit požár nebo výbuch.
Reaktivita
-Silné oxidační kyseliny jsou obecně rozpustné ve vodě za uvolňování vodíkových iontů. Výsledné roztoky mají pH 1 nebo blízké 1.
-Materiály v této skupině reagují s chemickými bázemi (např. Anorganické aminy a hydroxidy) za vzniku solí. K těmto neutralizačním reakcím dochází, když báze přijímá vodíkové ionty, které kyselina daruje.
-Neutralizace mohou v malých prostorech generovat nebezpečně velké množství tepla.
-Přidání vody ke kyselinám často vytváří v malé oblasti směsi dostatek tepla k explozivnímu varu této části vody, což může vést k velmi nebezpečným rozstřikům kyselin..
-Tyto materiály mají významnou kapacitu jako oxidační činidla, ale tato kapacita se liší od jednoho k druhému..
-Mohou reagovat s aktivními kovy (jako je železo a hliník) a také s mnoha méně aktivními kovy, aby rozpustily kov a uvolnily vodík a / nebo toxické plyny.
-Jeho reakce s kyanidovými solemi a jeho sloučeninami uvolňují plynný kyanovodík..
-Hořlavé a / nebo toxické plyny vznikají také jejich reakcemi s dithiokarbamáty, isokyanáty, merkaptany, nitridy, nitrily, sulfidy a slabými nebo silnými redukčními činidly..
-Další reakce vytvářející plyn se vyskytují u siřičitanů, dusitanů, thiosíranů (za vzniku H2S a SO3), dithionitů (SO2) a dokonce i uhličitanů: plynný oxid uhličitý není toxický, ale teplo a rozstřik z reakce mohou být narušeny.
-Roztoky kyseliny chloristé jsou silně oxidující kyselé roztoky.
-Mohou energicky reagovat nebo detonovat, když jsou smíchány s oxidovatelnými materiály (alkoholy, aminy, borany, dikyanogen, hydraziny, uhlovodíky, vodík, nitroalkany, práškové kovy, silany a thioly, mimo jiné).
-Kyselina chloristá se vznítí při kontaktu se sulfinylchloridem.
Toxicita
-Silné oxidační kyseliny jsou pro látky žíravé. Kyselé výpary vážně dráždí citlivé tkáně (jako jsou oči a dýchací systém).
-Vdechnutí, požití nebo kontakt (kůže, očí atd.) S roztoky kyseliny chloristé nebo s jejími parami může způsobit vážné zranění, popáleniny nebo smrt..
-Při kontaktu s ohněm mohou vytvářet dráždivé, leptavé a / nebo toxické plyny..
-Odtok z kontroly požáru nebo ředicí vody může způsobit kontaminaci.
Aplikace
-Kyselina chloristá se používá v oblastech vědeckého výzkumu a vývoje a při výrobě chemikálií a elektrických, elektronických a optických zařízení.
-Používá se jako prekurzor při výrobě čistého chloristanu amonného, základní přísady ve výbušninách a pevných pohonných látkách pro rakety a střely..
-Použití kyseliny chloristé v domácnosti zahrnuje toaletní, kovové a odtokové čističe, odstraňovače rzi, v bateriích a jako základ pro falešné nehty..
-Průmyslová použití zahrnují: zušlechťování kovů, instalatérství, bělení, leptání, galvanické pokovování, fotografování, dezinfekce, střelivo, výroba hnojiv, čištění kovů a odstraňování rzi.
-Kyselina chloristá se také v omezeném měřítku používá jako činidlo pro analytické účely..
Klinické účinky
Kyseliny způsobují koagulační nekrózu. Vodíkové ionty vysychají epiteliální buňky a způsobují otoky, erytém, vylučování tkání a nekrózu s tvorbou vředů a proleženin..
Při expozici těmto kyselinám gastrointestinálním způsobem se u pacientů mohou vyvinout popáleniny stupně II (povrchové puchýře, eroze a ulcerace), u kterých je riziko následného vzniku striktur, zejména žaludeční cesty a jícnu..
Mohou se také vyvinout hluboké popáleniny a nekróza gastrointestinální sliznice. Komplikace často zahrnují perforaci (jícnu, žaludek, zřídka duodenální), tvorbu píštěle (tracheoezofageální, aortoezofageální) a gastrointestinální krvácení..
Expozice vdechováním může způsobit dušnost, pleuritickou bolest na hrudi, kašel a bronchospazmus, otoky horních cest dýchacích a popáleniny. Edém horních cest dýchacích je běžný a často život ohrožující.
Expozice očí může způsobit silné podráždění spojivek a chemózy, epiteliální defekty rohovky, limbickou ischemii, trvalou ztrátu zraku a ve vážných případech perforaci..
Mírná dermální expozice může způsobit podráždění a popáleniny částečné tloušťky. Delší nebo vysoká koncentrace může způsobit popáleniny v plné tloušťce.
Komplikace mohou zahrnovat celulitidu, sepsi, kontraktury, osteomyelitidu a systémovou toxicitu.
Bezpečnost a rizika
Standardní věty o nebezpečnosti globálně harmonizovaného systému klasifikace a označování chemických látek (GHS)
Globálně harmonizovaný systém klasifikace a označování chemických látek (GHS) je mezinárodně schválený systém vytvořený Organizací spojených národů a navržený tak, aby nahradil různé standardy klasifikace a označování používané v různých zemích pomocí globálních konzistentních kritérií..
Třídy nebezpečnosti (a jejich odpovídající kapitola GHS), standardy klasifikace a označování a doporučení pro kyselinu chloristou jsou následující (Evropská chemická agentura, 2017; OSN, 2015; PubChem, 2017):
Prohlášení o nebezpečnosti podle GHS
H271: Může způsobit požár nebo výbuch; Silný oxidant [Nebezpečí Oxidující kapaliny; Oxidující pevné látky - kategorie 1] (PubChem, 2017).
H290: Může být korozivní pro kovy [Varování Korozivní pro kovy - kategorie 1] (PubChem, 2017).
H302: Zdraví škodlivý při požití [Varování Akutní toxicita, orální - Kategorie 4] (PubChem, 2017).
H314: Způsobuje těžké poleptání kůže a poškození očí [Nebezpečí Žíravost / dráždivost pro kůži - Kategorie 1A, B, C] (PubChem, 2017).
H318: Způsobuje vážné poškození očí [Nebezpečí Vážné poškození očí / podráždění očí - Kategorie 1] (PubChem, 2017).
H371: Může způsobit poškození orgánů [Varování Toxicita pro specifické cílové orgány, jednorázová expozice - Kategorie 2] (PubChem, 2017).
Kódy upozornění
P210, P220, P221, P234, P260, P264, P270, P280, P283, P301 + P312, P301 + P330 + P331, P303 + P361 + P353, P304 + P340, P305 + P351 + P338, P306 + P360, P309 + P311, P310, P321, P330, P363, P370 + P378, P371 + P380 + P375, P390, P404, P405 a P501 (PubChem, 2017).





Reference
- Evropská agentura pro chemické látky (ECHA). (2016). Kyselina chloristá. Stručný profil. Citováno dne 8. února 2017 z: echa.europa.eu.
- JSmol (2017) Kyselina chloristá. [obrázek] Obnoveno z: chemapps.stolaf.edu.
- NASA (2008) Ares-1 launch 02-2008 [image] Obnoveno z: commons.wikimedia.org.
- Národní centrum pro biotechnologické informace. Složená databáze PubChem. (2017). Kyselina chloristá - struktura PubChem. [obrázek] Bethesda, MD, EU: National Library of Medicine. Obnoveno z: pubchem.ncbi.nlm.nih.gov.
- Oelen, W. (2011) Perchloric acid 60 percent [obrázek] Obnoveno z: en.wikipedia.org.
- Wikipedia. (2017). Kyselina chloristá. Citováno 8. února 2017 z: es.wikipedia.org.
- Wikipedia. (2017). Kyselina chloristá. Citováno 8. února 2017 z: es.wikipedia.org.



Zatím žádné komentáře