
Struktura, vlastnosti a použití oxidu arsenitého (As2O3)
The oxid arzenitý je anorganická sloučenina, jejíž chemický vzorec je AsdvaNEBO3. Arsen v kovovém stavu se rychle přeměňuje na tento oxid, což je velmi toxický jed, který může mít akutní a chronické projevy..
Protože arzen a kyslík jsou prvky p bloku, s relativně nízkým rozdílem elektronegativity se očekává, že AsdvaNEBO3 je složen z kovalentní povahy; to znamená, že vazby As-O převládají v pevné látce nad elektrostatickými interakcemi mezi ionty As3+ mědva-.

Akutní intoxikace oxidem arsenitým nastává požitím nebo vdechnutím, jejichž nejdůležitějšími projevy jsou: závažné gastrointestinální poruchy, křeče, oběhový kolaps a plicní edém..
Navzdory své toxicitě se však průmyslově používá; například při ochraně dřeva, při výrobě pigmentů, polovodičů atd. Podobně se dříve používal při léčbě mnoha nemocí.
Oxid arsenitý je amfoterní sloučenina, rozpustná ve zředěných kyselinách a louzích, nerozpustná v organických rozpouštědlech a relativně rozpustná ve vodě. Vyskytuje se jako pevná látka (horní obrázek) se dvěma krystalickými formami: kubickou a monoklinickou.
Rejstřík článků
- 1 Struktura oxidu arzenitého
- 1.1 Klaudetit
- 1.2 Kapalné a plynné
- 1.3 Arsenolit
- 2 Vlastnosti
- 2.1 Obchodní názvy
- 2.2 Molekulová hmotnost
- 2.3 Fyzický vzhled
- 2.4 Zápach
- 2.5 Příchuť
- 2.6 Bod varu
- 2.7 Teplota tání
- 2.8 Bod vzplanutí
- 2.9 Rozpustnost ve vodě
- 2.10 Rozpustnost
- 2.11 Hustota
- 2.12 Tlak par
- 2.13 Rozklad
- 2.14 Žíravost
- 2.15 Odpařovací teplo
- 2.16 Disociační konstanta (Ka)
- 2.17 Index lomu
- 3 Reaktivita
- 4 Názvosloví
- 5 použití
- 5.1 Průmyslové
- 5.2 Lékaři
- 6 Reference
Struktura oxidu arzenitého
Claudetita
Při pokojové teplotě, AsdvaNEBO3 krystalizuje do dvou monoklinických polymorfů, které se nacházejí v minerálu klaudetitu. Mají trigonální pyramidové jednotky AsO3, které jsou spojeny svými atomy kyslíku, aby kompenzovaly elektronický nedostatek jednotky samostatně.
V polymorfu jsou jednotky AsO3 jsou spojeny tvořícími se řádky (klaudetit I) a na druhé jsou spojeny, jako by tkali síť (klaudetit II):
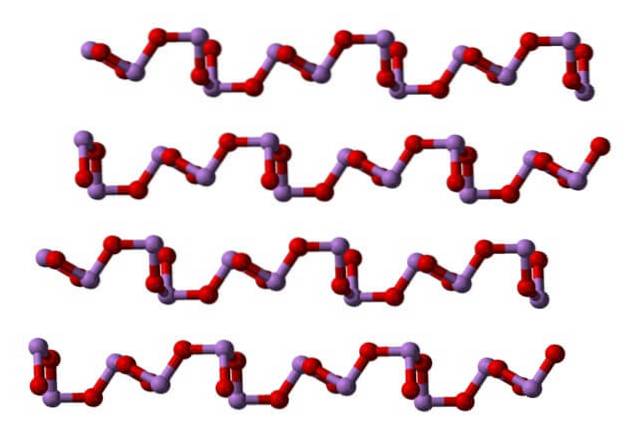
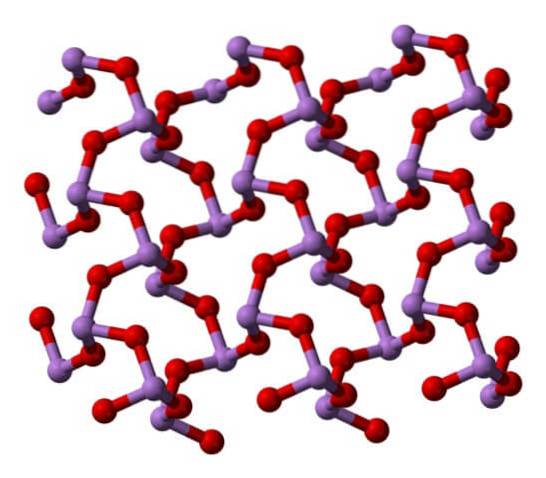
Kapalné a plynné
Když jsou všechny ty struktury, které definují monoklinické krystaly, zahřáté, vibrace jsou takové, že se rozbije několik vazeb As-O a převažuje menší molekula: As4NEBO6. Jeho struktura je znázorněna na obrázku níže.

Dalo by se říci, že se skládá z dimeru AsdvaNEBO3. Jeho stabilita je taková, že podporuje 800 ° C v plynné fázi; ale nad touto teplotou se fragmentuje na molekuly AsdvaNEBO3.
Arsenolit
Stejné eso4NEBO6 mohou vzájemně interagovat a krystalizovat do kubické pevné látky, jejíž struktura se nachází v minerálním arsenolitu.
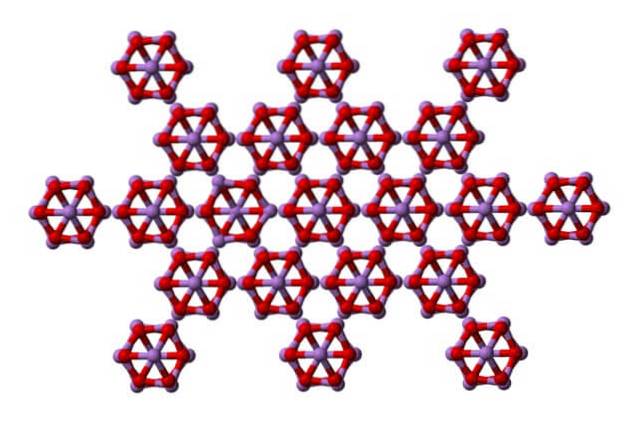
Všimněte si, že obrázek ukazuje strukturu z vyšší roviny. Ve srovnání s klaudetitem je zřejmý jeho strukturální rozdíl s arsenolitem. Tady jsou diskrétní molekuly As4NEBO6 že jednotky jsou udržovány Van der Waalsovými silami.
Vlastnosti
Obchodní názvy
-Arsenolit
-Arsodent
-Trisenox
-Claudetita
Molekulární váha
197,84 g / mol.
Fyzický vzhled
-Bílé krychlové krystaly (arsenolit).
-Bezbarvé monoklinické krystaly (klaudetit).
-Bílá nebo průhledná pevná látka, sklovité, amorfní hrudky nebo krystalický prášek.
Zápach
Toaleta.
Chuť
Bez chuti.
Bod varu
460 ° C.
Bod tání
-313 ° C (klaudetit).
-274 ° C (arsenolit).
bod vznícení
485 ° C (sublimáty).
Rozpustnost ve vodě
17 g / L při 18 ° C (20 g / L při 25 ° C).
Rozpustnost
Rozpustný v kyselinách (zejména kyselině chlorovodíkové) a zásadách. Prakticky nerozpustný v chloroformu a etheru.
Hustota
-3,85 g / cm3 (krychlové krystaly);
-4,15 g / cm3 (kosočtverečné krystaly).
Tlak páry
2,47 10-4 mmHg při 25 ° C.
Rozklad
Není hořlavý, ale při zahřívání může vytvářet toxický kouř, který může zahrnovat i arsin..
Žíravost
V přítomnosti vlhkosti může být korozivní pro kovy.
Odpařovací teplo
77 kJ / mol.
Disociační konstanta (Ka)
1110-4 při 25 ° C.
Index lomu
-1755 (arsenolit)
-1,92 - 2,01 (klaudetit).
Reaktivita
-Oxid arsenitý je amfoterní sloučenina, ale funguje přednostně jako kyselina.
-Může reagovat s kyselinou chlorovodíkovou nebo kyselinou fluorovodíkovou za vzniku chloridu arzenitého nebo fluoridu arzenitého.
-Stejně tak reaguje se silnými oxidanty, jako je kyselina dusičná, což způsobuje kyselinu arsenovou a oxid dusný..
-Oxid arsenitý může reagovat s kyselinou dusičnou za vzniku arsinu nebo prvku arsen v závislosti na reakčních podmínkách..
EsodvaNEBO3 + 6 Zn + 12 HNO3 => 2 AsH3 + 6 Zn (č3)dva + 3 HdvaNEBO.
Tato reakce sloužila jako základ pro vytvoření Marshova testu, který se používal k detekci otravy arsenem..
Nomenklatura
NadvaNEBO3 Lze jej pojmenovat podle následujících nomenklatur s vědomím, že arzen pracuje s valencí +3:
-Oxid arsenitý (tradiční názvosloví).
-Oxid arsenitý (základní nomenklatura).
-Oxid diarseničitý (systematické názvosloví).
Aplikace
Průmyslový
-Používá se při výrobě skla, konkrétně jako bělícího prostředku. Používá se také při výrobě keramiky, elektronických výrobků a zábavní pyrotechniky.
-Přidává se jako vedlejší složka do slitin na bázi mědi, aby se zvýšila korozní odolnost slitinových kovů.
-EsodvaNEBO3 je výchozím materiálem pro přípravu elementárního arzenu, pro zlepšení elektrických spojů a pro výrobu arzenidových polovodičů
-EsodvaNEBO3, stejně jako arzeničnan měďnatý se používají jako konzervační prostředky na dřevo. To bylo používáno v kombinaci s octanem měďnatým k výrobě pařížského zeleného pigmentu, který se používá k výrobě barev a rodenticidů..
Lékaři
-Oxid arsenitý je sloučenina, která se po staletí používá při léčbě mnoha nemocí. Používal se jako tonikum při léčbě poruch výživy, neuralgie, revmatismu, artritidy, astmatu, chorea, malárie, syfilisu a tuberkulózy..
-Podobně se používá při lokální léčbě kožních onemocnění a používá se ke zničení některých povrchových epiteliomů..
-Fowlerovo řešení bylo používáno k léčbě kožních onemocnění a leukémie. Užívání tohoto léku je přerušeno..
-V 70. letech provedl čínský výzkumník Zhang Tingdong výzkum týkající se použití oxidu arzenitého při léčbě akutní promyelocytární leukémie (APL). Což vedlo k výrobě léku Trisenox, který byl schválen americkým FDA.
-Přípravek Trisenox byl použit u pacientů s APL, kteří nereagují na léčbu „první linie“, sestávající z kyseliny all-trans retinové (ATRA). Bylo prokázáno, že oxid arsenitý indukuje apoptózu rakovinných buněk.
-Trisenox se používá jako cytostatikum při léčbě refrakterního promyelocytárního podtypu (M3) společností APL.
Reference
- Shen a kol. (2001). Studie klinické účinnosti a farmakokinetiky nízkodávkovaného oxidu arsenitého v léčbě relabující akutní promyelocytární leukémie: srovnání s konvenčním dávkováním. Leukemia 15, 735-741.
- Science Direct. (2014). Oxid arsenitý. Sevier. Obnoveno z: sciencedirect.com
- Wikipedia. (2019). Oxid arsenitý. Obnoveno z: en.wikipedia.org
- PubChem. (2019). Oxid arzenitý. Obnoveno z: pubchem.ncbi.nlm.nih.gov
- Deborah M. Rusta a Steven L. Soignetb. (2001). Profil rizika a přínosu oxidu arsenitého. The Oncologist sv. 6 Dodatek 2 29-32.
- The New England Journal of Medicine. (11. července 2013). Kyselina retinová a oxid arsenitý pro akutní promyelocytární leukémii. n engl j med 369; 2.



Zatím žádné komentáře