
Struktura uracilu, funkce, vlastnosti, syntéza
The uracil Jedná se o dusíkatou bázi pyrimidinového typu, která se nachází v ribonukleové kyselině (RNA). To je jedna z charakteristik, které odlišují RNA od deoxyribonukleové kyseliny (DNA), protože ta má místo uracilu thymin. Obě látky, uracil a thymin, se liší pouze tím, že druhá obsahuje methylovou skupinu.
Z evolučního hlediska bylo navrženo, že RNA byla první molekulou, která uchovávala genetickou informaci a fungovala jako katalyzátor v buňkách před DNA a enzymy. Z tohoto důvodu se předpokládá, že uracil hrál klíčovou roli ve vývoji života.
U živých organismů se uracil nenachází ve volné formě, ale běžně tvoří nukleotidy monofosfát (UMP), difosfát (UDP) a trifosfát (UTP). Tyto uracilové nukleotidy mají různé funkce, jako je biosyntéza RNA a glykogenu, izomerní interkonverze cukrů a regulace glutamin syntázy..
Rejstřík článků
- 1 Struktura a vlastnosti
- 2 Biosyntéza
- 2.1 Regulace biosyntézy
- 3 Role v biosyntéze RNA
- 4 Role v biosyntéze cukru
- 5 Role v izomerní interkonverzi cukrů
- 6 Role v biosyntéze glykoproteinů
- 7 Úloha v regulaci glutamin syntázy
- 8 Role v editaci RNA
- 9 Biosyntéza UDP-glukózy
- 10 Uracil DNA glykosyláza
- 11 Reference
Struktura a vlastnosti
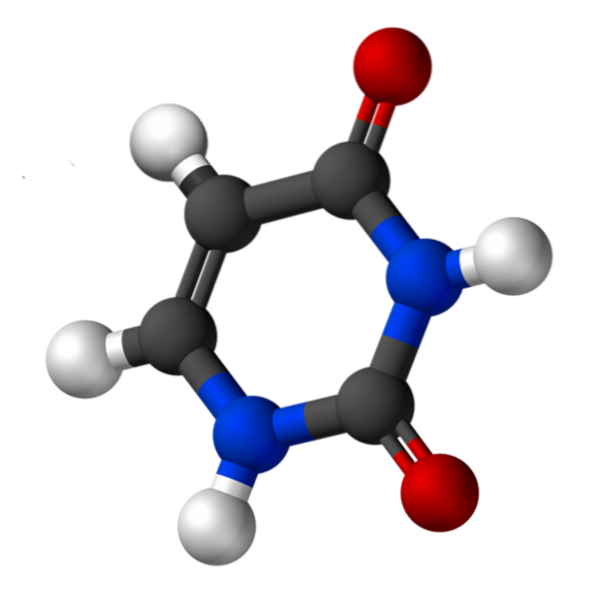
Uracil, nazývaný 2,4-dioxypyridin, má empirický vzorec C4H4NdvaNEBOdva, jehož molekulová hmotnost je 112,09 g / mol a je čištěn jako bílý prášek.
Struktura uridinu je heterocyklický kruh se čtyřmi atomy uhlíku a dvěma atomy dusíku, se střídavými dvojnými vazbami. Je rovinný.
Má rozpustnost 50 mg / ml při 25 ° C v 1M hydroxidu sodném a pKa mezi 7,9 a 8,2. Vlnová délka, kde dochází k jeho maximální absorbanci (ʎmax) je mezi 258 a 260 nm.
Biosyntéza
Existuje společná cesta pro biosyntézu pyrimidinových nukleotidů (uracil a cytokin). Prvním krokem je biosyntéza karbamoylfosfátu z COdva a NH4+, který je katalyzován karbamoylfosfát syntetázou.
Pyrimidin je vyroben z karboylfosfátu a aspartátu. Obě látky reagují a vytvářejí N-karbamoylaspartát, reakci katalyzovanou aspartát-transkobamoylázou (ATCase). Uzavření pyrimidinového kruhu je způsobeno dehydratací katalyzovanou dihydrootázou a produkuje L-dihydrorotát..
L-dihydrorotát se oxiduje a převádí na orotát; akceptor elektronů je NAD+. Jedná se o reakci katalyzovanou dihydroorotátdehydrogenázou. Dalším krokem je přenos fosforibosylové skupiny z fosforibosylpyrofosfátu (PRPP) na orotát. Vytváří orotidylát (OMP) a anorganický pyrofosfát (PPi), katalyzovaný orotátfosforibosyltransferázou.
Poslední krok spočívá v dekarboxylaci pyrimidinového kruhu orotidylátu (OMP). Vytváří uridylát (uridin-5'-monofosfát, UMP), který je katalyzován dekarboxylázou.
Poté, prostřednictvím účasti kinázy, je fosfátová skupina přenesena z ATP na UMP za vzniku UDP (uridin-5'-difosfát). Ten se opakuje a tvoří se UTP (uridin-5'-trifosfát).
Regulace biosyntézy
U bakterií dochází k regulaci biosyntézy pyrimidinu prostřednictvím negativní zpětné vazby na úrovni aspartát-transkobamoylázy (ATCase).
Tento enzym je inhibován CTP (cytidin-5'-trifosfát), který je konečným produktem biosyntetické dráhy pyrimidinu. ATCase má regulační podjednotky, které se vážou na alosterický regulátor CTP.
U zvířat dochází k regulaci biosyntézy pyrimidinu prostřednictvím negativní zpětné vazby na úrovni dvou enzymů: 1) karbamoylfosfát syntáza II, která je inhibována UTP a aktivována ATP a PRPP; a 2) OMP dekarboxyláza, která je inhibována produktem reakce, kterou katalyzuje, UMP. Rychlost biosyntézy OMP se liší podle dostupnosti PRPP.
Role v biosyntéze RNA
Uracil je přítomen ve všech typech RNA, jako je messenger RNA (mRNA), transferová RNA (tRNA) a ribozomální RNA (rRNA). K biosyntéze těchto molekul dochází prostřednictvím procesu zvaného transkripce..
Během transkripce jsou informace obsažené v DNA kopírovány do RNA pomocí RNA polymerázy. Reverzní proces, při kterém jsou informace obsažené v RNA kopírovány do DNA, se vyskytuje u některých virů a rostlin prostřednictvím reverzní transkriptázy..
Biosyntéza RNA vyžaduje nukleosid trifosfát (NTP), a to: uridin trifosfát (UTP), cytidin trifosfát (CTP), adenin trifosfát (ATP) a guanin trifosfát (GTP). Reakce je:
(RNA)n zbytků + NTP -> (RNA)n + 1 zbytek + PPi
Hydrolýza anorganického pyrofosfátu (PPi) poskytuje energii pro biosyntézu RNA.
Role v biosyntéze cukru
Estery cukru jsou v živých organismech velmi časté. Některé z těchto esterů jsou nukleosidové estery difosfáty, jako jsou UDP-cukry, které jsou v buňkách velmi hojné. UDP-cukry se účastní biosyntézy disacharidů, oligosacharidů a polysacharidů.
V rostlinách dochází k biosyntéze sacharózy dvěma cestami: primární a sekundární.
Hlavní cestou je přenos D-glukózy z UDP-D-glukózy na D-fruktózu za vzniku sacharózy a UDP. Sekundární cesta zahrnuje dva kroky: začíná UDP-D-glukózou a fruktóza-6-fosfátem a končí tvorbou sacharózy a fosfátu..
V mléčných žlázách dochází k biosyntéze laktózy z UDP-D-galaktózy a glukózy.
V rostlinách se biosyntéza celulózy provádí kontinuální kondenzací zbytků beta-D-glukosylu z UDP-glukózy na neredukující konec rostoucího polyglukózového řetězce. Podobně biosyntéza amylózy a amylopektinu vyžaduje UDP-glukózu jako substrát donoru glukózy pro rostoucí řetězec..
U zvířat se pro biosyntézu glykogenu používají jak UDP-glukóza, tak ADP-glukóza. Podobně biosyntéza chondroitin sulfátu vyžaduje UDP-xylózu, UDP-galaktózu a UDP-glukuronát..
Role v izomerní interkonverzi cukrů
Ke konverzi galaktózy na glykolýzní meziprodukt dochází cestou Leloir. Jeden z kroků v této dráze je katalyzován enzymem UDP-galaktóza-4-epimerázou, který usnadňuje interkonverzi UDP-galaktózy na UDP-glukózu..
Role v biosyntéze glykoproteinů
Během biosyntézy glykoproteinu proteiny procházejí cis, střední a trans vaky Golgiho aparátu.
Každý z těchto vaků má sadu enzymů, které zpracovávají glykoproteiny. Cukrové monomery, jako je glukóza a galaktóza, se přidávají k proteinovému oligosacharidu z UDP-hexózy a dalších nukleotidů-hexózy.
Hexózové nukleotidy jsou transportovány do Golgiho cisteren antiportem. UDP-galaktóza (UDP-Gal) a UDP-N-acetylgalaktosamin (UDP-GalNAc) vstupují do cisteren z cytosolu výměnou za UMP.
V Golgiho cisterně fosfatáza hydrolyzuje fosfátovou skupinu na UDP a tvoří UMP a Pi. UDP pochází z reakcí katalyzovaných galaktosyltransferázou a N-acetylgalaktosamyltransferázou. UMP tvořený fosfatázou slouží k výměně nukleotid-hexóza.
Role v regulaci glutamin syntázy
Regulačním mechanismem glutamin syntázy je kovalentní modifikace, která spočívá v adenylaci, která ji deaktivuje, a dedenylaci, která ji aktivuje. Tato kovalentní modifikace je reverzibilní a katalyzovaná adenyltransferázou..
Aktivita adenyltransferázy je modulována vazbou proteinu PII, která je regulována kovalentní modifikací, uridinylací.
Uridylace i deuridylace se provádějí uridylyltransferázou. V tomto enzymu je uridylační aktivita způsobena glutaminem a fosfátem a je aktivována vazbou alfa-ketoglutarátu a ATP na PII.
Role v editaci RNA
Některé mRNA jsou před překladem upraveny. U některých eukaryotických organismů, jako je např Trypanosoma brucei, probíhá RNA editace transkriptu genu podjednotky II cytochromoxidázy. K tomu dochází inzercí zbytků uracilu, reakcí katalyzovanou terminální uridyltransferázou..
Průvodce RNA, doplňující upravený produkt, funguje jako šablona pro proces úpravy. Páry bází vytvořené mezi počátečním transkriptem a vodicí RNA implikují páry bází G = U, které nejsou Watson-Crick a jsou v RNA běžné..
Biosyntéza UDP-glukózy
Za fyziologických podmínek je biosyntéza glykogenu z glukóza-1-fosfátu termodynamicky nemožná (ΔG pozitivní). Díky tomu před biosyntézou dochází k aktivaci glukóza-1-fosfátu (G1P). Tato reakce kombinuje G1P a UTP za vzniku uridindifosfátové glukózy (UDP-glukózy nebo UDPG)..
Reakce je katalyzována UDP-glukóza pyrofosforylázou a je následující:
G1P + UTP -> UDP-glukóza + 2Pi.
Variace volné Gibbsovy energie v tomto kroku je velká a negativní (-33,5 KJ / mol). Během reakce na kyslík G1P napadá atom alfa fosforu UTP a tvoří UDP-glukózu a anorganický pyrofosfát (PPi). Dále je PPi hydrolyzován anorganickou pyrofosfatázou, jejíž hydrolýzní energie řídí obecnou reakci.
UDP-glukóza je látka s „vysokou energií“. Umožňuje vytvářet glykosidické vazby mezi glukózovým zbytkem a rostoucím polysacharidovým řetězcem. Stejný energetický princip je použitelný pro reakce, na nichž se podílejí UDP-cukry, jako je biosyntéza disacharidů, oligosacharidů a glykoproteinů..
Uracil DNA glykosyláza
Existují léze DNA, které se vyskytují spontánně. Jednou z těchto lézí je spontánní deaktivace cytokinu a jeho následná přeměna na uracil. V tomto případě probíhá oprava odstraněním modifikované DNA báze enzymem nazývaným uracil DNA glykosyláza..
Enzym uracil DNA glykosyláza odstraňuje poškozený cytokin (uracil) za vzniku zbytku deoxyribózy, který postrádá dusíkatou bázi, nazývanou místo AP (apurinicko-apyrimidinové místo).
Enzym AP endonukleáza poté štěpí fosfodiesterovou kostru místa AP a odstraní zbytek cukr-fosfát. DNA polymeráza I obnovuje poškozené vlákno.
Reference
- Bohinski, R. 1991. Biochemistry. Addison-Wesley Iberoamericana, Wilmington, Delaware.
- Devlin, T.M. 2000. Biochemie. Redakční Reverté, Barcelona.
- Lodish, H., Berk, A., Zipurski, S.L., Matsudaria, P., Baltimore, D., Darnell, J. 2003. Buněčná a molekulární biologie. Redakční Medica Panamericana, Buenos Aires, Bogotá, Caracas, Madrid, Mexiko, Sāo Paulo.
- Nelson, D. L., Cox, M. M. 2008. Lehninger-Principles of biochemistry. W.H. Freeman, New York.
- Voet, D. a Voet, J. 2004. Biochemistry. John Wiley and Sons, USA.


Zatím žádné komentáře