
Složky extrapyramidové dráhy, funkce, dráha, nemoci

Pojem extrapyramidový přístup nebo extrapyramidový systém (SEP) vznikl jako výsledek anatomických a fyziologických studií zaměřených na pochopení způsobu, jakým centrální nervový systém řídil aktivitu kosterních svalů, s cílem, aby tělo zaujalo vhodné držení těla a vytvořilo dobrovolné pohyby.
V tomto procesu bylo zjištěno, že kontrola svalové aktivity vyžaduje kontrolu motorických neuronů předního rohu míchy, jediné spojení mezi centrálním nervovým systémem a vlákny kosterního svalstva a že tato kontrola byla prováděna nervovými projekcemi z mozkových center. lepší.
Mezi těmito projekcemi je důležitá dráha tvořena některými axony, které pocházejí z motorických oblastí mozkové kůry a sestupují přímo, tj. Bez šupin, do míchy, přičemž se při některých výběžcích spojují při průchodu míchy. které díky svému tvaru dostaly název „pyramidy“.
Tento trakt se nazýval „pyramidový trakt“ nebo „kortikospinální trakt“ a podílel se na ovládání jemných a obratných pohybů prováděných distálními částmi končetin, zatímco existence struktur s motorickou funkcí byla rozpoznána, ale nebyla zahrnuta. tímto způsobem (extra).
Termín „extrapyramidový motorický systém“, který je z fyziologického hlediska již zastaralý, se v klinickém žargonu stále používá k označení těch struktur mozku a mozkového kmene, které spolupracují při kontrole motoru, ale nejsou součástí pyramidového systému nebo přímého kortikospinálního systému.
Rejstřík článků
- 1 Anatomické komponenty a funkce pyramidové dráhy
- 1.1 - Jádra mozkového kmene
- 1.2 - Bazální ganglia
- 1.3 - Konektivita, dráha a neurochemie v bazálních gangliích
- 2 Nemoci bazálních ganglií
- 2.1 Huntingtonova choroba
- 2.2 Hemibalismus
- 2.3 Parkinsonova choroba
- 3 Odkazy
Anatomické komponenty a funkce pyramidové dráhy
Extrapyramidovou dráhu lze popsat jako organizovanou do dvou skupin složek: jedna by byla tvořena souborem jader mozkového kmene a jeho výčnělků směrem k míše a druhá by byla tvořena subkortikálními jádry známými jako jádra nebo bazální ganglia..
- Jádra mozkového kmene
V mozkovém kmeni existují skupiny neuronů, jejichž axony vyčnívají k šedé hmotě míchy a které byly popsány jako uspořádané do dvou systémů: jednoho mediálního a druhého laterálního..
Mediální systém
Mediální systém je tvořen vestibulospinálním, retikulospinálním a tektospinálním traktem, které sestupují ventrálními šňůrami šňůry a kromě proximálních svalů končetin zapojených do držení těla vykonávají kontrolu nad axiálními nebo kmenovými svaly..
Boční systém
Nejdůležitější složkou laterálního systému je rubrospinální trakt, jehož axony vyčnívají z červeného jádra středního mozku, sestupují postranní šňůrou šňůry a nakonec ovlivňují motorické neurony, které ovládají distální svaly končetin..
Z výše uvedeného lze odvodit, že mediální systém spolupracuje na základních posturálních úpravách nezbytných pro dobrovolnou motorickou činnost, zatímco laterální systém se zabývá, společně s přímou kortikospinální cestou, s pohyby končetin zaměřenými na účel, jako je dosahování a manipulace s předměty.
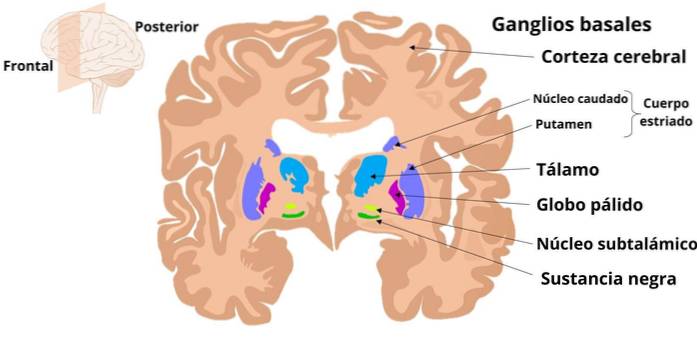
- Bazální ganglia
Bazální ganglia jsou subkortikální neuronální struktury, které se podílejí na zpracování motorických informací, jako je plánování a programování složitých obratných pohybů, a jejichž změny dávají klinické projevy, které jsou seskupeny do syndromů známých jako „extrapyramidové“.
Ganglie zahrnují striatum, které je tvořeno putamenem a jádrem caudate; bledý glóbus, který má vnější část (GPe) a vnitřní část (GPi); substantia nigra, uspořádaná do kompaktní části (SNc) a síťované části (SNr), a subtalamické nebo Lewisovo jádro.
Tyto struktury fungují tak, že přijímají informace hlavně z různých oblastí mozkové kůry; informace, které aktivují vnitřní obvody ovlivňující výstupní neuronální aktivitu, která se vrací přes motorickou část thalamu do mozkové kůry.
- Konektivita, dráha a neurochemie v bazálních gangliích
Informace o gangliích vstupují skrz striatum (caudate a putamen). Odtamtud začínají cesty, které se spojují s výstupními jádry, kterými jsou GPi a SNr, jejichž axony jdou do ventroanteriálních a ventrolaterálních jader thalamu, které zase vyčnívají do kůry.
Různá stadia obvodu jsou pokryta neurony, které patří do určitého neurochemického systému a které mohou mít inhibiční nebo excitační účinek. Kortikálně pruhovaná spojení, thalamicko-kortikální a subtalamická vlákna uvolňují glutamát a jsou excitační.
Neurony, jejichž axony opouštějí striatum, používají jako hlavní neurotransmiter kyselinu gamaaminomáselnou (GABA) a jsou inhibiční. Existují dvě subpopulace: jedna syntetizuje látku P jako kotransmiter [GABA (+ Subst. P)] a druhá enkefalin [GABA (+ Encef.)].
GABA neurony (+ Subst. P)
Neurony GABA (+ Sust. P) mají dopaminové receptory D1 a jsou excitovány dopaminem (DA); také vytvářejí přímé inhibiční spojení s vývody bazálních ganglií (GPi a SNr), které jsou také GABAergní, ale „+ dynorphin“, a inhibují glutamátergní buňky thalamicko-kortikální projekce.
GABA neurony (+ encef.)
GABA (+ Encef.) Neurony mají dopaminové D2 receptory a jsou dopaminem inhibovány. Navazují nepřímé excitační spojení s výstupy (GPi a SNr), protože promítají do GPe inhibující jeho GABAergní neurony, které inhibují glutamatergické neurony subtalamického jádra, jejichž funkcí je aktivovat výstupy (GPi a SNr).
Kompaktní část substantia nigra (SNc) má dopaminergní neurony (DA), které se spojují s vytvářením striata, jak již bylo zmíněno, excitační D1 na buňkách GABA (+ Sub. P) a inhibiční D2 na buňkách GABA (+ Encef.).
Poté a v souladu s výše uvedeným končí aktivace přímé dráhy inhibicí výstupů bazálních ganglií a uvolněním aktivity v thalamicko-kortikálních spojeních, zatímco aktivace nepřímé dráhy aktivuje výstupy a snižuje thalamickou aktivitu. -kortikální.
Ačkoli interakce a přesné společné fungování přímých a nepřímých cest, o nichž se uvažuje, nebyly objasněny, popsaná anatomická a neurochemická organizace nám pomáhá alespoň částečně porozumět některým patologickým stavům vyplývajícím z dysfunkce bazálních ganglií.
Onemocnění bazálních ganglií
Ačkoli patologické procesy, které se usazují v bazálních gangliích, mají různorodou povahu a ovlivňují nejen určité motorické funkce, ale také kognitivní, asociativní a emoční funkce, v klinických obrazech zaujímají motorické změny významné místo a většina výzkumu se na ně zaměřila.
Pohybové poruchy typické pro dysfunkci bazálních ganglií lze rozdělit do jedné ze tří skupin, a to:
- Hyperkinézy, jako je Huntingtonova choroba nebo chorea a hemibalismus.
- Hypokineze, jako je Parkinsonova choroba.
- Dystonie, jako je atetóza.
Obecně lze říci, že hyperkinetické poruchy charakterizované nadměrnou motorickou aktivitou vykazují snížení inhibice, kterou výstupy (GPi a SNr) působí na thalamicko-kortikální projekce, které se stávají aktivnějšími.
Hypokinetické poruchy jsou naopak doprovázeny zvýšením této inhibice se snížením thalamicko-kortikální aktivity.
Huntingtonova choroba
Jedná se o hyperkinetickou poruchu charakterizovanou nedobrovolným a spasmodickým náhodným třesením končetin a orofaciální oblasti, choreiformními nebo „tanečními“ pohyby, které se postupně zvyšují a invalidizují, poruchy řeči a progresivní vývoj demence.
Onemocnění je brzy doprovázeno degenerací striatálních neuronů GABA (+ Encef.) Nepřímé dráhy.
Protože tyto neurony již neinhibují GPe GABAergní neurony, nadměrně inhibují subthalamické jádro, které přestává excitovat inhibiční výstupy (GPi a SNr) a thalamicko-kortikální projekce jsou deaktivovány..
Hemibalismus
Skládá se z násilných kontrakcí proximálních svalů končetin, které se při síle pohybů s velkou amplitudou promítají silou. Poškozením v tomto případě je degenerace subtalamického jádra, která vede k něčemu podobnému tomu, které bylo popsáno pro chorea, i když ne hyperinhibicí, ale destrukcí subtalamického jádra.
Parkinsonova choroba
Vyznačuje se obtížemi a zpožděním při zahájení pohybů (akineze), zpomalení pohybů (hypokineze), výrazu obličeje nebo obličeje v masce bez výrazu, změně chůze se sníženými přidruženými pohyby končetin během pohybu a třesu v klidu v klidu.
Poškození v tomto případě spočívá v degeneraci nigrostriatálního systému, což jsou dopaminergní projekce, které vycházejí z kompaktní oblasti substantia nigra (SNc) a spojují se s striatálními neurony, které vedou k přímé a nepřímé dráze..
Potlačení excitace, kterou dopaminergní vlákna vyvíjejí na GABA (+ Sust. P) buňky přímé dráhy, odstraňuje inhibici, kterou tyto působí na GABAergní vývody (GPi a SNr) směrem k thalamu, který je nyní více inhibován. intenzita. Jedná se pak o dezinhibici výstupů.
Na druhou stranu potlačení inhibiční aktivity, kterou dopamin působí na buňky GABA (+ Encef.) Z nepřímé dráhy je uvolňuje a zvyšuje inhibici, kterou působí na buňky GABA GPe, což dezinhibuje neurony jádro subtalamické, které pak hyperaktivuje výstupy.
Jak je vidět, konečný výsledek účinků dopaminergní degenerace na dvě vnitřní cesty, přímou a nepřímou, je stejný, ať už je to disinhibice nebo stimulace GABAergních výstupů (GPi a SNr), které inhibují thalamická jádra a snižují jejich výstup do kůry, což vysvětluje hypokinézu
Reference
- Ganong WF: Reflexní a dobrovolná kontrola držení těla a pohybu, v: Recenze lékařské fyziologie, 25. vydání New York, McGraw-Hill Education, 2016.
- Guyton AC, Hall JE: Příspěvky mozečku a bazální ganglie k celkové kontrole motoru, v: Učebnice lékařské fyziologie, 13. vydání, AC Guyton, JE Hall (eds). Philadelphia, Elsevier Inc., 2016.
- Illert M: Motorisches System: Basalganglien, In: Physiologie, 4. vydání; P Deetjen a kol. (Eds). München, Elsevier GmbH, Urban & Fischer, 2005.
- Luhmann HJ: Sensomotorische systeme: Kórperhaltung und Bewegung, in: Fyziologie, 6. vydání; R. Klinke a kol. (Eds). Stuttgart, Georg Thieme Verlag, 2010.
- Oertel WH: Basalganglienerkrankungen, v: Physiologie des Menschen mit Pathophysiologie, 31. vydání, RF Schmidt et al (eds). Heidelberg, Springer Medizin Verlag, 2010.
- Wichmann T a DeLong MR: The Basal Ganglia, In: Principles of Neural Science, 5. vydání; E. Kandel a kol. (Eds). New York, McGraw-Hill, 2013.



Zatím žádné komentáře