
Struktura, vlastnosti chlornanu draselného (KOCl)
The chlornan draselný Je to draselná sůl kyseliny chlorné. Je to také ternární sůl draslíku, kyslíku a chloru a představuje anorganickou sloučeninu. Jeho chemický vzorec je KOCl, což znamená, že kation K se nachází v iontové pevné látce.+ a anion OCl- ve stechiometrickém poměru 1: 1.
Z jejich homologních sloučenin (LiOCl, NaOCl, Ca (OCl)dva) je možná nejméně používaný a populárně známý v chemické a pragmatické kultuře. Všechny tyto soli mají společného jmenovatele chlornanového aniontu (OCl-), což jim dává jejich hlavní vlastnosti bělícího prostředku.
Historie chlornanu draselného a jeho fyzikálně-chemické vlastnosti jsou podobné jako s chlornanem sodným. To bylo původně produkováno v roce 1789 Claude Louis Berthollet v Javel, Paříž. Reakce autora, která vedla k syntéze uvedené sloučeniny, je vyjádřena následující chemickou rovnicí:
Cldva + 2KOH => KCl + KClO + HdvaNEBO
Podle rovnice reaguje molekulární chlor s hydroxidem draselným (nebo s hydroxidem draselným), čímž redukuje a oxiduje atomy chloru. To lze ověřit porovnáním oxidačního čísla Cl v KCl (-1) s množstvím Cl v KClO (+1).
Rejstřík článků
- 1 Chemická struktura
- 2 Názvosloví
- 3 Vlastnosti
- 3.1 Molární hmotnost
- 3.2 Vzhled
- 3.3 Hustota
- 3.4 Bod tání
- 3.5 Bod varu
- 3.6 Rozpustnost ve vodě
- 3.7 Reaktivita
- 4 použití
- 5 Reference
Chemická struktura

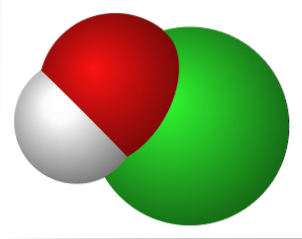
Horní obrázek představuje elektrostatické interakce mezi kationtem K.+ a anion OCl- (s kyslíkem nesoucím záporný formální náboj).
Tyto ionty mají stejné stechiometrické proporce (1: 1) a jejich nesměrové síly tvoří krystalické uspořádání, kde K+ je umístěn co nejblíže atomu O.
Ačkoli neexistují žádné studie, které by popisovaly krystalový systém KOCl (kubický, ortorombický, monoklinický atd.), Stačí jej vizualizovat jako velkou sféru K+ přitahován iontem lineární geometrie OCl-.
Lze si myslet, že na rozdíl od NaOCl tvoří KOCl krystaly s nižší energií mřížky, protože K+ je větší než Na+ ve srovnání s OCl-. Tato větší odlišnost mezi jejich iontovými poloměry snižuje elektrostatické síly přítomné mezi nimi méně efektivní..
Lze očekávat, že výkon této soli ve vodném roztoku bude podobný výkonu NaOCl. Obklopen vodou, K+ -objemnější - musí mít větší hydratační sféru než Na+. Jinak se vlastnosti jeho roztoků (barva, vůně a bělící schopnost) významně neliší..
Nomenklatura
Proč je chlornan draselný tak pojmenovaný? Abychom na to mohli odpovědět, musíme se uchýlit k nomenklatuře ternárních solí, která se řídí IUPAC. Za prvé, protože draslík má pouze valenční hodnotu +1, není nutné jej zapisovat; proto je ignorován. Nepište tedy chlornan draselný (I).
Kyselina chlorová má vzorec HClO3. Jak počet kyslíků klesá, atom chloru získává více elektronů; to znamená, že má méně pozitivní oxidační čísla. Například v této kyselině má Cl oxidační číslo +5.
Stejně jako v HClO má Cl oxidační číslo +1, které má navíc o dvě jednotky méně atomů O (1 místo 3 ve srovnání s HClO3), jeho přípona názvu se změní na -oso. Podobně, protože +1 je nejmenší oxidační číslo, kterého může atom Cl dosáhnout, je přidána předpona -hypo..
HClO se tedy nazývá kyselina chlorná. KOCl je však jeho draselná sůl a pro čísla oxidace Cl menší než +5 se přípona -oso zamění za příponu -ito. Jinak se u oxidačních čísel rovných nebo větších než +5 změní přípona na -ate. Název tedy zůstává chlornan draselný.
Vlastnosti
Molární hmotnost
90,55 g / mol.
Vzhled
Je to mírně šedivá kapalina.
Hustota
1,16 g / cm3
Bod tání
-2 ° C (28 ° F; 271 ° K). Tato nízká teplota tání, navzdory iontovému charakteru jejích vazeb, ukazuje slabou krystalickou mřížkovou energii její čisté pevné látky, produktu monovalentních nábojů K+ a OCl-, a na rozdíl od jeho iontových poloměrů.
Bod varu
102 ° C (216 ° F; 375 ° K). Je jen o málo vyšší než čistá voda.
Rozpustnost ve vodě
25% hmotn./obj., Což je přiměřená hodnota vzhledem ke snadnosti molekul vody solvatovat ionty K.+.
Vodné roztoky chlornanu draselného mají bělící vlastnosti, stejně jako NaOCl. Je dráždivý a při kontaktu s pokožkou, očima a sliznicemi může způsobit vážné poškození. Stejně tak jeho vdechování vyvolává podráždění průdušek, dýchací potíže a plicní edém..
Reaktivita
-Chlornan draselný je silné oxidační činidlo, které se nepovažuje za prvek, který způsobuje požáry nebo výbuchy. Je však schopen kombinovat s různými chemickými prvky za vzniku hořlavých a výbušných sloučenin..
-Při kontaktu s močovinou může tvořit NCl3, vysoce výbušná směs. Při zahřátí nebo při kontaktu s kyselinami vytváří vysoce toxický chloridový kouř. Při potenciálně výbušné reakci prudce reaguje s aktivním uhlím.
-Spojuje se s acetylenem za vzniku výbušného chloracetylenu. Stejně tak může jeho reakce s organickými látkami, olejem, uhlovodíky a alkoholy způsobit exploze. Jeho reakce s nitromethanem, methanolem a ethanolem může být výbušná.
-Rozkládá uvolňující kyslík, což je proces, který může být katalyzován rzí nebo kovovou nádobou, která ho obsahuje..
-Chlornan draselný musí být skladován za studena, aby se zabránilo tvorbě chlorečnanu draselného, jehož rozklad může být dokonce výbušný..
Aplikace
-Používá se jako dezinfekční prostředek na povrch a pitnou vodu.
-Odbourávání chlornanu draselného v půdě na chlorid draselný naznačuje jeho použití v plodinách jako zdroj draslíku, což je primární nutriční prvek pro rostliny..
-Některé společnosti navrhly jeho použití jako náhradu za NaOCl jako bělicí prostředek, přičemž tvrdí, že má příznivé vlastnosti iontu K.+ proti dopadům na životní prostředí způsobeným Na+.
Reference
- Enviro Tech. Bez sodíku. [PDF]. Citováno 29. května 2018 z: envirotech.com
- PubChem. (2018). Chlornan draselný. Citováno dne 29. května 2018 z: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2018). Chlornan draselný. Citováno dne 29. května 2018 z: en.wikipedia.org
- Chemická kniha. (2017). Chlornan draselný. Citováno dne 29. května 2018 z: chemicalbook.com
- Whitten, Davis, Peck a Stanley. Chemie. (8. vydání). CENGAGE Learning, s. 873, 874.



Zatím žádné komentáře