
Atomový objem Jak se liší v periodické tabulce a příkladech
The atomový objem je relativní hodnota, která označuje vztah mezi molární hmotností prvku a jeho hustotou. Tento objem tedy závisí na hustotě prvku a hustota zase na fázi a na tom, jak jsou v něm uspořádány atomy..
Atomový objem prvku Z tedy není stejný v jiné fázi, než ve které vykazuje při pokojové teplotě (kapalná, pevná nebo plynná), nebo pokud je součástí určitých sloučenin. Atomový objem Z ve sloučenině ZA se tedy liší od atomového objemu Z ve sloučenině ZB.

Proč? Abychom tomu porozuměli, je nutné porovnat atomy například s kuličkami. Kuličky, stejně jako namodralé na obrázku výše, mají velmi dobře definovaný materiální okraj, který lze vidět díky jejich lesklému povrchu. Naproti tomu hranice atomů je difuzní, i když je lze považovat za vzdáleně sférické.
To, co určuje bod za atomovou hranicí, je tedy nulová pravděpodobnost nalezení elektronu, a tento bod může být dále nebo blíže k jádru v závislosti na tom, kolik sousedních atomů interaguje kolem uvažovaného atomu..
Rejstřík článků
- 1 Atomový objem a poloměr
- 2 Další vzorec
- 3 Jak se mění atomový objem v periodické tabulce?
- 3.1 Atomové objemy přechodných kovů
- 4 příklady
- 4.1 Příklad 1
- 4.2 Příklad 2
- 5 Reference
Atomový objem a poloměr
Interakcí dvou atomů H v molekule H.dva, jsou definovány polohy jejich jader a také vzdálenosti mezi nimi (mezijaderné vzdálenosti). Pokud jsou oba atomy sférické, poloměr je vzdálenost mezi jádrem a fuzzy hranicí:
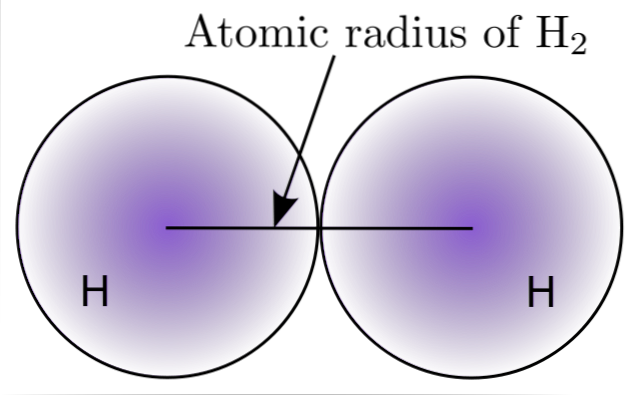
Na obrázku výše vidíte, jak klesá pravděpodobnost nalezení elektronu, když se pohybuje od jádra. Pak vydělením mezijaderné vzdálenosti dvěma získáme atomový poloměr. Dále, za předpokladu sférické geometrie atomů, se vzorec použije k výpočtu objemu koule:
V = (4/3) (Pi) r3
V tomto výrazu r je atomový poloměr určený pro molekulu H.dva. Hodnota V vypočítaná touto nepřesnou metodou se může změnit, pokud se vezme v úvahu například Hdva v kapalném nebo kovovém stavu. Tato metoda je však velmi nepřesná, protože tvary atomů jsou ve svých interakcích velmi daleko od ideální sféry..
Pro stanovení atomových objemů v pevných látkách je bráno v úvahu mnoho proměnných týkajících se uspořádání, které jsou získány rentgenovými difrakčními studiemi..
Další vzorec
Molární hmotnost vyjadřuje množství hmoty, která má mol atomů chemického prvku.
Jeho jednotky jsou g / mol. Na druhou stranu, hustota je objem, který jeden gram prvku zabírá: g / ml. Vzhledem k tomu, že jednotky atomového objemu jsou ml / mol, musíte hrát s proměnnými, abyste se dostali k požadovaným jednotkám:
(g / mol) (ml / g) = ml / mol
Nebo co je stejné:
(Molární hmotnost) (1 / D) = V
(Molární hmotnost / D) = V
Lze tedy snadno vypočítat objem jednoho molu atomů prvku; zatímco pomocí vzorce sférického objemu je vypočítán objem jednotlivého atomu. K dosažení této hodnoty od první je nutná konverze prostřednictvím čísla Avogadra (6,02 · 10-2. 3).
Jak se liší atomový objem v periodické tabulce?
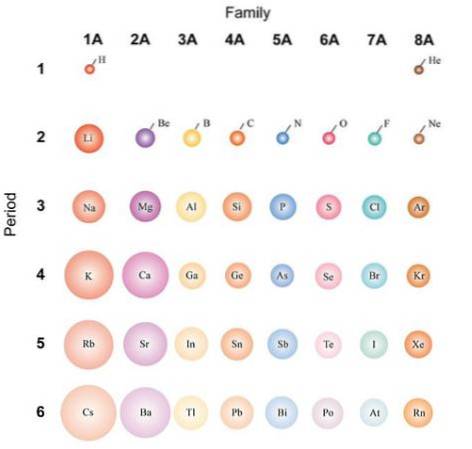
Pokud jsou atomy považovány za sférické, bude jejich variace stejná jako variace pozorovaná v atomových poloměrech. Na obrázku výše, který zobrazuje reprezentativní prvky, je znázorněno, že atomy se zprava doleva zmenšují; místo toho se shora dolů stávají objemnějšími.
Je to proto, že ve stejném období jádro začleňuje protony, když se pohybuje doprava. Tyto protony vyvíjejí přitažlivou sílu na vnější elektrony, které pociťují efektivní jaderný náboj Zef, menší než skutečný jaderný náboj Z.
Elektrony vnitřních skořápek odpuzují elektrony vnějšího pláště a snižují tak účinek jádra na ně; toto se nazývá efekt obrazovky. Ve stejném období nemůže efekt clony působit proti nárůstu počtu protonů, takže elektrony ve vnitřním obalu nebrání atomům ve smršťování..
Sestup do skupiny však umožňuje nové energetické úrovně, které umožňují elektronům obíhat dále z jádra. Podobně se zvyšuje počet elektronů ve vnitřním obalu, jehož stínící účinky se začnou snižovat, pokud jádro znovu přidá protony..
Z těchto důvodů se oceňuje, že skupina 1A má nejvíce objemných atomů, na rozdíl od malých atomů skupiny 8A (nebo 18), vzácných plynů..
Atomové objemy přechodných kovů
Atomy přechodných kovů začleňují elektrony do vnitřních d orbitalů. Toto zvýšení efektu obrazovky a stejně jako skutečného jaderného náboje Z se zruší téměř stejně, takže jejich atomy si ve stejném období udrží podobnou velikost..
Jinými slovy: v jednom období mají přechodné kovy podobné atomové objemy. Tyto malé rozdíly jsou však nesmírně významné při definování kovových krystalů (jako by to byly kovové kuličky).
Příklady
K výpočtu atomového objemu prvku jsou k dispozici dva matematické vzorce, každý s odpovídajícími příklady.
Příklad 1
Vzhledem k atomovému poloměru vodíku -37 pm (1 pikometr = 10-12m) - a cesium -265 pm-, vypočítat jejich atomové objemy.
Pomocí vzorce sférického objemu pak máme:
PROTIH= (4/3) (3.14) (37 hodin)3= 212,07 odp3
PROTIČs= (4/3) (3.14) (265 pm)3= 77912297,67 odp3
Tyto objemy vyjádřené v pikometrech jsou však přemrštěné, takže se transformují na jednotky angstromů a vynásobí je konverzním faktorem (1Å / 100pm)3:
(212.07 hodin3) (1Å / 100pm)3= 2,1207 × 10-4 NA3
(77912297,67 hod3) (1Å / 100pm)3= 77,912 Å3
Rozdíly ve velikosti mezi malým atomem H a objemným atomem Cs jsou tedy numericky doloženy. Je třeba mít na paměti, že tyto výpočty jsou pouze aproximacemi pod tvrzením, že atom je zcela sférický, který putuje před realitou.
Příklad 2

Hustota čistého zlata je 19,32 g / ml a jeho molární hmotnost je 196,97 g / mol. Použitím vzorce M / D pro výpočet objemu jednoho molu atomů zlata se získá toto:
PROTIAu= (196,97 g / mol) / (19,32 g / ml) = 10,19 ml / mol
To znamená, že 1 mol atomů zlata zabírá 10,19 ml, ale jaký objem konkrétně zabírá atom zlata? A jak to vyjádřit v jednotkách pm3? K tomu jednoduše použijte následující převodní faktory:
(10,19 ml / mol) · (mol / 6,02 · 10-2. 3 atomy) · (1 m / 100 cm)3(13:00 / 10-12m)3= 16,92 · 106 odpoledne3
Na druhé straně je atomový poloměr zlata 166 hodin. Pokud jsou porovnány oba objemy - objem získaný předchozí metodou a objem vypočtený pomocí vzorce sférického objemu - bude zjištěno, že nemají stejnou hodnotu:
PROTIAu= (4/3) (3,14) (166 hodin)3= 19,15 · 106 odpoledne3
Který z těchto dvou je nejblíže přijatelné hodnotě? Ten, který je nejblíže experimentálním výsledkům získaným rentgenovou difrakcí krystalové struktury zlata.
Reference
- Helmenstine, Anne Marie, Ph.D. (9. prosince 2017). Atomový objem Definice. Citováno dne 6. června 2018 z: thoughtco.com
- Mayfair, Andrew. (13. března 2018). Jak vypočítat objem atomu. Vědění. Citováno dne 6. června 2018 z: sciencing.com
- Wiki Kids Ltd. (2018). Křivky atomového objemu Lothar Meyer. Citováno dne 6. června 2018 z: wonderwhizkids.com
- Lumen. Periodické trendy: atomový poloměr. Citováno dne 6. června 2018 z: courses.lumenlearning.com
- Camilo J. Derpich. Atomový objem a hustota. Citováno dne 6. června 2018 z: es-puraquimica.weebly.com
- Whitten, Davis, Peck a Stanley. Chemie. (8. vydání). CENGAGE Learning, s. 222-224.
- Nadace CK-12. (22. února 2010). Srovnávací atomové velikosti. [Postava]. Citováno dne 6. června 2018 z: commons.wikimedia.org
- Nadace CK-12. Vydání (22. února 2010). Atomový poloměr Hdva. [Postava]. Citováno dne 6. června 2018 z: commons.wikimedia.org



Zatím žádné komentáře