
Specifický objem vody, vzduchu, páry, dusíku a ideálního plynu
The konkrétní objem jedná se o intenzivní vlastnost charakteristickou pro každý prvek nebo materiál. Matematicky je definován jako vztah mezi objemem obsazeným určitým množstvím hmoty (kilogramem nebo gramem); jinými slovy, je to převrácená hodnota hustoty.
Hustota udává, kolik váží 1 ml hmoty (kapalné, pevné, plynné nebo homogenní nebo heterogenní směsi), zatímco specifický objem odpovídá objemu, který zabírá 1 g (nebo 1 kg). Když tedy známe hustotu látky, stačí vypočítat reciproční hodnotu a určit její specifický objem.

Na co odkazuje slovo „konkrétní“? Když se říká, že některá vlastnost je konkrétní, znamená to, že je vyjádřena jako funkce hmotnosti, která umožňuje její transformaci z rozsáhlé vlastnosti (která závisí na hmotnosti) na intenzivní (spojitou ve všech bodech systému)..
Jednotky, ve kterých je specifický objem obvykle vyjádřen, jsou (m3/ Kg) nebo (cm3/ g). Ačkoli tato vlastnost nezávisí na hmotnosti, záleží na jiných proměnných, jako je teplota nebo tlak dopadající na látku. To způsobí, že gram látky zabírá při vyšších teplotách větší objem..
Rejstřík článků
- 1 Z vody
- 2 Ze vzduchu
- 3 Z páry
- 4 Dusík
- 5 Ideálního plynu
- 6 Reference
Vody
Na prvním obrázku vidíte kapku vody, která se brzy smísí s povrchem kapaliny. Protože je to přirozeně látka, její hmotnost zabírá objem jako každá jiná. Tento makroskopický objem je produktem objemu a interakcí jeho molekul.
Molekula vody má chemický vzorec HdvaNebo s molekulovou hmotností přibližně 18 g / mol. Hustoty, které prezentuje, závisí také na teplotě a v makroscale je distribuce jeho molekul považována za co nejhomogennější..
Při hodnotách hustoty ρ při teplotě T stačí k výpočtu měrného objemu kapalné vody použít následující vzorec:
v = (1 / ρ)
Vypočítává se experimentálním stanovením hustoty vody pomocí pyknometru a následným provedením matematického výpočtu. Protože se molekuly každé látky navzájem liší, bude se lišit i výsledný měrný objem.
Pokud je hustota vody v širokém teplotním rozmezí 0,997 kg / m3, jeho specifický objem je 1 003 m3/ kg.
Ze vzduchu

Vzduch je homogenní plynná směs složená převážně z dusíku (78%), následovaného kyslíkem (21%) a nakonec dalšími plyny v zemské atmosféře. Jeho hustota je makroskopickým vyjádřením celé té směsi molekul, které neinteragují efektivně a šíří se všemi směry..
Protože se o látce předpokládá, že je spojitá, její šíření v nádobě nemění její složení. Opět měřením hustoty za popsaných podmínek teploty a tlaku je možné určit, jaký objem zabírá 1 g vzduchu.
Protože měrný objem je 1 / ρ a jeho ρ je menší než objem vody, je jeho měrný objem větší.
Vysvětlení této skutečnosti je založeno na molekulárních interakcích voda versus vzduch; druhý ani v případě vlhkosti nekondenzuje, pokud není vystaven velmi nízkým teplotám a vysokým tlakům.
Z páry
Bude za stejných podmínek zabírat gram páry větší objem než gram vzduchu? Vzduch je v plynné fázi hustší než voda, protože na rozdíl od molekul vody jde o výše zmíněnou směs plynů..
Jelikož specifický objem je inverzní k hustotě, gram páry zaujímá větší objem (je méně hustý) než gram vzduchu.
Fyzikální vlastnosti páry jako kapaliny jsou zásadní v mnoha průmyslových procesech: uvnitř tepelných výměníků, ke zvýšení vlhkosti, mimo jiné k čištění strojů..
Existuje mnoho proměnných, které je třeba vzít v úvahu při manipulaci s velkým množstvím páry v průmyslových odvětvích, zejména pokud jde o mechaniku tekutin..
Dusík
Stejně jako ostatní plyny závisí jeho hustota značně na tlaku (na rozdíl od pevných látek a kapalin) a na teplotě. Hodnoty jeho konkrétního objemu se tedy liší podle těchto proměnných. Proto je potřeba určit jeho specifický objem k vyjádření systému z hlediska intenzivních vlastností.
Bez experimentálních hodnot je pomocí molekulárního uvažování obtížné porovnat hustotu dusíku s hustotou jiných plynů. Molekula dusíku je lineární (N≡N) a molekula vody je úhlová.
Protože „řádek“ zabírá menší objem než „řádek“Bumerang”, Pak lze očekávat, že podle definice hustoty (m / V) je dusík hustší než voda. Použitím hustoty 1 2506 Kg / m3, měrný objem za podmínek, ve kterých byla tato hodnota měřena, je 0,7996 m3/ Kg; je to prostě reciproční (1 / ρ).
Ideálního plynu
Ideální plyn je ten, který se řídí rovnicí:
P = nRT / V
Je vidět, že rovnice nezohledňuje žádnou proměnnou, jako je molekulární struktura nebo objem; nezohledňuje ani to, jak molekuly plynu interagují navzájem v prostoru definovaném systémem.
V omezeném rozsahu teplot a tlaků se všechny plyny „chovají“ stejně; z tohoto důvodu je do jisté míry platné předpokládat, že se řídí rovnicí ideálního plynu. Z této rovnice lze tedy určit různé vlastnosti plynů, včetně měrného objemu.
K jeho vyřešení je nutné vyjádřit rovnici z hlediska proměnných hustoty: hmotnosti a objemu. Mole jsou reprezentovány n, a to je výsledek dělení hmotnosti plynu jeho molekulovou hmotností (m / M).
Vezmeme-li proměnnou hmotnost m v rovnici, je-li rozdělena objemem, lze získat hustotu; odtud stačí vyčistit hustotu a poté „převrátit“ obě strany rovnice. Tímto způsobem se konečně určí konkrétní objem.
Obrázek níže ilustruje každý z kroků k dosažení konečného vyjádření specifického objemu ideálního plynu.
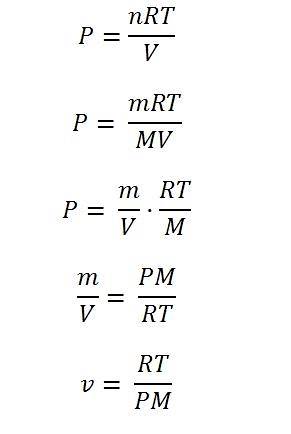
Reference
- Wikipedia. (2018). Specifický objem. Převzato z: en.wikipedia.org
- Study.com. (21. srpna 2017). Co je to specifický objem? - Definice, vzorec a jednotky převzaté z: study.com
- HRNEC. (5. května 2015). Specifický objem. Převzato z: grc.nasa.gov
- Michael J. Moran a Howard N. Shapiro. (2004). Základy technické termodynamiky. (2. vydání). Redakční reverté, strana 13.
- Jednotka 1: Pojmy termodynamiky. [PDF]. Převzato z: 4.tecnun.es
- TLV. (2018). Hlavní aplikace pro Steam. Převzato z: tlv.com



Zatím žádné komentáře