
Klasifikace materiálových systémů, fáze a příklady
The materiálové systémy Jsou to všechny ty, které se skládají z hmoty a které jsou izolovány od zbytku vesmíru, který má být studován. Hmota je všude a dává vnímání každodenního života formu a skutečný význam, ale když chcete studovat část hmoty, její okolí je opovrhováno a mluvíme o hmotném systému..
Jsou velmi variabilní, protože existují čisté a kompozitní materiály, stejně jako různé stavy a fáze agregací. Jak definovat hranici mezi hmotným systémem a jeho okolím? Vše závisí na uvažovaných proměnných. Například na obrázku pod každým mramorem může být studovaný systém..

Pokud se však má brát v úvahu barevná proměnná, je nutné vzít v úvahu všechny kuličky v automatu. Protože stroj není zajímavý, jedná se o prostředí kuliček. Materiálním systémem příkladu tedy je hmota kuliček a jejich vlastnosti (ať už žvýkačky, máty atd.).
Chemicky jsou však materiálové systémy definovány jako jakákoli čistá látka nebo jejich směs klasifikovaná podle jejich fyzikálních aspektů..
Rejstřík článků
- 1 Klasifikace
- 1.1 Systém homogenního materiálu
- 1.2 Systém heterogenního materiálu
- 2 fáze
- 2.1 Fázový diagram
- 3 příklady
- 4 Odkazy
Klasifikace
Systém homogenního materiálu
Studovaná látka může vykazovat jednotný vzhled, ve kterém její vlastnosti zůstávají konstantní bez ohledu na analyzovaný vzorek. Jinými slovy: tento druh systému se vyznačuje tím, že na první pohled má pouze jednu fázi hmoty.
Čistá látka a sloučeniny
Pokud je analyzována čistá látka, pak se zjistí, že fyzikálně-chemické vlastnosti se shodují ve stejných hodnotách a výsledcích, i když je odebráno mnoho vzorků (a v různých zeměpisných oblastech)..
Pokud by se například porovnal vzorek vápníku s vzorkem z Asie, Evropy, Afriky a Ameriky, měly by všechny stejné vlastnosti. Totéž by se stalo, kdyby byl odebrán vzorek čistého uhlíku.
Na druhou stranu čistá sloučenina také projevuje výše uvedené. Pokud by bylo zaručeno, že břidlice je vyrobena z jednoho a jediného materiálu, pak by byla klasifikována jako systém homogenního materiálu.
K tomu však u minerálního vzorku nedochází, protože obecně obsahuje nečistoty z jiných asociovaných minerálů a v tomto případě se jedná o heterogenní materiálový systém. Podobně tyto hmotné systémy, jako jsou stromy, kameny, hory nebo řeky, spadají do druhé klasifikace..
Rozpuštění
Obchodní ocet je 5% vodný roztok kyseliny octové; tj. 5 ml čisté kyseliny octové se rozpustí ve 100 ml vody. Jeho vzhled je však průhledná kapalina, i když ve skutečnosti jde o kombinaci dvou čistých sloučenin (voda a kyselina octová).
Systém heterogenního materiálu
Na rozdíl od homogenního není v této třídě systému ani vzhled, ani vlastnosti konstantní a jsou nepravidelné po celou dobu jeho rozšíření..
Kromě toho jej lze podrobit fyzikálním nebo chemickým separačním technikám, ze kterých se extrahují fáze, které se považují za homogenní systém..
Fáze
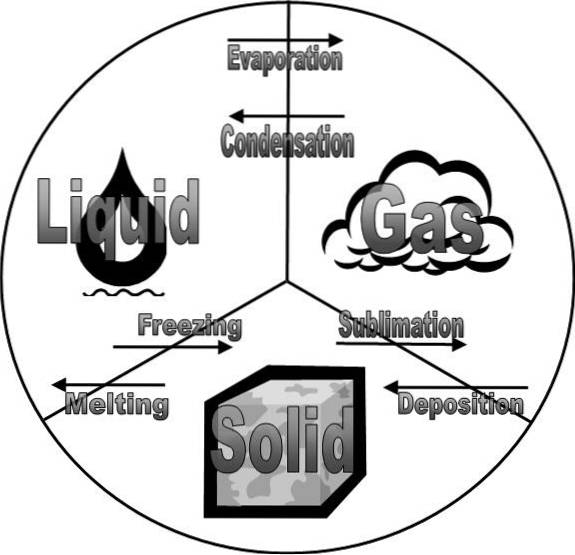
Horní obrázek ukazuje stavy hmoty a jejich změny. Ty úzce souvisí s fázemi hmoty, protože i když jsou stejné, představují jemné rozdíly..
V tomto případě jsou fáze hmotného systému pevné, kapalné a plynné. Jinými slovy, u určité hmoty podrobené analýze může přijmout kteroukoli z předchozích fází.
Vzhledem k tomu, že interakce v pevných látkách jsou velmi silné a závisí na proměnných, jako je tlak a teplota, systém může nebo nemusí mít různé pevné fáze.
Například sloučenina X, pevná při teplotě místnosti, má fázi I; ale když je tlak na něj velmi vysoký, jeho molekuly se přeskupí kompaktnějším způsobem a pak dojde k přechodu z fáze I do pevné fáze II..
Existují dokonce i další fáze, například III a IV, které pocházejí z II při různých teplotách. Systém homogenního materiálu X zdánlivé pevné fáze tedy může získat až čtyři pevné fáze: I, II, III a IV.
V případě kapalných a plynných systémů mohou molekuly obecně přijmout pouze jednu fázi v těchto stavech hmoty. Jinými slovy, nemusí existovat plynná fáze I a plynná fáze II..
Fázový diagram
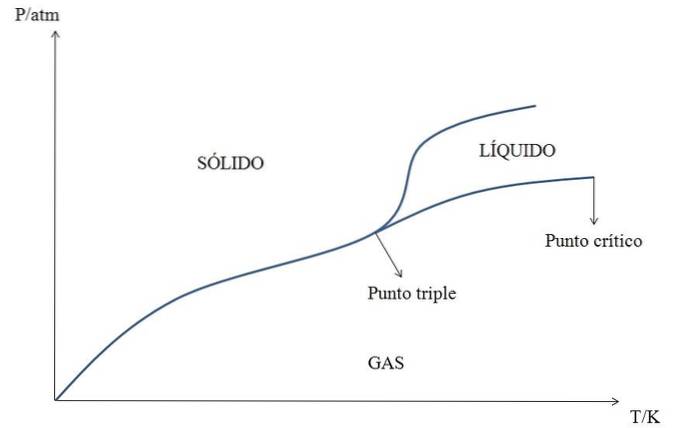
Existuje mnoho fázových diagramů: některé pro jednu sloučeninu nebo látku (jako na obrázku výše) a jiné pro binární systémy (například sůl ve vodě) nebo ternární (tři složky).
Nejjednodušší ze všech je fázový diagram látky. U hypotetické látky Y je tedy její fáze představována jako funkce tlaku (osa y) a teploty (osa x).
Při nízkých tlacích je to plyn bez ohledu na jeho teplotu. Při zvyšování tlaku se však plyn Y ukládá v pevné látce Y.
Avšak při teplotách nad kritickým bodem Y plyn kondenzuje na kapalinu Y, a pokud se také zvýší tlak (jeden stoupá vertikálně diagramem), kapalina tuhne.
Každá čára představuje rovnováhu mezi dvěma fázemi, které odděluje: pevný plyn, kapalný plyn, pevný-kapalný, kapalný-pevný a pevný-kapalný-plyn v trojném bodě.
Navíc od kritického bodu Y není ukázán žádný fyzický rozdíl mezi plynnou fází a kapalnou fází: tvoří to, co je známé jako superkritická tekutina..
Příklady

- Balón je hmotný systém, protože jeho obsah je plynný, a proto má chemickou povahu; pokud je plyn méně hustý než vzduch, balón vystoupá k obloze.
- Binární systém voda-olej má dvě fáze: jednu z vody a druhou, logicky, z oleje. Sada obou je heterogenní systém, zatímco jednotlivé vrstvy jsou homogenní systémy. Pokud byste chtěli olej extrahovat, budete muset provést extrakci kapalina-kapalina organickým a těkavým rozpouštědlem..
- Systém pevných látek může sestávat ze směsi bílého a hnědého cukru. Zde rozdíl barev mezi krystaly činí tento případ heterogenním systémem.
- Mořská voda je dalším příkladem systému homogenního materiálu. Skládá se z roztoku mnoha iontů, které jsou zodpovědné za jeho charakteristickou slanou chuť. Pokud by se vzorek mořské vody odpařil v nádobě, usazoval by v ní bílé soli..
Reference
- Systém a jeho okolí. Citováno dne 27. května 2018 z: chem.libretexts.org
- Antonio de Ulloa. Materiálové systémy. [PDF]. Citováno dne 27. května 2018 z: 2.educarchile.cl
- Daniel J. Berger. (2001). Citováno dne 27. května 2018 z: bluffton.edu
- Systém a okolí v chemii. Citováno dne 27. května 2018 z: chemteam.info
- Helmenstine, Anne Marie, Ph.D. (6. února 2018). Definice otevřeného systému v chemii. Citováno dne 27. května 2018 z webu: thoughtco.com
- Glen Research Center. Fáze hmoty. Citováno dne 27. května 2018 od: grc.nasa.gov
- Alison H. (2006-09-15). Spuštění balónu. Citováno 28. května 2018 z: flickr.com

Zatím žádné komentáře