
Struktura, vlastnosti, použití, octan hlinitý (Al (CH3COO) 3)

The octan hlinitý je organická sloučenina tvořená hliníkovým iontem Al3+ a tři octanové ionty CH3VRKAT-. Jeho chemický vzorec je Al (CH3VRKAT)3. Je také známý jako triacetát hlinitý. Je to mírně hygroskopická bílá pevná látka a je rozpustná ve vodě..
K získání této sloučeniny je nutné použít zcela bezvodé podmínky, tj. Bez vody, jinak by se vytvořil diacetát hlinitý Al (OH) (CH3VRKAT)dva.
Roztoky octanu hlinitého mají antibakteriální a protiplísňové vlastnosti, a proto se od 19. století používají k léčbě infekcí, zejména uší..
Nejznámější je Burowovo řešení navržené německým lékařem. Jeho použití však občas vedlo k poškození středního ucha..
Toto řešení se také používá k léčbě kožních problémů, jako jsou svědění a vyrážky. Používá se dokonce jako lék proti spálení.
Acetát hlinitý a jeho deriváty se používají k získání velmi malých struktur nebo částic oxidu hlinitého AldvaNEBO3. Tyto struktury nebo nanočástice mohou být ve formě listů, květů nebo nanotrubiček..
Rejstřík článků
- 1 Struktura
- 2 Názvosloví
- 3 Vlastnosti
- 3.1 Fyzický stav
- 3,2 Molekulová hmotnost
- 3.3 Rozpustnost
- 3.4 Chemické vlastnosti
- 3.5 Další vlastnosti
- 4 Získání
- 5 Použití v medicíně
- 5.1 Ušní infekce
- 5.2 Kožní onemocnění
- 6 Jiná použití
- 6.1 Ukončení používání
- 7 Škodlivé účinky
- 8 Reference
Struktura
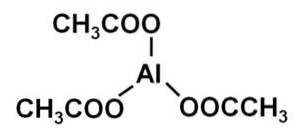
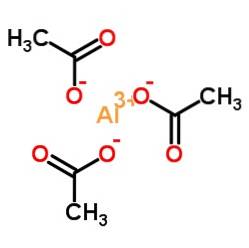
Triacetát hlinitý je vyroben z hliníkového kationtu Al3+ a tři acetátové anionty CH3VRKAT-. Je to hliníková sůl kyseliny octové CH3COOH.
Hliník je vázán na acetátové anionty prostřednictvím svého kyslíku. Jinými slovy, je připojen ke třem kyslíkům. Tyto spoje jsou iontové.
Nomenklatura
- Octan hlinitý
- Triacetát hlinitý
- Ethanoát hlinitý
- Burowovo řešení (překlad z angličtiny Burowovo řešení): Je to roztok octanu hlinitého.
Vlastnosti
Fyzický stav
Plně bílá.
Molekulární váha
204,11 g / mol
Rozpustnost
Rozpustný ve vodě.
Chemické vlastnosti
Ve vodném roztoku se triacetát hlinitý rozpustí a má sklon k tvorbě diacetátu Al (OH) (CH3COO) a někdy Al (OH) monoacetátdva(CH3VRKAT). Vše závisí na pH a množství kyseliny octové CH3COOH přítomný v roztoku.
Al (CH3VRKAT)3 + HdvaO OH Al (OH) (CH3VRKAT)dva + CH3COOH
Al (CH3VRKAT)3 + 2 hdvaO ⇔ Al (OH)dva(CH3COO) + 2 CH3COOH
Další vlastnosti
Acetát hlinitý je mírně hygroskopický, to znamená, že má tendenci absorbovat vodu ze vzduchu.
Získávání
Acetát hlinitý se výhodně získává za přísně bezvodých podmínek, tj. Za úplné nepřítomnosti vody. To zahrnuje také nepřítomnost vzduchu, protože může obsahovat vlhkost..
Zahřejte směs ledové kyseliny octové CH3COOH a anhydrid kyseliny octové (CH3CO)dvaNebo za takových podmínek, aby bylo možné vyloučit veškerou přítomnou vodu. K této horké směsi se přidá chlorid hlinitý AlCl.3 bezvodá pevná látka (bez vody).
Bílá pevná látka Al (CH3VRKAT)3.
AlCl3 + 3 CH3COOH → Al (CH3VRKAT)3 + 3 HCl
Úplná nepřítomnost vody je důležitá, aby se zabránilo tvorbě solí monoacetátu hlinitého Al (OH)dva(CH3COO) a diacetát hlinitý Al (OH) (CH3VRKAT)dva.
Lze jej také získat reakcí hydroxidu hlinitého Al (OH)3 a kyselina octová CH3COOH.
Použití v medicíně
Ušní infekce
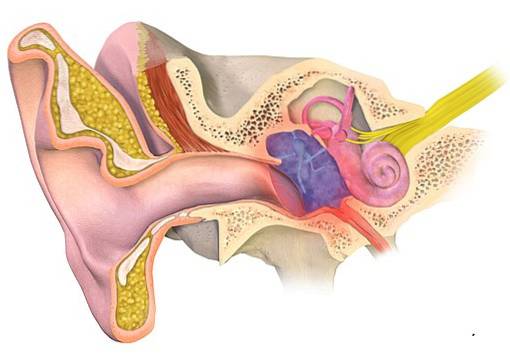
Acetát hlinitý se používá od 19. století k léčbě otitis, což je zánět vnějšího nebo středního ucha obvykle doprovázený infekcí. Jeho použití je způsobeno jeho antibakteriálním a antifungálním účinkem.
Používá se ve formě 13% roztoku octanu hlinitého, který původně vytvořil německý lékař Karl August von Burow, a proto se mu říká Burowovo řešení..
Bylo zjištěno, že inhibuje růst mikroorganismů běžně se vyskytujících v otitis media nebo externa, jako je otitis media. Pseudomonas aeruginosa, the Zlatý stafylokok a Proteus mirabilis.

Existují však lidé, kteří uvádějí, že tato řešení mohou být škodlivá pro ucho. Některé studie na zvířatech zkoumají jeho toxické účinky na ucho, ale uvádějí protichůdné výsledky..
Někteří vědci doporučují nepoužívat octan hlinitý, když je tympanická membrána perforována, protože bylo pozorováno, že má zánětlivý účinek na střední ucho.
Kožní choroby
Burowův roztok se používá jako antiseptikum, adstringens a jako lokální roztok k léčbě závažných vyrážek, dermatitidy, zánětů, svědění, pálení a spálení sluncem. Působí uklidňující a snižující podráždění.
Jiná použití
Triacetát hlinitý a jeho deriváty se používají pro mnoho kvalitativních a kvantitativních chemických experimentů.
Derivát triacetátu hlinitého, Al (OH) (CH3VRKAT)dva také se nazývá acetát hydroxidu hlinitého, používá se jako prekurzor k získání nanostruktur gama-oxidu hlinitého (γ-AldvaNEBO3).
V tomto případě prekurzor znamená, že y-Al nanostruktury jsou připraveny z diacetátu hlinitého (získaného konkrétním způsobem).dvaNEBO3, a toho je dosaženo zahřátím na velmi vysoké teploty.
Nanostruktury jsou velmi malé částice, které lze pozorovat pouze pomocí speciálních mikroskopů, jako jsou elektronové mikroskopy. S octanem hlinitým jako prekurzorem byly získány y-Al nanostrukturydvaNEBO3 podobné listím, květům, vláknům a dokonce i nanotrubicím.

Ukončení používání
Na začátku 20. století se octan hlinitý používal jako konzervační látka v potravinách, jako jsou konzervované klobásy.
Roztok octanu hlinitého byl připraven smícháním síranu hlinitého Aldva(SW4)3, uhličitan vápenatý CaCO3, kyselina octová CH3COOH a voda HdvaNebo a bylo přidáno do jídla.
Když tento roztok přijde do styku s masem, je hliník ve svých složkách fixován ve formě sloučeniny, která je nerozpustná ve vroucí vodě, ale která se rozpouští v žaludečních šťávách přibližně z 80%.
Již v roce 1904 bylo známo, že soli hliníku zpomalují trávení, a to jak v žaludku, tak ve střevech. Proto je nežádoucí praxí přidávat do konzervovaných potravin roztoky octanu hlinitého..

Škodlivé účinky
Vzhledem k tomu, že existují studie, které uvádějí, že octan hlinitý může být toxický, byly provedeny testy, při nichž byly laboratorním myším injekčně podán octan hlinitý..
Výsledky naznačují, že tato sloučenina způsobuje poškození páteře uvedených zvířat, stejně jako poškození chromozomů a spermií zvířat. Jinými slovy je genotoxický.
To vás upozorní na potenciální zdravotní rizika, která by mohla být způsobena nadměrným vystavením octanu hlinitému, a na péči, kterou je třeba při jeho používání věnovat..
Reference
- Mac-Kay Chace, E. (1904). Použití zásaditého octanu hlinitého jako konzervační látky v uzeninách. Journal of the American Chemical Society 1904, 26, 6: 662-665. Obnoveno z pubs.acs.org.
- Hood, G.C. a Ihde, A.J. (1950). Acetáty a propionáty hlinité - jejich příprava a složení. Journal of the American Chemical Society 1950, 72, 5: 2094-2095. Obnoveno z pubs.acs.org.
- Pitaro, J. a kol. (2013). Ototoxicita octového roztoku octanu hlinitého / benzenethoniumchloridu na zvířecím modelu činčily. Laryngoscope, 2013; 123 (10): 2521-5. Obnoveno z ncbi.nlm.nih.gov.
- Thorp, M.A. et al. (2000). Burowovo řešení při léčbě aktivního slizničního chronického hnisavého zánětu středního ucha: stanovení účinného ředění. The Journal of Laryngology & Otology, June 2000, Vol. 114, str. 432-436. Obnoveno z ncbi.nlm.nih.gov.
- D'Souza, pane P. et al. (2014). Stanovení genotoxicity octanu hlinitého v kostní dřeni, zárodečných buňkách samců a fetálních jaterních buňkách švýcarských albínských myší. Mutation Research 766 (2014) 16-22. Obnoveno z ncbi.nlm.nih.gov.
- Basal, Y. a kol. (2015). Účinky aktuálního Burowova a Castellaniho řešení na sliznici středního ucha potkanů. J. Int Adv Otol 2015; 11 (3): 253-6. Obnoveno z advancedotology.org.
- NÁS. Národní lékařská knihovna. (2019). Octan hlinitý. Obnoveno z pubchem.ncbi.nlm.nih.gov.
- Buttaravoli, P. a Leffler, S.M. (2012). Úžeh. Co dělat. V případě drobných mimořádných událostí (třetí vydání). Obnoveno ze sciencedirect.com.
- Thompson, E. a Kalus, A. (2017). Akutní kožní reakce a bakteriální infekce. Léčba. V příručce o cestování a tropické medicíně (páté vydání). Obnoveno ze sciencedirect.com.
- Kim, T. a kol. (2010). Řízená morfologie Syntéza nanostruktur gama-oxid hlinitý prostřednictvím iontové kapalinové hydrotermální cesty. Crystal Growth & Design, sv. 10, č. 7, 2010, str. 2928-2933. Obnoveno z pubs.acs.org.
- Rajala, J.W. et al. (2015). Dutá keramická vlákna Electrospun z dutého oxidu hlinitého s jádrem. Vlákna 2015, 3, 450-462. Obnoveno z mdpi.com.



Zatím žádné komentáře