
Struktura ethylacetátu, vlastnosti, syntéza, použití
The ethylacetát nebo ethylethanoát (Název IUPAC) je organická sloučenina, jejíž chemický vzorec je CH3COOCdvaH5. Skládá se z esteru, kde alkoholová složka pochází z ethanolu, zatímco její složka karboxylové kyseliny pochází z kyseliny octové..
Je to kapalina za normálních podmínek teploty a tlaku, která má příjemnou ovocnou vůni. Tato vlastnost je dokonale v souladu s tím, co se očekává od esteru; což je ve skutečnosti chemická podstata ethylacetátu. Z tohoto důvodu nachází použití v potravinářských výrobcích a alkoholických nápojích..

Horní obrázek ukazuje kosterní strukturu ethylacetátu. Vlevo si všimněte jeho složky karboxylové kyseliny a vpravo alkoholové složky. Ze strukturálního hlediska lze očekávat, že se tato sloučenina bude chovat jako hybrid mezi octem a alkoholem; vykazuje však své vlastní vlastnosti.
Právě zde vynikají takové hybridy zvané estery. Ethylacetát nemůže reagovat jako kyselina, ani nemůže být dehydratován kvůli nepřítomnosti skupiny OH. Místo toho prochází bazickou hydrolýzou v přítomnosti silné báze, jako je hydroxid sodný, NaOH.
Tato hydrolýzní reakce se používá ve výukových laboratořích pro chemické kinetické experimenty; kde reakce je také druhého řádu. Když dojde k hydrolýze, ethylethanoát se prakticky vrací ke svým původním složkám: kyselině (deprotonované NaOH) a alkoholu.
Ve své strukturní kostře je pozorováno, že atomy vodíku převládají nad atomy kyslíku. To ovlivňuje jejich schopnost interakce s druhy, které nejsou tak polární jako tuky. Podobně se používá k rozpuštění sloučenin, jako jsou pryskyřice, barviva a obecně organické pevné látky..
Navzdory příjemné vůni má dlouhodobé působení této kapaliny negativní dopad (jako téměř všechny chemické sloučeniny) na tělo..
Rejstřík článků
- 1 Struktura ethylacetátu
- 1.1 Absence atomů donoru vodíkové vazby
- 2 Fyzikální a chemické vlastnosti
- 2.1 Jména
- 2.2 Molekulární vzorec
- 2.3 Molekulová hmotnost
- 2.4 Fyzický popis
- 2.5 Barva
- 2.6 Zápach
- 2.7 Příchuť
- 2.8 Prahová hodnota zápachu
- 2.9 Bod varu
- 2.10 Bod tání
- 2.11 Rozpustnost ve vodě
- 2.12 Rozpustnost v organických rozpouštědlech
- 2.13 Hustota
- 2.14 Hustota par
- 2.15 Stabilita
- 2.16 Tlak par
- 2.17 Viskozita
- 2.18 Spalné teplo
- 2.19 Odpařovací teplo
- 2.20 Povrchové napětí
- 2.21 Index lomu
- 2.22 Skladovací teplota
- 2,23 pKa
- 3 Syntéza
- 3.1 Fisherova reakce
- 3.2 Tiščenkova reakce
- 3.3 Jiné metody
- 4 použití
- 4.1 Rozpouštědlo
- 4.2 Umělé příchutě
- 4.3 Analýza
- 4.4 Organické syntézy
- 4.5 Chromatografie
- 4.6 Entomologie
- 5 Rizika
- 6 Reference
Struktura ethylacetátu
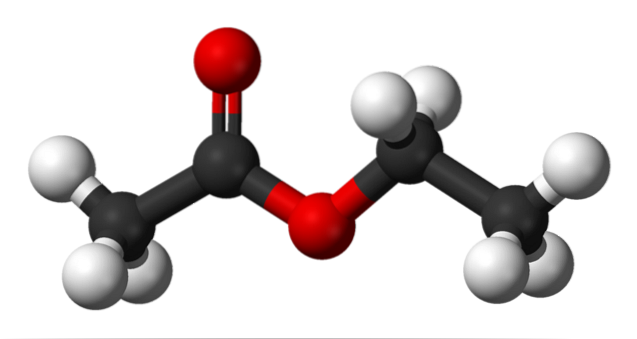
Horní obrázek ukazuje strukturu ethylacetátu s modelem koulí a pruhů. V tomto modelu jsou atomy kyslíku zvýrazněny červenými koulemi; nalevo je frakce odvozená od kyseliny a napravo frakce odvozená od alkoholu (alkoxyskupina, -OR).
Karbonylová skupina je viditelná vazbou C = O (dvojité sloupce). Struktura kolem této skupiny a sousedního kyslíku je plochá, kvůli skutečnosti, že dochází k delokalizaci náboje rezonancí mezi oběma kyslíky; skutečnost, která vysvětluje relativně nízkou kyselost α vodíků (těch ze skupiny -CH3, spojené s C = O).
Otáčením dvou svých vazeb molekula přímo upřednostňuje její interakci s jinými molekulami. Přítomnost dvou atomů kyslíku a asymetrie ve struktuře mu dodávají permanentní dipólový moment; což je zase zodpovědné za jejich interakce dipól-dipól.
Například hustota elektronů je vyšší poblíž dvou atomů kyslíku a ve skupině -CH značně klesá.3, a postupně ve skupině OCHdvaCH3.
Díky těmto interakcím tvoří molekuly ethylacetátu za normálních podmínek kapalinu, která má značně vysokou teplotu varu (77 ° C)..
Absence atomů donoru vodíkové vazby
Když se podíváte pozorně na strukturu, všimnete si nepřítomnosti atomu schopného darovat vodíkovou vazbu. Atomy kyslíku jsou však takovými akceptory a kvůli ethylacetátu je velmi rozpustný ve vodě a interaguje v odhadovatelné míře s polárními sloučeninami a donory vodíkových vazeb (jako jsou cukry)..
To mu také umožňuje vynikající interakci s ethanolem; důvod, proč jeho přítomnost nechybí v alkoholických nápojích.
Na druhé straně jeho alkoxyskupina umožňuje interakci s určitými nepolárními sloučeninami, jako je chloroform, CH3Cl.
Fyzikální a chemické vlastnosti
Jména
-Ethylacetát
-Ethyl ethanoát
-Etylacetátový ester
-Acetoxyethan
Molekulární vzorec
C4H8NEBOdva nebo CH3COOCdvaH5
Molekulární váha
88,106 g / mol.
Fyzický popis
Čirá bezbarvá kapalina.
Barva
Bezbarvá kapalina.
Zápach
Charakteristické pro étery, podobné vůni ananasu.
Chuť
Příjemné po zředění dodá pivu ovocnou chuť.
Prahová hodnota zápachu
3,9 ppm. 0,0196 mg / m3 (nízký zápach); 665 mg / m3 (silný zápach).
Zápach detekovatelný při 7 - 50 ppm (průměr = 8 ppm).
Bod varu
171 ° F až 760 mmHg (77,1 ° C).
Bod tání
--83,8 ° C.
Rozpustnost ve vodě
80 g / l.
Rozpustnost v organických rozpouštědlech
Mísitelný s ethanolem a ethyletherem. Velmi dobře rozpustný v acetonu a benzenu. Rovněž mísitelný s chloroformem, stálými a těkavými oleji a také s okysličenými a chlorovanými rozpouštědly.
Hustota
0,9003 g / cm3.
Hustota par
3,04 (ve vzduchu: 1 poměr).
Stabilita
Rozkládá se pomalu vlhkostí; nekompatibilní s různými plasty a silnými oxidačními činidly. Míchání s vodou může být výbušné.
Tlak páry
93,2 mmHg při 25 ° C
Viskozita
0,423 mPoise při 25 ° C.
Spalné teplo
2 238,1 kJ / mol.
Odpařovací teplo
35,60 kJ / mol při 25 ° C.
Povrchové napětí
24 dyn / cm při 20 ° C.
Index lomu
1373 při 20 ° C / D.
Skladovací teplota
2 - 8 ° C.
pKa
16 - 18 při 25 ° C.
Syntéza
Fisherova reakce
Ethylacetát se průmyslově syntetizuje Fisherovou reakcí, při které se ethanol esterifikuje kyselinou octovou. Reakce se provádí při teplotě místnosti.
CH3CHdvaOH + CH3COOH <=> CH3COOCHdvaCH3 + HdvaNEBO
Reakce je urychlena kyselou katalýzou. Rovnováha se posune doprava, tj. Směrem k produkci ethylacetátu, odstraněním vody; podle zákona hromadné akce.
Tiščenkova reakce
Ethylacetát se také průmyslově připravuje pomocí Tishchenkovy reakce konjugující dva ekvivalenty acetaldehydu s použitím alkoxidu jako katalyzátoru..
2 CH3CHO => CH3COOCHdvaCH3
Jiné metody
-Ethylacetát se syntetizuje jako vedlejší produkt při oxidaci butanu na kyselinu octovou při reakci prováděné při teplotě 175 ° C a tlaku 50 atm. Používá se jako katalyzátor iontů kobaltu a chrómu.
-Ethylacetát je vedlejším produktem ethanolýzy polyvinylacetátu na polyvinylalkohol.
-Ethylacetát se také v průmyslu vyrábí dehydrogenací ethanolu, který katalyzuje reakci použitím mědi při vysoké teplotě, avšak nižší než 250 ° C..
Aplikace
Solventní
Ethylacetát se používá jako rozpouštědlo a ředidlo, které se používá při čištění desek plošných spojů. Používá se jako rozpouštědlo při výrobě modifikovaného chmelového extraktu a při bezkofeinaci kávy a čajových lístků. Používá se do inkoustů používaných k označování ovoce a zeleniny.
Ethylacetát se používá v textilním průmyslu jako čisticí prostředek. Používá se při kalibraci teploměrů používaných při oddělování cukrů. V nátěrovém průmyslu se používá jako rozpouštědlo a ředidlo pro použité materiály..
Umělé příchutě
Používá se při výrobě ovocných příchutí; například: banán, hruška, broskev a ananas, stejně jako hroznové aroma atd..
Analytics
Používá se při stanovení bismutu, boru, zlata, molybdenu a platiny, jakož i rozpouštědla pro thalium. Ethylacetát má schopnost extrahovat mnoho sloučenin a prvků přítomných ve vodném roztoku, například: fosfor, kobalt, wolfram a arsen.
Organické syntézy
Ethylacetát se v průmyslu používá jako reduktor viskozity pro pryskyřice používané ve formulacích fotorezistu. Používá se při výrobě acetamidu, acetylacetátu a methylheptanonu.
Chromatografie
Ethylacetát se používá v laboratořích jako mobilní fáze sloupcové chromatografie a jako extrakční rozpouštědlo. Jelikož ethylacetát má relativně nízkou teplotu varu, lze jej snadno odpařit, což umožňuje koncentraci látek rozpuštěných v rozpouštědle.
Entomologie
Ethylacetát se v entomologii používá k udušení hmyzu umístěného v kontejneru, což umožňuje jeho sběr a studium. Páry ethylacetátu zabijí hmyz, aniž by jej zničily a zabránily jeho ztvrdnutí, což usnadňuje jeho shromažďování pro sběr..
Rizika
-LDpadesátka ethylacetátu u potkanů naznačuje nízkou toxicitu. Může však dráždit pokožku, oči, kůži, nos a hrdlo..
-Vystavení vysokým úrovním může způsobit závratě a mdloby. Stejně tak může dlouhodobá expozice ovlivnit játra a ledviny..
-Vdechnutí ethylacetátu v koncentraci 20 000 - 43 000 ppm může způsobit plicní edém a krvácení..
-Limit expozice na pracovišti stanovila OSHA na 400 ppm ve vzduchu, průměrně za 8hodinovou směnu..
Reference
- Steven A. Hardinger. (2017). Ilustrovaný glosář organické chemie: ethylacetát (EtOAc). Obnoveno z: chem.ucla.edu
- Graham Solomons T.W., Craig B.Fryhle. (2011). Organická chemie. Miny. (10th edice.). Wiley plus.
- Morrison, R. T. a Boyd, R. N. (1990). Organická chemie. (5ta edice). Redakční Addison-Wesley Iberoamericana.
- Wikipedia. (2019). Ethylacetát. Obnoveno z: en.wikipedia.org
- Cotton S. (s.f.). Ethylacetát. Obnoveno z: chm.bris.ac.uk
- PubChem. (2019). Ethylacetát. Obnoveno z: pubchem.ncbi.nlm.nih.gov
- Newseed Chemical. (2018). Aplikace a použití ethylacetátu. Obnoveno z: foodsweeteners.com
- Ministerstvo zdravotnictví seniorských služeb v New Jersey. (2002). Ethylacetát. [PDF]. Obnoveno z: nj.gov



Zatím žádné komentáře