
Základ, příprava a použití agaru Müeller Hinton
The Müeller Hintonův agar Jedná se o pevné neselektivní živné médium, které se skládá z masového nálevu, kyselého kaseinového peptonu, škrobu, agaru a destilované vody. Toto médium umožňuje vynikající mikrobiální růst většiny rychle rostoucích bakterií.
To bylo původně vytvořeno John Howard Müeller a Jane Hinton izolovat nutričně náročné bakterie, jako je Neisseria gonorrhoeae Y Neisseria meningitidis. Díky svým charakteristikám se však ukázalo, že je ideální pro studium citlivosti na antibiotika a poskytuje spolehlivé a reprodukovatelné výsledky..
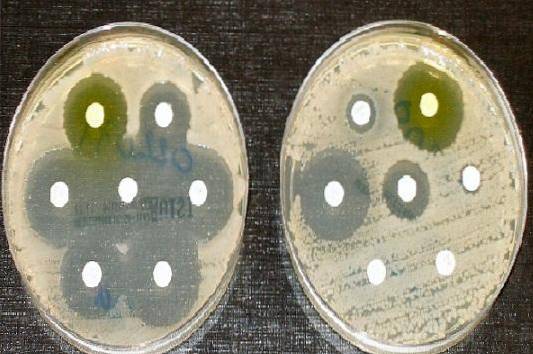
Proto je agar Müeller Hinton kultivační médium akceptované Institutem pro klinické a laboratorní standardy (CLSI) a Evropským výborem pro testování antimikrobiální citlivosti pro provádění testu antimikrobiální citlivosti metodou Kirbyho diskové difúze a Bauera.
Rejstřík článků
- 1 Odůvodnění
- 2 Příprava
- 3 použití
- 3.1 Antibiogramová technika
- 3.2 Strategické umístění disků na agaru Müeller Hinton
- 4 Příčiny chybných výsledků
- 5 Omezení
- 6 Kontrola kvality
- 7 Reference
Základ
Protože je to neselektivní výživné médium, je vynikající pro růst většiny patogenních bakterií..
Na druhé straně jeho jednoduché složení způsobuje, že látky na něm snadno difundují, což je základní charakteristikou pro test citlivosti diskovou difúzní metodou..
Další z jeho charakteristik je, že obsahuje malé množství inhibitorů, což umožňuje účinné hodnocení sulfonamidů, trimethoprimu a tetracyklinů..
Je však třeba mít na paměti, že médium musí splňovat určité podmínky, aby bylo zajištěno jeho správné fungování, včetně:
Úprava pH, hloubky agaru a vhodné koncentrace thyminu, thymidinu, Ca++, Mg++ a Zn++.
Musíte také vědět, že metodika je standardizovaná, a proto musí být splněny všechny parametry, například:
Koncentrace inokula, koncentrace a konzervace antibiotických disků, umístění příslušného počtu disků na agaru, vzdálenost mezi jednotlivými disky, strategické umístění určitých antibiotik, atmosféra, teplota a doba inkubace.
Příprava
Naváží se 37 g dehydratovaného média Müeller Hinton a rozpustí se v 1 litru destilované vody. Zahřejte médium za míchání, aby se napomohlo rozpuštění. Vařte 1 minutu.
Autoklávujte pro sterilizaci při 121 ° C po dobu 15 minut. Při vyjímání z autoklávu by se baňka měla ochladit ve vodní lázni o teplotě 50 ° C. Nalijte 25 až 30 ml do sterilních Petriho misek o průměru 10 cm.
Desky by měly mít průměrnou tloušťku 4 mm (ideální), s povoleným rozsahem 3-5 mm.
Je-li žádoucí připravit krevní agar za použití agaru Müeller Hinton jako základu, nalijte 5% sterilní a defibrinovanou jehněčí krev před podáváním na misky..
Konečné pH média by mělo být mezi 7,2 až 7,4.
Investujte a uchovávejte v chladničce až do použití. Před použitím nechte destičku ohřát na pokojovou teplotu.
Barva připraveného média je světle béžová.
Aplikace
Používá se k provedení testu antibiogramu nebo citlivosti na antibiotika u většiny rychle rostoucích nenáročných patogenů.
Pokud je agar doplněn krví, používá se k provádění antibiogramu náročných mikroorganismů, jako jsou: Streptococcus pneumoniae, Haemophilus sp, Neisseria meningitidis, mezi ostatními. Používá se také k izolaci Legionella pneumophila.
Antibiogramová technika
Před provedením antibiogramu musí být připraven bakteriální roztok odpovídající 1,5 x 10.8 buňky.
K tomu se odeberou 3 až 4 kolonie čisté kultury a suspendují se v bujónu sójové tryptikázy nebo v bujónu Müeller Hinton, inkubují se 2 až 6 hodin a koncentrace se upraví sterilním fyziologickým roztokem, ve srovnání se standardem Mac Farland 0,5 %.
Pokud požadují mikroorganismy, mohou být kolonie suspendovány přímo až do koncentrace 0,5% Mac Farland. Následně se deska Müeller Hinton vyseje tamponem impregnovaným připraveným bakteriálním roztokem..
Za tímto účelem je tampon ponořen do roztoku a poté je přebytečná kapalina odstraněna přitlačením ke stěnám zkumavky. Bezprostředně poté se tampon nechá projít celým povrchem a nezanechá žádná místa nedotčená, poté se destička mírně otočí a znovu se naočkuje. Operace se opakuje ještě dvakrát.
Nechejte 10 minut stát a poté připojte disky s antibiotiky pomocí sterilních kleští, přičemž mezi nimi zůstane mezera 24 mm. Po umístění každého disku na agar jej jemně přitlačte kleštěmi, abyste se ujistili, že jsou dobře přilepeny..
Jakmile je proces dokončen, je destička převrácena a inkubována při 35-37 ° C v aerobióze po dobu 16 až 18 hodin. Pokud se jedná o náročný mikroorganismus, může vyžadovat mikroaerofilii a pokud antibiogram obsahuje disky s oxacilinem, je třeba jej přečíst po 24 hodinách..
Pravítko se používá k měření průměru každé halo. Výsledky by měly být zaznamenány v mm. Získané hodnoty jsou následně korelovány s tabulkami řezných bodů publikovanými v aktuální příručce CLSI..

Nahlásit jako citlivé (S), střední (I) nebo rezistentní (R).
Antibiotika se vybírají podle izolovaného mikroorganismu a typu infekce, která způsobuje.
Někdy je třeba vzít v úvahu strategické umístění antibiotik, aby se prokázaly fenotypové vzorce rezistence.
Strategické umístění disků na agaru Müeller Hinton
U enterobakterií by měl být disk s kyselinou klavulanovou umístěn proti cefalosporinům 3. a 4. generace. Rozšíření ve tvaru vejce naznačuje, že kmen je producentem beta-laktamáz s rozšířeným spektrem (ESBL). To znamená, že pacient by neměl být léčen žádnými cefalosporiny..
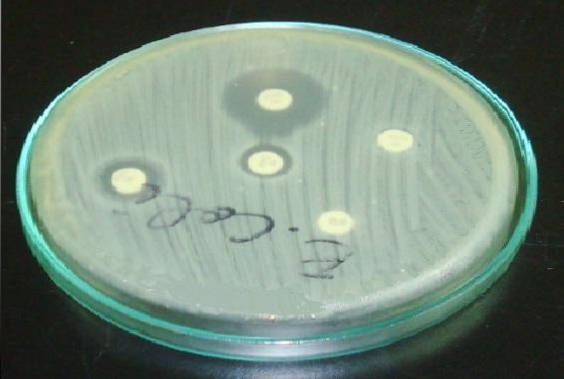
U Staphylococcus je důležité umístit disk s erythromycinem nebo azithromycinem před disk s klindamycinem (D-test).
Rezistentní halo v erythromycinu a zploštění v klindamycinovém halo naznačuje, že kmen má kmenově indukovatelnou rezistenci na klindamycin (ICR). To znamená, že léčba klindamycinem nebude účinná..
Při hledání indukovatelných kmenů AMP C u Enterobacteriaceae a některých nefermentujících gramnegatních tyčinkách jsou disky ceftazidimu, cefoxitinu nebo piperacilinu tazobaktanu otočeny proti disku imipenem ve vzdálenosti 27 mm.
Zploštělá halo na jednom z disků směřujících k imipenemu indikuje přítomnost indukovatelného AMP C.
Pro hledání konstitutivního C-AMP je 500 ug kloxacilinového disku potažen ceftazidimem (30 ug) a cefotaximem (30 ug) ve vzdálenosti 25 mm. Rozšířená halo v kterémkoli z cefalosporinů naznačuje pozitivitu.
Kloxacilinový disk může být také nahrazen 9 mm diskem filtračního papíru Whatman č. 6 impregnovaného kyselinou fenylboritou (400 ug) se vzdáleností 18 mm. Interpretuje se stejně jako předchozí.
Nakonec prozkoumat produkci metallobetalaktamáz zejména v Pseudomonas aeruginosa, Použije se disk impregnovaný 10 ul kyseliny ethylendiamintetraoctové (EDTA 750 μg) a kyseliny thioglykolové (SMA 300 μg), který je obrácen k diskům imipenem a meropenem, ve vzdálenosti 15 mm.
Test je pozitivní, pokud dojde k rozšíření halos imipenemu nebo meropenemu směrem k disku EDTA / SMA. Tento výsledek musí být potvrzen upraveným Hodgeovým testem..
Tato metoda spočívá v naočkování kmene Escherichia coli ATCC 25922 na desce Müeller Hinton. Disk imipenemu je umístěn do středu destičky a poté je vytvořen pruh z disku směrem k obvodu s kmenem P. aeruginosa podezřelý. Na misku lze testovat až 4 kmeny.
Test bude pozitivní, pokud kolem strií existuje zóna zkreslení imipenemové halo.
Příčiny chybných výsledků
-Špatně konzervované disky s antibiotiky mohou způsobit falešnou rezistenci. Například disk oxacilinu je velmi citlivý na změny teploty..
-Hodnota pH média pod uvedenou hodnotou (kyselá) produkuje menší halo v aminoglykosidech a makrolidech (riziko falešné rezistence) a větší halo v penicilinu, tetracyklinu a novobiocinu (riziko falešné citlivosti).
-Pokud je pH vyšší než uvedené (alkalické), jsou účinky popsané výše obráceny.
-Média se zvýšenou koncentrací thyminu a thymidinu mají vliv tím, že významně snižují inhibiční halo sulfonamidů a trimethoprimu..
-Vysoké koncentrace vápníku a hořčíku produkují falešnou rezistenci aminoglykosidů, polymyxinu B a tetracyklinů proti kmenům Pseudomonas aeruginosa.
-Nízké koncentrace vápníku a hořčíku produkují falešné citlivosti aminoglykosidů, polymyxinu B a tetracyklinů na kmeny Pseudomonas aeruginosa.
-Přítomnost zinku ovlivňuje výsledky karbapenemových disků (imipenem, meropenem a ertapenem).
-Tloušťka média pod 3 mm bude produkovat falešné výsledky citlivosti, zatímco tloušťka nad 5 bude produkovat falešný odpor.
-Mobilizace disků v antibiogramu způsobí deformaci halo, protože vypouštění antibiotik je okamžité.
- Velmi slabá inokula ovlivňují výsledky, protože na agaru nedojde k rovnoměrnému nebo splývavému růstu, což je nezbytná podmínka pro měření inhibičních halo, navíc k tomu, že halo může dávat větší než normální.
-Příliš nabitá inokula mohou dávat menší než běžné halo.
-Nerespektování vzdálenosti mezi disky způsobí, že se jedna svatozář překrývá s druhou a nelze je správně přečíst.
-Inkubujte s COdva zvyšuje velikost halo tetracyklinových a meticilinových disků.
-Inkubace při teplotách nižších než 35 ° C vytváří větší halo.
-Přidání krve zmenšuje velikost sulfonamidového halo.
Omezení
Citlivost antibiotika prokázaná na antibiogramu proti mikroorganismu (in vitro) není záruka, že to bude fungovat in vivo.
QA
Abychom věděli, zda médium obsahuje dostatečné množství thyminu, je třeba pěstovat kmen Enterococcus faecalis ATCC 29212 a otestujte citlivost na trimethoprim sulfamethoxazol (SXT), musí být dostatečná halo nebo větší než 20 mm.
Reference
- „Müller-Hintonův agar.“ Wikipedia, The Free Encyclopedia. 16. listopadu 2018, 12:23 UTC. 27. ledna 2019, 04:22
- Forbes B, Sahm D, Weissfeld A. (2009). Bailey & Scott mikrobiologická diagnostika. 12 ed. Redakční Panamericana S.A. Argentina.
- Cona E. Podmínky pro dobrou studii citlivosti agarovým difúzním testem. Rev Chil Infect, 2002; 19 (2): 77-81
- Laboratoř Difco Francisco Soria Melguizo. Müeller Hintonův agar s 5% ovčí krve. 2009. Dostupné na: http://f-soria.es
- BD Müeller Hinton II Agar Laboratory. 2017. Dostupné na: .bd.com
- Britannia Laboratories. Müeller Hintonův agar. 2015. Dostupné na: britanialab.com
- Koneman E, Allen S, Janda W, Schreckenberger P, Winn W. (2004). Mikrobiologická diagnostika. 5. vyd. Redakční Panamericana S.A. Argentina.
- Martínez-Rojas D. Betalaktamázy typu AmpC: Obecnosti a metody fenotypové detekce. Soc. Ven. Microbiol. 2009; 29 (2): 78-83. K dispozici na: scielo.org.
- Perozo A, Castellano M, Ling E, Arraiz N. Fenotypová detekce metallobetalaktamáz v klinických izolátech Pseudomonas aeruginosa. Kasmera, 2012; 40 (2): 113-121. K dispozici na: scielo.org.



Zatím žádné komentáře