
Vzorec bromidu hlinitého, vlastnosti a použití
The bromid hlinitý Je to sloučenina složená z atomu hliníku a různého počtu atomů bromu. Vzniká v závislosti na počtu valenčních elektronů, které hliník má.
Jelikož se jedná o sloučeninu spojenou kovem (hliníkem) a nekovem (bromem), vytvářejí se kovalentní vazby, které dávají strukturám velmi dobrou stabilitu, ale bez dosažení iontové vazby..
Bromid hlinitý je látka, která se běžně vyskytuje v pevném stavu s krystalickou strukturou.
Barvy různých bromidů hliníku vypadají jako světle žluté barvy různých odstínů a někdy se objevují bez zjevné barvy.
Barva závisí na schopnosti odrazu světla sloučeniny a mění se v závislosti na strukturách, které jsou vytvořeny, a formách, které má..
Pevný stav těchto sloučenin krystalizuje, takže mají dobře definované struktury se vzhledem podobným mořské soli, ale lišící se barvou..
Vzorec
Bromid hlinitý je tvořen atomem hliníku (Al) a různými množstvími atomů bromu (Br), v závislosti na valenčních elektronech, které hliník má..
Z tohoto důvodu lze obecný vzorec pro bromid hlinitý psát takto: AlBrx, kde „x“ je počet atomů bromu, které se váží na hliník.
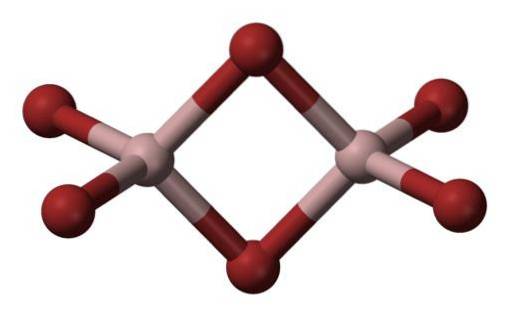
Nejběžnější formou, ve které se vyskytuje, je Al2Br6, což je molekula se dvěma atomy hliníku jako hlavními bázemi struktury..
Vazby mezi nimi jsou tvořeny dvěma bromy uprostřed, takže každý atom hliníku má ve své struktuře čtyři atomy bromu, ale zase sdílejí dva.
Vlastnosti
Díky své povaze je vysoce rozpustný ve vodě, ale na rozdíl od jiných typů látek je také částečně rozpustný ve sloučeninách, jako je methanol a aceton..
Má molekulovou hmotnost 267 g / mol a je tvořen kovalentními vazbami.
Bromid sodný dosáhne svého bodu varu při 255 ° C a svého bodu tání dosáhne při 97,5 ° C.
Další charakteristikou této sloučeniny je, že při odpařování emituje toxiny, proto se nedoporučuje pracovat s ní při vysokých teplotách bez odpovídající ochrany a příslušných bezpečnostních znalostí..
Aplikace
Jedno z použití tohoto typu látky vzhledem k jeho kovové a nekovové povaze je použití látek při zkouškách chemické čistoty..
Testování čistoty je velmi důležité při určování kvality reagencií a při výrobě produktů, s nimiž jsou lidé spokojeni..
Ve vědeckém výzkumu se používá velmi variabilně. Například pro vytváření složitých struktur, činidel při syntéze dalších cenných chemických produktů, při hydrogenaci dihydroxynaftalenů a při selektivitě reakcí, mimo jiné..
Tato sloučenina není komerčně populární. Jak je vidět výše, má některé aplikace, které jsou velmi specifické, ale pro vědeckou komunitu velmi zajímavé..
Reference
- Chang, R. (2010). Chemie (10. vydání) McGraw-Hill Interamericana.
- Krahl, T. a Kemnitz, E. (2004). Amorfní fluorid hlinitý bromid (ABF). Angewandte Chemie - mezinárodní vydání, 43(48), 6653-6656. doi: 10,1002 / anie.200460491
- Golounin, A., Sokolenko, V., Tovbis, M., & Zakharova, O. (2007). Komplexy nitronaftolů s bromidem hlinitým. Russian Journal of Applied Chemistry, 80(6), 1015-1017. doi: 10.1134 / S107042720706033X
- Koltunov, K.Y. (2008). Kondenzace naftalendiolů s benzenem v přítomnosti bromidu hlinitého: Efektivní syntéza 5-, 6- a 7-hydroxy-4-fenyl-1- a 2-tetralonů. Čtyřstěn dopisy, 49(24), 3891-3894. doi: 10.1016 / j.tetlet.2008.04.062
- Guo, L., Gao, H., Mayer, P. a Knochel, P. (2010). Příprava organohlinitých činidel z propargylových bromidů a hliníku aktivovaného PbCl2 a jejich regio- a diastereoselektivní přidání k karbonylovým derivátům. Chemistry-a European Journal, 16(32), 9829-9834. doi: 10,1002 / chem.201000523
- Ostashevskaya, L. A., Koltunov, K. Y., & Repinskaya, I. B. (2000). Iontová hydrogenace dihydroxynaftalenů s cyklohexanem v přítomnosti bromidu hlinitého. Russian Journal of Organic Chemistry, 36(10), 1474-1477.
- Iijima, T. a Yamaguchi, T. (2008). Účinná regioselektivní karboxylace fenolu na kyselinu salicylovou se superkritickým CO2 v přítomnosti bromidu hlinitého. Journal of Molecular Catalysis A: Chemical, 295(1-2), 52-56. doi: 10.1016 / j.molcata.2008.07.017
- Murachev, V. B., Byrikhin, V. S., Nesmelov, A. I., Ezhova, E. A., & Orlinkov, A. V. (1998). 1H NMR spektroskopická studie kationtového iniciačního systému terc-butylchlorid - bromid hlinitý. Ruský chemický bulletin, 47(11), 2149-2154.


Zatím žádné komentáře