
Karbid křemíku, chemická struktura, vlastnosti a použití

The Karbid křemíku Je to kovalentní pevná látka složená z uhlíku a křemíku. Má velkou tvrdost s hodnotou 9,0 až 10 podle Mohsovy stupnice a jeho chemický vzorec je SiC, což může naznačovat, že uhlík je vázán na křemík kovalentní trojnou vazbou s kladným nábojem (+) na Si a a záporný náboj (-) na uhlíku (+Ano≡C-).
Ve skutečnosti jsou vazby v této sloučenině zcela odlišné. Objevil ji v roce 1824 švédský chemik Jön Jacob Berzelius, když se pokoušel syntetizovat diamanty. V roce 1893 francouzský vědec Henry Moissani objevil minerál, jehož složení obsahovalo karbid křemíku.

Tento objev byl učiněn při zkoumání vzorků hornin z kráteru meteoritu v Devil's Canyon, USA. Tento minerál pojmenoval moissanit. Na druhou stranu Edward Goodrich Acheson (1894) vytvořil metodu syntézy karbidu křemíku reagujícího písku nebo křemene vysoké čistoty s ropným koksem..
Goodrich pojmenoval produkt získaný karborundem (nebo karborundiem) a založil společnost na výrobu brusiv.
Rejstřík článků
- 1 Chemická struktura
- 2 Vlastnosti
- 2.1 Obecné vlastnosti
- 2.2 Tepelné vlastnosti
- 2.3 Mechanické vlastnosti
- 2.4 Elektrické vlastnosti
- 3 použití
- 3.1 Jako brusivo
- 3.2 Ve formě strukturované keramiky
- 3.3 Jiná použití
- 4 Odkazy
Chemická struktura
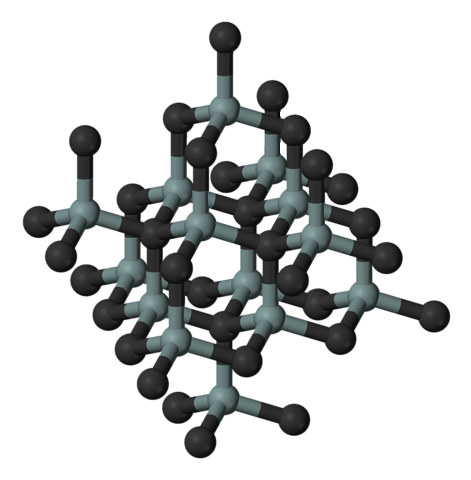
Obrázek výše ilustruje kubickou a krystalickou strukturu karbidu křemíku. Toto uspořádání je stejné jako u diamantu, navzdory rozdílům v atomových poloměrech mezi C a Si..
Všechny vazby jsou silně kovalentní a směrové, na rozdíl od iontových pevných látek a jejich elektrostatických interakcí.
SiC tvoří molekulární čtyřstěn; to znamená, že všechny atomy jsou spojeny se čtyřmi dalšími. Tyto čtyřboké jednotky jsou spojeny kovalentními vazbami, které přijímají vrstvené krystalické struktury..
Tyto vrstvy mají také svá vlastní krystalová uspořádání, která jsou tří typů: A, B a C.
To znamená, že vrstva A se liší od B a druhá od C. Krystal SiC tedy spočívá ve skládání sledu vrstev, což je jev známý jako polytypismus..
Například kubický polytyp (podobný jako u diamantu) se skládá z hromady vrstev ABC, a proto má krystalickou strukturu 3C..
Další hromádky těchto vrstev také generují další struktury, mezi těmito romboedrickými a šestihrannými polytypy. Ve skutečnosti jsou krystalické struktury SiC nakonec „krystalickou poruchou“.
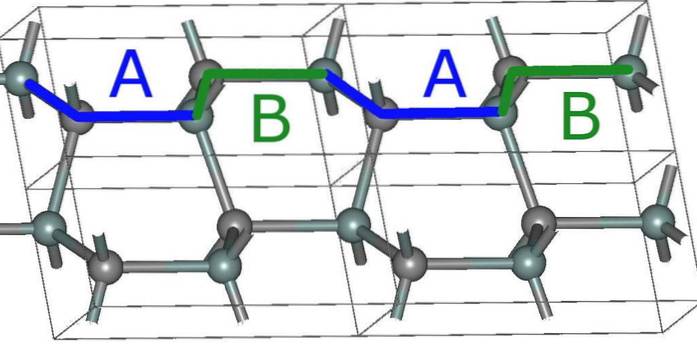
Nejjednodušší hexagonální struktura pro SiC, 2H (horní obrázek), je vytvořena jako výsledek skládání vrstev se sekvencí ABABA ... Po každých dvou vrstvách se sekvence opakuje, a odtud pochází číslo 2.
Vlastnosti
Obecné vlastnosti
Molární hmotnost
40,11 g / mol
Vzhled
Liší se podle způsobu získání a použitých materiálů. Může to být: žluté, zelené, černomodré nebo duhové krystaly.
Hustota
3,16 g / cm3
Bod tání
2830 ° C.
Index lomu
2.55.
Krystaly
Existuje polymorfismus: šestihranné krystaly αSiC a krychlové krystaly βSiC.
Tvrdost
9 až 10 podle Mohsovy stupnice.
Odolnost proti chemickým látkám
Je odolný vůči působení silných kyselin a zásad. Karbid křemíku je navíc chemicky inertní..
Tepelné vlastnosti
- Vysoká tepelná vodivost.
- Odolává vysokým teplotám.
- Vysoká tepelná vodivost.
- Nízký koeficient lineární tepelné roztažnosti, takže vydrží vysoké teploty s nízkou roztažností.
- Odolný vůči tepelnému šoku.
Mechanické vlastnosti
- Vysoká odolnost proti stlačení.
- Odolný proti oděru a korozi.
- Je to lehký materiál s velkou pevností a odolností.
- Udržuje si pružnou odolnost při vysokých teplotách.
Vlastnosti elektrický
Jedná se o polovodič, který může plnit své funkce při vysokých teplotách a extrémních napětích, s malým rozptýlením své energie do elektrického pole..
Aplikace
Jako brusivo
- Karbid křemíku je polovodič schopný odolat vysokým teplotám, gradientům vysokého napětí nebo elektrickému poli 8krát více, než vydrží křemík. Z tohoto důvodu je užitečný při konstrukci diod, tranzistorů, potlačovačů a vysokoenergetických mikrovlnných zařízení..
- Ze sloučeniny byly vyrobeny světelné diody (LED) a detektory pro první rádia (1907). V současné době byl karbid křemíku při výrobě LED žárovek nahrazen nitridem galia, který vyzařuje 10 až 100krát jasnější světlo.
- V elektrických systémech se karbid křemíku používá jako hromosvod v elektrických energetických systémech, protože mohou regulovat jeho odpor regulací napětí na něm..
Ve formě strukturované keramiky
- V procesu známém jako slinování se částice karbidu křemíku - stejně jako částice společníků - zahřívají na teplotu nižší, než je teplota tání této směsi. Zvyšuje tak odolnost a pevnost keramického předmětu vytvářením silných vazeb mezi částicemi..
- Konstrukční keramika z karbidu křemíku má širokou škálu aplikací. Používají se v kotoučových brzdách a spojkách motorových vozidel, ve filtrech pevných částic a jako přísada do olejů ke snížení tření.
- Použití konstrukční keramiky z karbidu křemíku se rozšířilo v částech vystavených vysokým teplotám. Jedná se například o hrdlo injektorů raket a válečky pecí..
- Díky kombinaci vysoké tepelné vodivosti, houževnatosti a vysoké teplotní stability jsou součásti trubek výměníku tepla vyrobeny z karbidu křemíku..
- Konstrukční keramika se používá ve vstřikovačích pískování, těsněních vodních čerpadel automobilů, ložiskách a vytlačovacích lisech. Je to také materiál pro kelímky, který se používá při tavení kovů..
- Je součástí topných prvků používaných při tavení skla a neželezných kovů, jakož i při tepelném zpracování kovů.
Jiná použití
- Může být použit při měření teploty plynů. V technice známé jako pyrometrie se vlákno z karbidu křemíku zahřívá a emituje záření, které koreluje s teplotou v rozmezí 800-2500 ° K..
- Používá se v jaderných elektrárnách k zabránění úniku štěpného materiálu.
- Při výrobě oceli se používá jako palivo.
Reference
- Nicholas G. Wright, Alton B. Horsfall. Karbid křemíku: Návrat starého přítele. Materiálové záležitosti, svazek 4, článek 2. Citováno dne 5. května 2018, z: sigmaaldrich.com
- John Faithfull. (Únor 2010). Krystaly karborunda. Citováno dne 5. května 2018 z: commons.wikimedia.org
- Charles & Colvard. Polytypismus a moissanit. Citováno dne 5. května 2018 z: moissaniteitalia.com
- Vědec v oboru materiálů. (2014). Struktura SiC2 [Postava]. Citováno dne 5. května 2018 z: commons.wikimedia.org
- Wikipedia. (2018). Karbid křemíku. Citováno dne 5. května 2018 z: en.wikipedia.org
- Navarro SiC. (2018). Karbid křemíku. Citováno dne 5. května 2018 z: navarrosic.com
- University of Barcelona. Karbid křemíku, SiC. Citováno dne 5. května 2018 z: ub.edu
- CarboSystem. (2018). Karbid křemíku. Citováno dne 5. května 2018 z: carbosystem.com



Zatím žádné komentáře