
Struktura sirouhlíku (CS2), vlastnosti, použití, rizika
The sirouhlík Je to sloučenina vytvořená spojením atomu uhlíku (C) a dvou atomů síry (S). Jeho chemický vzorec je CSdva. Je to bezbarvá nebo světle žlutá kapalina s nepříjemným zápachem kvůli nečistotám, které obsahuje (sloučeniny síry). Když je čistý, jeho vůně je jemná a sladká, podobně jako chloroform nebo ether..
Přirozeně pochází z působení slunečního světla na organické molekuly nacházející se v mořské vodě. Kromě toho se vyrábí v bažinných vodách a je také vyloučen ze sopek spolu s dalšími plyny.
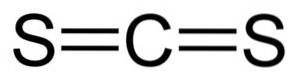
Sulfid uhličitý je těkavá kapalina a je také vysoce hořlavý, proto by měl být chráněn před plameny a jiskrami nebo před zařízeními, která je mohou produkovat, dokonce i před elektrickými žárovkami..
Má schopnost rozpouštět velké množství sloučenin, materiálů a prvků, jako je fosfor, síra, selen, pryskyřice, laky atd. Proto najde využití jako rozpouštědlo.
Je také prostředníkem v různých průmyslových chemických reakcích, jako je výroba hedvábí nebo umělého hedvábí..
Musí se s ním zacházet opatrně as ochrannými nástroji, protože je velmi toxický a nebezpečný.
Rejstřík článků
- 1 Struktura
- 2 Názvosloví
- 3 Vlastnosti
- 3.1 Fyzický stav
- 3,2 Molekulová hmotnost
- 3.3 Bod tání nebo tuhnutí
- 3.4 Bod varu
- 3.5 Bod vzplanutí
- 3.6 Teplota samovznícení
- 3.7 Hustota
- 3.8 Tlak par
- 3.9 Rozpustnost
- 3.10 Chemické vlastnosti
- 4 Získání
- 4.1 Přítomnost v přírodě
- 5 použití
- 5.1 V chemickém průmyslu
- 5.2 Při výrobě hedvábí a celofánu
- 5.3 Při výrobě tetrachlormethanu
- 5.4 V různých aplikacích
- 5.5 Starověké použití
- 6 Rizika
- 7 Reference
Struktura
Sirouhlík má na jedné straně jeden atom uhlíku a dva atomy síry..
Vazby mezi atomem uhlíku a atomy síry jsou kovalentní a dvojité, proto jsou velmi silné. Molekula CSdva má lineární a symetrickou strukturu.

Nomenklatura
- Sirouhlík
- Sirouhlík
- Dithiokarbonanhydrid
Vlastnosti
Fyzický stav
Bezbarvá až nažloutlá kapalina.
Molekulární váha
76,15 g / mol
Bod tání nebo tuhnutí
-110,8 ° C
Bod varu
46,0 ° C
Bod vzplanutí
-30 ° C (metoda uzavřeného kelímku).
teplota samovznícení
90 ° C
Hustota
Kapalina = 1,26 g / cm3 při 20 ° C.
Pára = 2,67krát vyšší než u vzduchu.
Jeho páry jsou více než dvakrát těžší než vzduch a kapalina je těžší než voda.
Tlak páry
279 mmHg při 25 ° C.
Jedná se o vysoký tlak par.
Rozpustnost
Velmi málo rozpustný ve vodě: 2,16 g / l při 25 ° C. Rozpustný v chloroformu. Mísitelný s ethanolem, methanolem, etherem, benzenem, chloroformem a tetrachlormethanem.
Chemické vlastnosti
CSdva snadno se odpařuje při pokojové teplotě, protože jeho bod varu je velmi nízký a tlak par je velmi vysoký.
Sirovodík je extrémně hořlavý. Jeho páry se velmi snadno vznítí, dokonce i při žáru elektrické žárovky. To znamená, že reaguje s kyslíkem velmi rychle:
CSdva + 3 O.dva → COdva + 2 SOdva
Skutečnost, že při pokojové teplotě má vysoký tlak par, činí nebezpečným být poblíž plamene.
Při zahřátí na rozklad může snadno explodovat a uvolňovat toxické plyny oxidu siřičitého. Při teplotě nad 90 ° C se samovolně vznítí.
Při dlouhodobém skladování se rozkládá. Napadá měď a její slitiny. Reaguje také s některými plasty, kaučuky a povlaky.
Reaguje za určitých podmínek s vodou za vzniku karbonylsulfidu OCS, oxidu uhličitého COdva a sirovodík HdvaS:
CSdva + HdvaO → OCS + HdvaS
CSdva + 2 hdvaO → COdva + 2 hdvaS
S alkoholy (ROH) v alkalickém prostředí tvoří xantháty (RO-CS-SNa):
CSdva + ROH + NaOH → HdvaO + RO-C (= S) -SNa
Získávání
Sulfid uhličitý se komerčně připravuje reakcí síry s uhlíkem. Proces se provádí při teplotách 750-900 ° C.
C + 2 S → CSdva
Místo uhlí lze použít také metan nebo zemní plyn a dokonce se použil ethan, propan a propylen, přičemž v tomto případě reakce probíhá při 400-700 ° C s vysokým výtěžkem..
Může být také připraven reakcí zemního plynu se sirovodíkem HdvaS při velmi vysoké teplotě.
Přítomnost v přírodě
CSdva je to přírodní produkt přítomný v atmosféře ve velmi malém množství (stopy). Vyrábí se fotochemicky v povrchových vodách.
Působení slunečního světla na určité sloučeniny přítomné v mořské vodě, jako je cystein (aminokyselina), vede k tvorbě sirouhlíku.

Rovněž se uvolňuje přirozeně během sopečných erupcí a nachází se v malém množství v bažinách..
Normálně jsme vystaveni dýchání ve velmi malém množství a je přítomno v některých potravinách. Vyskytuje se také v cigaretovém kouři.
V prostředí se slunečním světlem rozkládá. Po zemi se pohybuje skrz něj. Některé mikroorganismy v půdě ji rozkládají.
Aplikace
V chemickém průmyslu
Sulfid uhličitý je důležitá chemická sloučenina, protože se používá k přípravě dalších chemických látek. Může působit jako chemický meziprodukt.
Používá se také jako procesní rozpouštědlo, například k rozpuštění fosforu, síry, selenu, bromu, jodu, tuků, pryskyřic, vosků, laků a gum.
Umožňuje mimo jiné výrobu léčiv a herbicidů.
Při výrobě hedvábí a celofánu
S CSdva Připravují se xantáty, což jsou sloučeniny používané při výrobě hedvábí a celofánu.
K získání umělého hedvábí nebo umělého hedvábí se používá celulóza, která je ošetřena alkáliemi a sirouhlíkem CSdva a je transformován na xanthát celulózy, rozpustný v alkáliích. Toto řešení je viskózní a proto se nazývá „viskózní“.
Viskóza je vytlačována přes velmi malé otvory v kyselé lázni. Zde se xanthát celulózy přeměňuje zpět na celulózu, která je nerozpustná a tvoří se dlouhé a lesklé nitě..
Vlákna nebo vlákna lze spřádat do materiálu známého jako umělé hedvábí.
(1) Celulóza + NaOH → Alkalická celulóza
ROH + NaOH → RONa
(2) Alkali-celulóza + sirouhlík → xanthát celulózy
RONa + S = C = S → RO-C (= S) -SNa
(3) xanthát celulózy + kyselina → celulóza (vlákna)
Kyselina RO-C (= S) -SNa + → ROH

Pokud se celulóza vysráží průchodem xanthátu úzkou štěrbinou, celulóza se regeneruje ve formě tenkých desek, které tvoří celofán. To je změkčeno glycerolem a používá se jako ochranný film pro předměty.

Při výrobě tetrachlormethanu
Sulfid uhličitý reaguje s chlorem Cldva za vzniku chloridu uhličitého CCl4, což je důležité nehořlavé rozpouštědlo.
CSdva + 3 Cldva → CCl4 + SdvaCldva
V různých aplikacích
Sulfid uhličitý se podílí na vulkanizaci kaučuků za studena, slouží jako meziprodukt při výrobě pesticidů a používá se k výrobě katalyzátorů v ropném průmyslu a při výrobě papíru..
Xantháty připravené s CSdva se používají při minerální flotaci.
Starověké použití
CSdva je to jed pro živé organismy. Dříve to bylo používáno k ničení škůdců, jako jsou krysy, sviště a mravenci, nalití kapaliny do jakéhokoli uzavřeného prostoru, ve kterém tato zvířata žila (nory a mraveniště).
Pokud byly použity pro tento účel, husté toxické páry zničily veškerý živý organismus, který se nacházel v uzavřeném prostoru..
Používal se také jako antihelmintikum pro zvířata a pro eliminaci larev mouchy z břicha koní..
V zemědělství se používal jako insekticid a nematicid, k fumigaci půdy, k fumigaci školek, sýpek, sil a mlýnů na obiloviny. Postříkány byly také železniční vozy, lodě a čluny.

Všechna tato použití byla zakázána kvůli vysoké hořlavosti a toxicitě CSdva.
Rizika
CSdva je vysoce hořlavý. Mnoho z jejich reakcí může způsobit požár nebo výbuch. Směsi jeho par se vzduchem jsou výbušné. Při zapálení produkuje dráždivé nebo toxické plyny.
Sulfid uhličitý by neměl být nalit do kanalizace, protože v trubkách zůstává směs CSdva a vzduch, který může při náhodném zapálení způsobit výbuch.
Jeho páry se samovolně vznítí při kontaktu s jiskrami nebo horkými povrchy.
Sulfid uhličitý silně dráždí oči, kůži a sliznice.
Při vdechování nebo požití vážně ovlivňuje centrální nervový systém, kardiovaskulární systém, oči, ledviny a játra. Může být také absorbován kůží a způsobit poškození.
Reference
- NÁS. Národní lékařská knihovna. (2020). Sirouhlík. Obnoveno z pubchem.ncbi.nlm.nih.gov.
- Mopper, K. a Kieber, D.J. (2002). Fotochemie a cyklování uhlíku, síry, dusíku a fosforu. In Biogeochemistry of Marine Dissolved Organic Matter. Obnoveno ze sciencedirect.com.
- Meyer, B. (1977). Průmyslové využití síry a jejích sloučenin. Sulfid uhličitý. V síře, energii a životním prostředí. Obnoveno ze sciencedirect.com.
- Pohanish, R.P. (2012). C. Sirouhlík. V Sittig's Handbook of Toxic and Hazardous Chemicals and Carcinogens (šesté vydání). Obnoveno ze sciencedirect.com.
- Morrison, R.T. a Boyd, R.N. (2002). Organická chemie. 6. vydání. Prentice-Hall.
- Windholz, M. a kol. (redaktoři) (1983). Index společnosti Merck. Encyclopedia of Chemicals, Drugs, and Biologicals. Desáté vydání. Merck & CO., Inc..



Zatím žádné komentáře