
Struktura fosforečnanu sodného, vlastnosti, syntéza, použití

The Fosforečnan sodný je anorganická sůl, jejíž chemický vzorec je Na3PO4. Nazývá se také fosforečnan sodný (TSP): Fosforečnan sodný) nebo fosforečnan sodný, protože zcela chybí schopnost darovat vodíkové ionty H+.
Když se na něj odkazuje množným způsobem, fosforečnany sodné, vztahuje se na celé kompendium solí, hydratovaných nebo ne, pocházejících z elektrostatických interakcí mezi Na+ a PO43-. Některé z těchto solí dokonce sestávají z pyrofosforečnanů sodných nebo anorganických polymerů, které mají PO43- jako monomer.

Proto, pokud není uvedena specifikace, bude vždy odkazovat na Na3PO4, a ne NaHdvaPO4, NadvaHPO4, Na4PdvaNEBO7 ani na žádnou jinou sůl.
Obrázek výše ukazuje vzhled fosforečnanu sodného, který má bílé krystaly podobné běžné nebo stolní soli, nebo je zakoupen jako bílý, amorfně vypadající prášek. Pak3PO4 je schopen tvořit různé hydráty, přičemž je Na3PO412HdvaNebo ten, který je uváděn na trh nejvíce.
Najde uplatnění hlavně v potravinářském průmyslu, v detergentech, sportovních doplňcích a slouží jako hyperosmotické projímadlo.
Rejstřík článků
- 1 Chemická struktura
- 2 Vlastnosti
- 2.1 Fyzický vzhled
- 2.2 Teplota tání
- 2.3 Bod varu
- 2.4 Rozpustnost ve vodě
- 2.5 Hustota
- 2.6 Stabilita
- 2,7 pH
- 3 Syntéza
- 4 použití
- 4.1 Jídlo
- 4.2 Čisticí prostředky
- 4.3 Léčivé
- 5 Reference
Chemická struktura
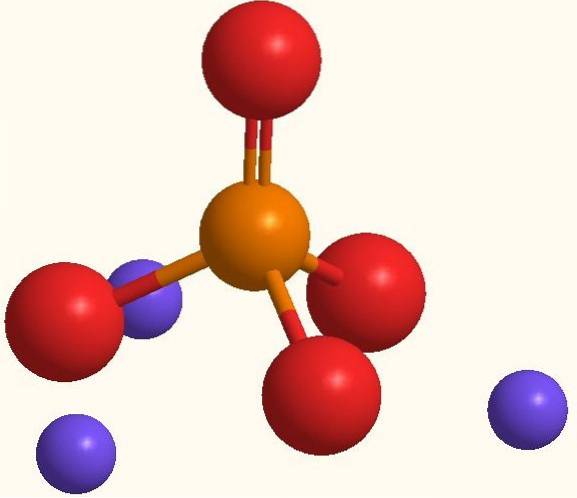
Stejný vzorec Na3PO4 označuje, že pro každý anion PO43- existují tři Na kationty+. Tyto ionty lze vidět na obrázku výše. Všimněte si, že PO43- má čtyřbokou geometrii a její atomy kyslíku nesou rezonanční záporný náboj, který přitahuje Na+ životního prostředí.
Podobně vzorec Na3PO4 zdůrazňuje, že jde o bezvodou sůl, takže v jejích krystalech nejsou obsaženy žádné molekuly vody. Elektrostatické přitažlivosti mezi Na+ a PO43- nakonec definují trigonální bílý krystal. Jeho iontová vazba je taková, že Na3PO4 má teplotu tání 1583 ° C, podstatně vyšší než teplota různých solí.
Jak Na+ jako PO43- Jsou to ionty, které lze vysoce hydratovat, aniž by to negativně ovlivnilo stabilitu krystalů.
Z tohoto důvodu mohou hydráty také krystalizovat; jeho teploty tání jsou však nižší než teploty tání bezvodé soli, protože intermolekulární vodíkové vazby ve vodě oddělují ionty a oslabují jejich interakce. V Na3PO412HdvaNebo například jeho teplota tání je 73,4 ° C, mnohem nižší než teplota tání Na3PO4.
Vlastnosti
Fyzický vzhled
Může se jevit jako definované bílé krystaly nebo jako prášek nebo granule stejné barvy. Všechna níže uvedená fyzikální množství se vztahují pouze na bezvodou sůl Na3PO4.
Bod tání
1583 ° C
Bod varu
100 ° C
Rozpustnost ve vodě
14,5 g / 100 ml při 25 ° C, a proto je považován za fosforečnan zcela rozpustný ve vodě. Je však nerozpustný v organických rozpouštědlech, jako je ethanol a sirouhlík..
Hustota
2,536 g / cm3 při 17,5 ° C.
Stabilita
Je to hygroskopická pevná látka. Proto by měl být skladován tak, aby nemohl být vystaven vlhkosti.
pH
Je to silně zásaditá sůl. Například jeho 0,1% vodný roztok již má pH 11,5. Tato vlastnost slouží k použití jako přísada do detergentů.
Syntéza
Jak se vyrábí nebo syntetizuje fosforečnan sodný? Za tímto účelem vycházíme z kyseliny fosforečné, H3PO4, nebo z fosforečnanu sodného na bázi dikyseliny, NaHdvaPO4.
V převážné většině syntéz je preferováno H3PO4. H tedy reaguje3PO4 s bází, která neutralizuje své tři OH skupiny, s přihlédnutím k tomu, že tato kyselina může být také zapsána jako PO (OH)3.
Bázou je přednostně hydroxid sodný, NaOH (v Německu), ale je také možné (a levnější) použít uhličitan sodný nebo uhličitan sodný, NadvaCO3 (ve Spojených státech). Rovnice pro obě neutralizační reakce jsou:
NadvaCO3 + H3PO4 → NadvaHPO4 + COdva + HdvaNEBO
NadvaHPO4 + NaOH → Na3PO4 + HdvaNEBO
Pamatujte, že při použití NadvaCO3 Na není získán3PO4 ale NadvaHPO4, který bude potřebovat následnou neutralizaci. Protože je reakční prostředí vodné, krystaluje Na3PO412HdvaNebo tedy musí být kalcinován, aby se odstranil jeho obsah vody a tím vznikla bezvodá sůl.
Pak3PO412HdvaNebo se vyznačuje „fúzováním“ svých krystalů do kompaktní hmoty, kterou je obtížné rozbít. Čím menší je velikost vašich krystalů, tím rychlejší bude jejich kalcinace.
Aplikace
Jídlo

Při použití fosforečnanu sodného je nevyhnutelné míchat Na3PO4 nebo na Na3PO412HdvaNebo, protože druhý je nejvíce komerčně dostupný hydrát. Například jeden z těchto dvou přispívá neškodně ionty (teoreticky) do potravin, do kterých jsou přidávány, obohacuje je fosfáty a zvyšuje jejich slanost současně..
V solí masa Na3PO412HdvaNebo zahrnuty, aby zůstaly déle čerstvé během skladování. Podobně se přidává jako emulgátor, takže směs oleje a vody „neřezává“, ale zůstává jednotná; a jako regulátor pH, protože pomáhá snižovat kyselost potravin (včetně obilovin).
Kromě toho se používá k zahuštění některých rajčatových omáček a k pečení koláčů nebo chleba (horní obrázek). Ten je způsoben Na3PO412HdvaNebo má tendenci uvolňovat vodní páru, což zvyšuje velikost pórů a objem moučného těsta..
Čistící prostředky
Fosforečnan sodný je dostatečně zásadní pro zmýdelnění některých tuků nebo olejů, s nimiž přichází do styku. Jeho alkalita se poté používá ke zlepšení působení detergentů, pokud povrch, který má být odmaštěn, není kovový, protože by ho mohly poškodit..
Výroba detergentů obohacených o fosforečnany však byla snížena v důsledku eutrofizace jezer a řek a tím i množení řas, které pokrývají jejich povrchy..
Také se z něj vyrábí dezinfekční prostředek: Na3PO41 / 4NaOCl11HdvaNebo, který se připravuje s použitím chlornanu sodného, NaOCl, místo NaOH nebo NadvaCO3 neutralizovat H3PO4.
Léčivý
Pak3PO4 vyvolává defekaci tím, že působí jako hyperosmotické projímadlo, které je nezbytné k vyčištění tlustého střeva předtím, než pacient podstoupí kolonoskopii. Na druhou stranu se také používá (přidává) do energetických doplňků.
Reference
- Shiver & Atkins. (2008). Anorganická chemie. (Čtvrté vydání). Mc Graw Hill.
- Národní centrum pro biotechnologické informace. (2019). Fosforečnan sodný. Databáze PubChem. CID = 24243. Obnoveno z: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2019). Fosforečnan sodný. Obnoveno z: en.wikipedia.org
- Curran M.P. & Plosker G.L. (2004). Perorální roztok fosforečnanu sodného: přehled jeho použití jako kolorektálního čističe. DOI: 10.2165 / 00003495-200464150-00009
- Corey Whelan. (22. prosince 2017). Fosforečnan sodný. Obnoveno z: healthline.com
- Jacobs, Joel B. Taborosi, Steve. (2019). Způsob výroby fosforečnanu sodného. Obnoveno z: freepatentsonline.com
- MaryAnn Marks. (2018). Proč je do naší stravy přidáván fosforečnan trisodný (TSP)? Obnoveno z: theingredientguru.com



Zatím žádné komentáře